2008 年至今,我国实施的" 新药创制" 重大专项在创新药研发方面取得丰硕成果。尤其自2015年以来,创新药物的政策环境不断优化,创新活力不断释放,中国的创新药进入了一个新的阶段,迎来了黄金收获期。 2021年仅第一季度国家药品监督管理局就已经批准了3个1类创新药。这些包括新的抗肺癌药甲磺酸伏美替尼片和普拉替尼胶囊以及新的抗乳腺癌药优替德隆注射液。根据世界卫生组织国际癌症研究机构(IARC)公布的数据显示2020年全球乳腺癌新发病例高达226万例,超过了肺癌的220万例,乳腺癌取代肺癌,成为全球第一大癌(见图1),并且中国的新发癌症人数位居全球第一(见图2)【1】。这意味着,这些新药在国内上市将为中国的肺癌和乳腺癌患者提供更多的治疗选择。
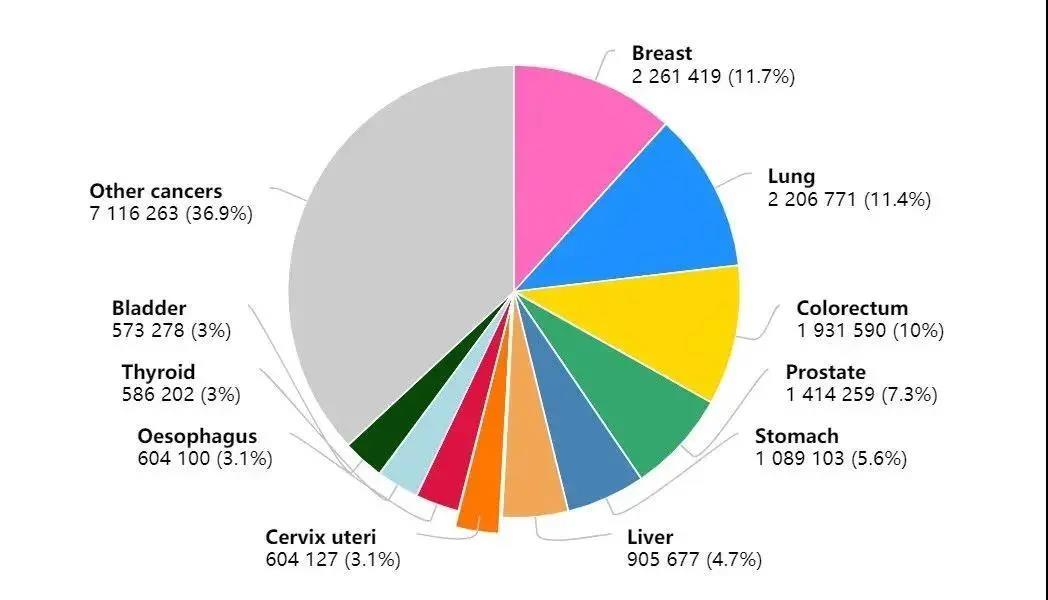
图1 2020年癌症新发病例数前十的癌症类型
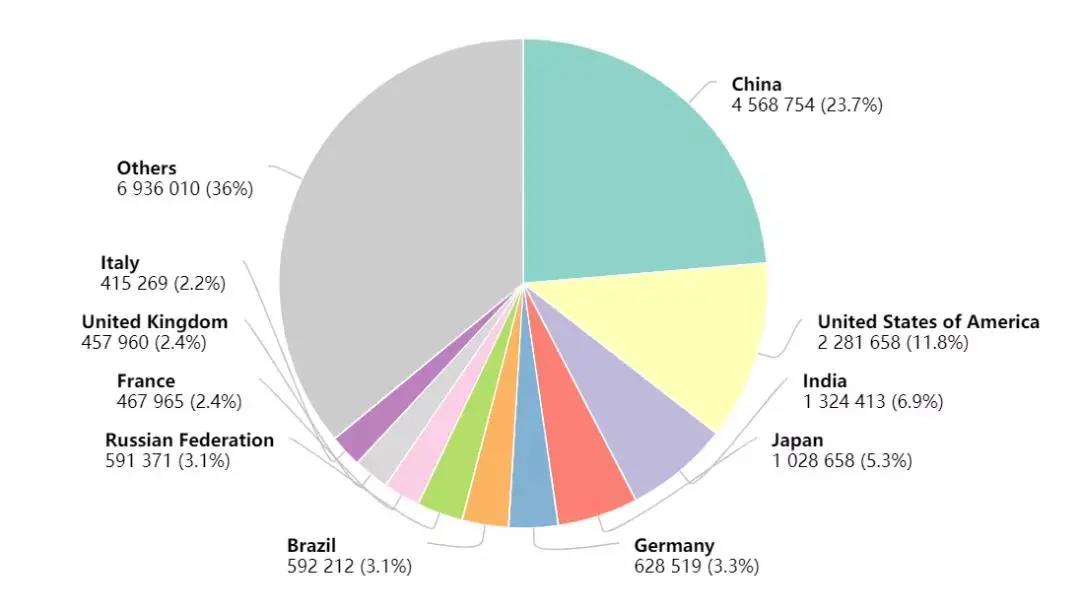
图2 2020年各国癌症新发病例数
下面本文将逐一介绍2021年第一季度NMPA批准的三个1类新药的药理学数据及临床意义。
一、甲磺酸伏美替尼(furmonertinib mesilate)
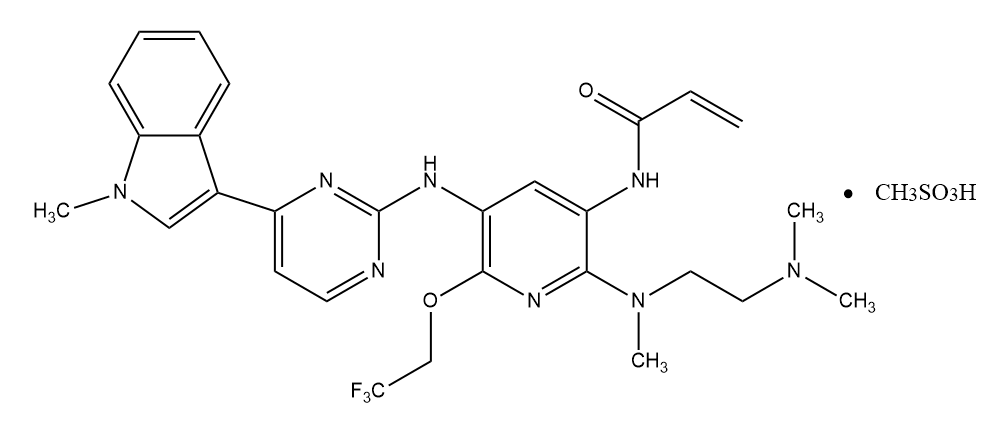
2021年3月3日,国家药品监督管理局发布公告,通过优先审评审批程序附条件批准上海艾力斯医药科技股份有限公司申报的1类创新药艾弗沙(甲磺酸伏美替尼)上市。该药是拥有自主知识产权专利的药物。艾弗沙用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的治疗。
艾弗沙属于第三代EGFR-TKI药物,具有“双活性、高选择、强缩瘤、安全佳”的特点。此次申请是基于艾弗沙治疗T790M突变阳性的局部晚期或转移性NSCLC患者的关键注册临床研究。该研究结果已于2020年在美国临床肿瘤学会(ASCO)年会上发布。结果显示:艾弗沙治疗EGFR T790M突变阳性局部晚期或晚期NSCLC的客观缓解率(ORR)为74.1%,疾病控制率(DCR)为93.6%【2】。艾弗沙安全性好,治疗相关腹泻和皮疹发生率低,分别为5%和7%,且均为1-2级,体现出艾弗沙对EGFR野生型具有较高的选择性【2】。
在第21届世界肺癌大会(WCLC 2020)上,艾力斯公司公布了艾弗沙治疗中枢神经系统(CNS)转移NSCLC的分析结果【3】。该分析结果来自艾弗沙治疗EGFR T790M突变阳性局部晚期或转移性NSCLC的I-II期剂量扩展研究。研究显示,80mg 艾弗沙剂量组治疗CNS转移NSCLC患者的CNS ORR为60.0%,160mg剂量组 艾弗沙剂量组治疗 CNS转移NSCLC患者的CNS ORR为84.6%,DCR为100%【3】,为艾弗沙用于CNS转移NSCLC患者的治疗提供了有力支持。
肺癌是致死率极高的恶性肿瘤。根据世界卫生组织国际癌症研究机构(IARC)发布的最新数据显示,我国2020年肺癌发病人数约81.6万,死亡人数约71.5万,均占世界首位【2】。在肺癌患者中,NSCLC人群占85%;亚洲肺癌人群EGFR突变约占50%【4】。相信艾弗沙一定能让中国肺癌患者从比肩国际水准的中国原研第三代EGFR-TKI治疗中获益,也一定能为提高我国肺癌患者的整体生存率做出贡献。
二、优替德隆(Utidelone,UTD1)
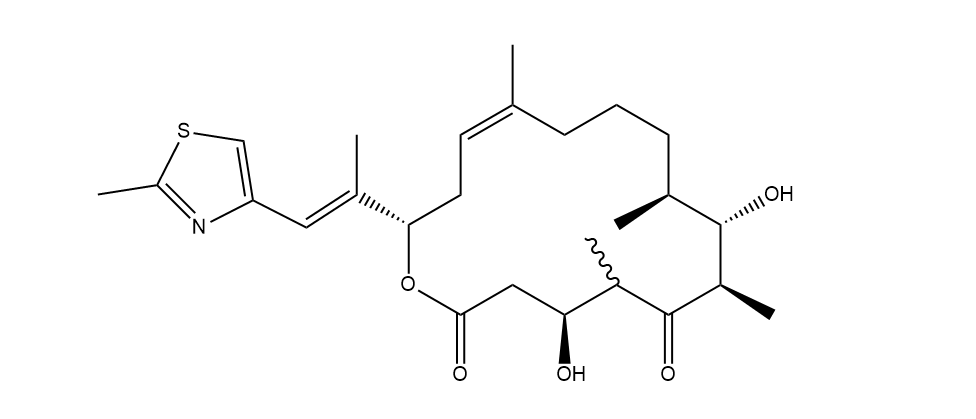
2021年3月15日,成都华昊中天药业有限公司的1类新药优替德隆注射液(商品名:优替帝)正式获国家药监管理局批准。该药是拥有自主知识产权专利的药物。优替德隆(Utidelone,UTD1)是通过基因工程改造的埃博霉素类似物,通过促进微管蛋白的聚合,诱导细胞凋亡。此次优替德隆的获批是基于一项前瞻性、多中心的3期临床研究结果。该研究结果分别两次入选ASCO(美国临床肿瘤学年会)大会口头汇报,研究结果也发表于国际知名肿瘤学期刊Lancet Oncology和Annals of Oncology。
研究数据显示,对既往使用过蒽环类和紫杉类药物的晚期乳腺癌患者,优替德隆联合卡培他滨与卡培他滨单药相比,总生存期由15.7个月显著延长至20.9个月,死亡风险降低31%;无进展生存期由4.11个月显著延长至8.57个月,疾病进展风险降低54%;缓解率由26.7%提高至49.8%【5】。在安全性方面,化疗药物常见的不良反应,包括血液学毒性、胃肠道毒性和肝肾功能损伤均较低,唯一比较常见的不良反应为抗微管类药物常见的外周神经病变,但可逆、可控、恢复快,这些优势大大降低了患者的治疗风险和处理相关不良反应导致的额外花费;也提升了患者整体治疗的耐受性,为长期生存获益提供了保障。这意味着,与现有治疗方法相比,优替德隆具有显著的临床效益和安全性优势【5】。
三、普拉替尼(pralsetinib)
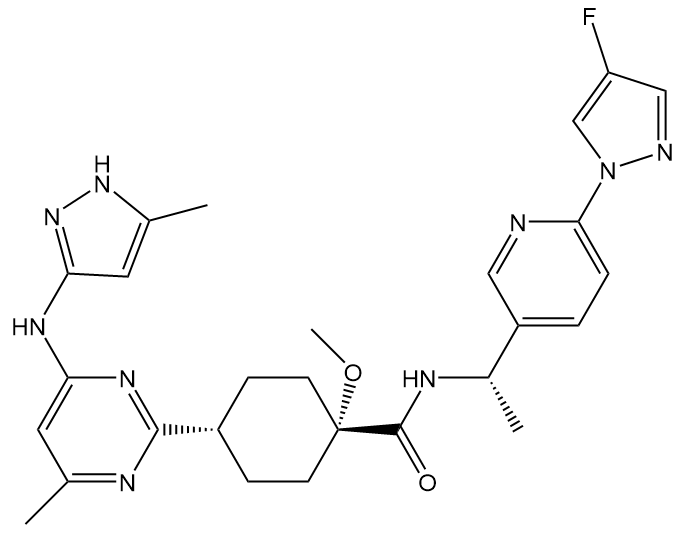
2021年3月24日,基石药业1类新药普拉替尼胶囊(商品名:普吉华)正式获国家药品监督管理局批准上市。该药本次申请的适应症为既往接受过含铂化疗的RET(rearranged during transfection,转染时发生重排)基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)。由此,普拉替尼成为国内首款上市的RET融合抑制剂。
值得一提的是,普拉替尼是由基石药业战略合作伙伴BlueprintMedicines Corporation开发的一款口服、强效和高选择性靶向致癌性RET变异(包括可预见的耐药突变)的药物。2018年6月,基石药业通过与Blueprint签订独家合作及授权许可协议,获得普拉替尼单药或联合治疗在大中华地区(包括中国大陆、香港、澳门和台湾地区)的临床开发与商业化权利。早在2020年9月,Blueprint的普拉替尼就获得FDA批准。
此次普拉替尼国内的获批是基于2020年WCLC大会上公布全球性I/II期的ARROW研究中国内患者的数据结果。截至2020年5月22日,共纳入10个中国研究中心的37例晚期RET融合阳性非小细胞肺癌患者。结果显示:32例基线有可评估病灶的患者中,确认的客观缓解率(ORR) 为56%,包括1例完全缓解和17例部分缓解(PR),除此之外,还有2例部分缓解待确认。疾病控制率为97%,其中1例不可评估,该研究结果与全球结果一致,且该药在中国患者人群中的安全性及耐受性良好【6】。
目前具有RET活性的MKIs(如卡博替尼和凡德他尼)的特征是对多个激酶靶点的活性,最显著的是受体酪氨酸激酶VEGFR2,它调节血管生成和血管内皮的通透性。药物抑制VEGFR2活性可导致临床相关的剂量限制毒性,如高血压、血栓形成和出血,药物对RET的选择性差。相比之下,普拉替尼在RET上的作用比在RET驱动的恶性肿瘤中研究的MKIS更强,并且在人类激酶中具有高度的选择性【7】。
总结:
近年来,随着我国卫生健康医疗水平的提高,仿制药已经无法满足社会需求,创新药成为今后发展的一个重点方向,我国医药产业发展正处在从仿制药向创新药的转型期。以上三种创新药的上市很大程度上解决了社会上仍未被满足的临床需求,给中国的患者带来了福音。虽然我国创新药近年来发展较快,但与发达国家还有较大的差距,并且创新药研发周期长、投入大,具有很高的不确定性,为此需要良好的创新生态,需要创新药企业加大研发投入,参与国际竞争,需要发挥有效市场和有为政府的作用【8】。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论