近年来,抗体偶联药物(ADC)在肿瘤领域异军突起。2019年与2020年,开启了ADC批准的爆发期,FDA先后批准了5个 ADC药物(Polivy、Padcev、Enhertu、Blenrep和Trodelvy)。最近获批的ADC是Akalux,该药物于2020年9月在日本附条件批准上市,用于头颈癌的治疗。可见,ADC领域愈发火热,竞争也愈发激烈。
已上市的ADC抗体
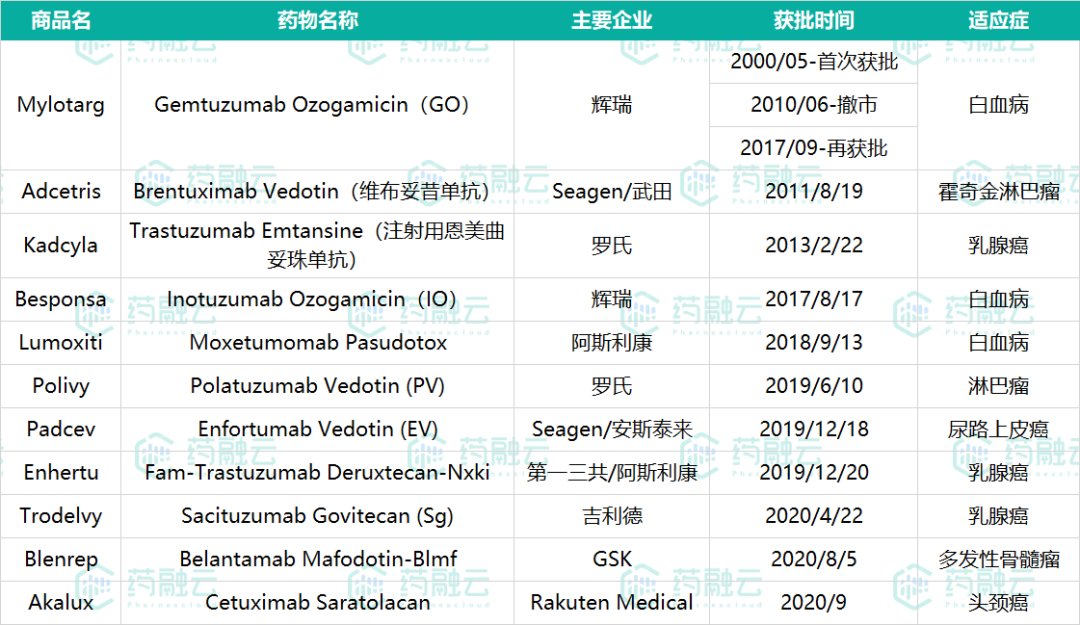
目前,全球共有11个ADC药物获批,分别是武田/Seagen的Adcetris、罗氏Kadcyla、辉瑞/惠氏的Besponsa、辉瑞/惠氏Mylotarg、阿斯利康的Lumoxiti、罗氏的Polivy、第一三共/阿斯利康的Enhertu、Immunomedics的Trodelvy、GSK的Blenrep和Rakuten Medical的Akalux。
其中,进入中国市场的ADC药物有2个,罗氏的Kadcyla(注射用恩美曲妥珠单抗)和Seagen/武田的Adcetris(维布妥昔单抗),分别于2020年1月、2020年5月获得NMPA批准上市。
药融云数据(www.pharnexcloud.com)显示,国内在开发ADC药物的企业有:荣昌生物、恒瑞医药、百奥泰、百力司康、博安生物、云顶新耀、豪森药业、百济神州、新码生物、多禧生物、科伦药业、基石药业、德琪医药、宜联生物、康威生物、诗健生物、应世生物、齐鲁制药、美雅珂/乐普生物、天广实、普方生物(ProfoundBio)、尚健生物、丽珠生物、和元艾迪斯、保合安特生物、启德医药、无锡智康弘义生物、诺灵生物、石药集团、东曜药业、上海医药、复旦张江、嘉和生物、新理念、礼新医药、联宁(苏州)生物、复宏汉霖、特瑞思、百利药业、海正药业、三生制药等等。
偶联药物中,抗体偶联药物(ADC)是近年来的研究热门,国内已然呈现扎堆研发的现象,而对其他的偶联药物药物技术,如多肽偶联药物(PDC)却鲜有公司投入研发。或许投身多肽偶联药物(PDC)的研发,对企业来说能够实现弯道超车的机会。
PDC的技术特色
PDC(Peptide Drug Conjugate)是一种新型的偶联药物,其结构主要包含3个元素——细胞毒素,Linker以及靶向多肽,通过一个可分解的Linker将特定的多肽序列与细胞毒素共价结合。它将细胞毒素以提高局部浓度的形式靶向递送至患病组织,减轻非疾病组织中的毒性效应,从而减轻不良反应,达到增效减毒的科学目的。
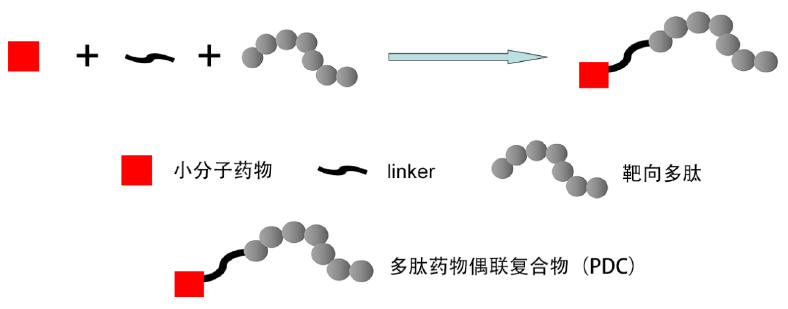
PDC整合了多肽的优势,与抗体偶联药物(Antibody Drug Conjugate,ADC)相比,其分子量更小,不易引起自身免疫反应;与抗体生产的复杂工艺过程相比,PDC更易合成与纯化,有效降低大规模生产的成本。
全球上市的PDC药物

从全球市场来看:目前仅有两个PDC药物获批上市,行业关注度低、整体处于早期开发状态,国内在这个领域尚是一片处女地。Lutathera由诺华子公司Advanced Accelerator Applications S.A开发上市,是第一款肽受体放射性核素治疗(PRRT)药物。Melflufen是一种首创的、靶向氨肽酶的抗癌肽偶联药(PDC),可将烷化剂与靶向氨肽酶的多肽偶联在一起。氨肽酶存在于所有人类细胞中,在多种肿瘤中过度表达,包括多发性骨髓瘤。Melflufen的加速获批是得益于一项关键II期HORIZON的临床结果。试验纳入157例患者与地塞米松联用,治疗复发/难治性多发性骨髓瘤(MM),总缓解率达到23.7%,中位缓解持续时间为4.2个月。
PDC在研产品
目前PDC的在研产品以国外公司为主,研发进展较快且活跃的公司有Oncopeptipes、Bicycle Therapeutics、Cybrexa Therapeutics等。国内布局该领域的企业有盛诺基医药、同宜医药、泰尔康生物等。其中盛诺基医药与加拿大公司Angiochem合作开发的SNG1005,正在中国开展III期临床试验。是国内进展最快的PDC项目。
Bicycle Therapeutics公司有三款PDC在研产品,分别是BT1718、BT5528 和BT8009,均处在临床I/II期开发阶段。
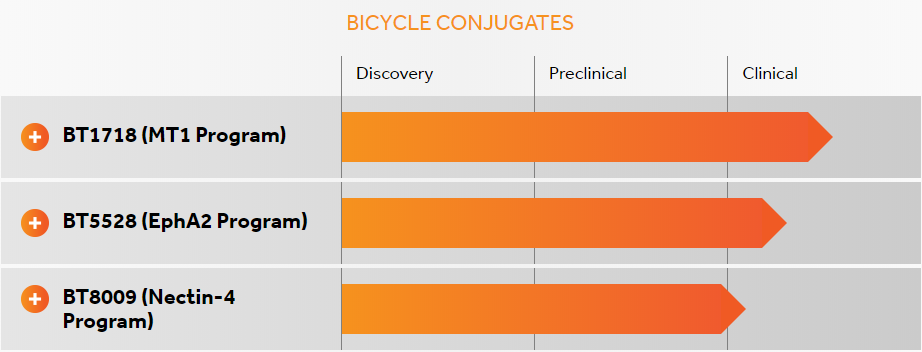
(数据来源:公司官网,下同)
同宜医药凭借核心技术平台BESTTM,开发出一系列抗肿瘤偶联药物(XDC)。其中以PDC药物CBP-1008进展最快,目前正在进行I期临床试验。
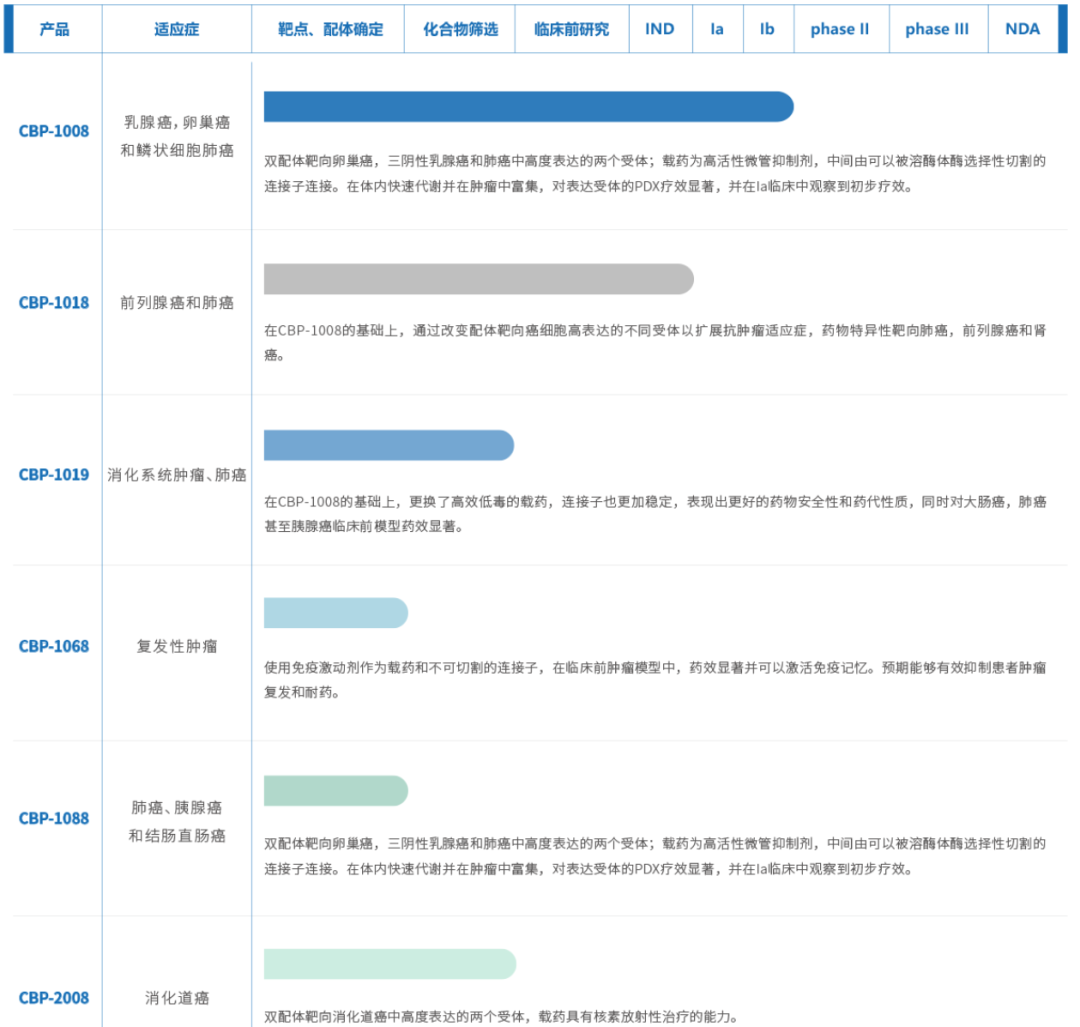
其余国内在研的PDC药物基本处于临床前研发阶段,整体研发热度与ADC药物相差甚远,没有受到太多关注。
结语
从全球PDC药物市场来看,该领域整体热度不高,跟ADC抗体药物初期研发阶段情况相似。2000年辉瑞推出第一个ADC药物Mylotarg后市场不温不火,11年后才上市第二个ADC药物Adcetris,最近两三年ADC药物才迎来了爆发期,PDC或许目前就处于当初ADC启程的那个时间点。中国正在经历生物类似药、PD-1/L1、ADC药物疯狂扎堆的时代,PDC药物或许是中国偶联药物开发企业另辟蹊径所在。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论