
IL-4R是哮喘和特应性皮炎的重磅潜力靶点,IL-4R抗体药物为患者带来了有效的治疗药物和新的希望。特别是再生元和赛诺菲的度普利尤单抗,自2017年上市以来,由于其在全球的畅销,以一己之力带动了整个IL-4R抗体药物市场不断扩充,2017年仅2亿美元,2020年就大幅增至40亿美元,年复合增长率高达153.9%。而在2021年,度普利尤单抗全球范围内售卖了$60亿美元,同比增长64%。
随着IL-4R抗体药物市场的不断扩大,越来越多的药企发现了其巨大的潜力,IL-4R也在全球范围内越来越受到药物研发者的青睐。就在今年8月初,国内IL-4R抗体药物研发领域传来了新的喜讯:据药融云《医药行业观察周报》整理,康诺亚生物的CM310注射液临床试验获批,默示许可适应症为过敏性鼻炎。CM310是康诺亚生物创新药产品研发中进度最快的,由于也是其核心候选产品,因此被大众广为关注。


截图来源:药融云《医药行业观察周报》
经药融云数据库查询,CM310重组人源化单克隆抗体注射液是由康诺亚生物自主研发,以人IL-4受体α亚基(IL-4Rα)为靶点的创新型人源化单克隆抗体。CM310可选择性地与IL-4Rα相结合,阻断IL-4Rα与IL-4以及IL-13的结合从而抑制其生物学活性。康诺亚的CM310是国内首家获批临床的IL-4R抗体药物,拟开展特应性皮炎、慢性鼻窦炎、哮喘临床研究。截至目前,CM310注射液针对慢性鼻窦炎和中重度特应性皮炎的适应症研发进展最快,均推进至临床3期试验阶段。
CM310注射液临床试验情况
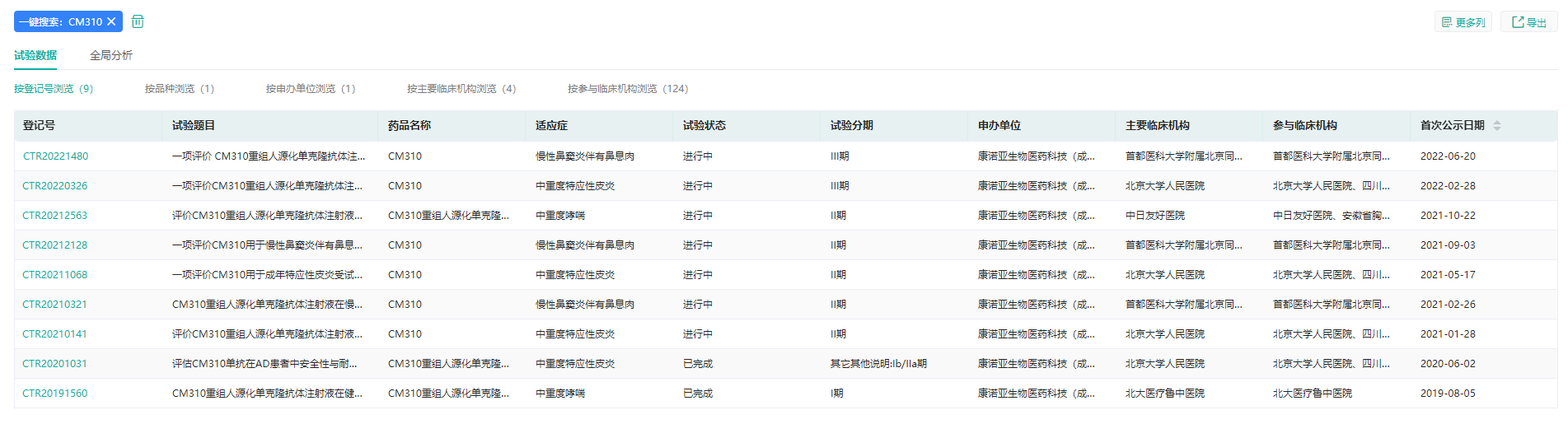
截图来源:药融云中国临床试验数据库
据悉,CM310注射液在今年还获得了国家特殊审批。2022年6月14日,康诺亚-B(02162)公布,国家药品监督管理局药品审评中心(CDE)授予公司自主研发的1类新药CM310重组人源化单克隆抗体注射液突破性治疗药物认定,用于治疗中重度特应性皮炎。
CM310重组人源化单克隆抗体注射液审批情况
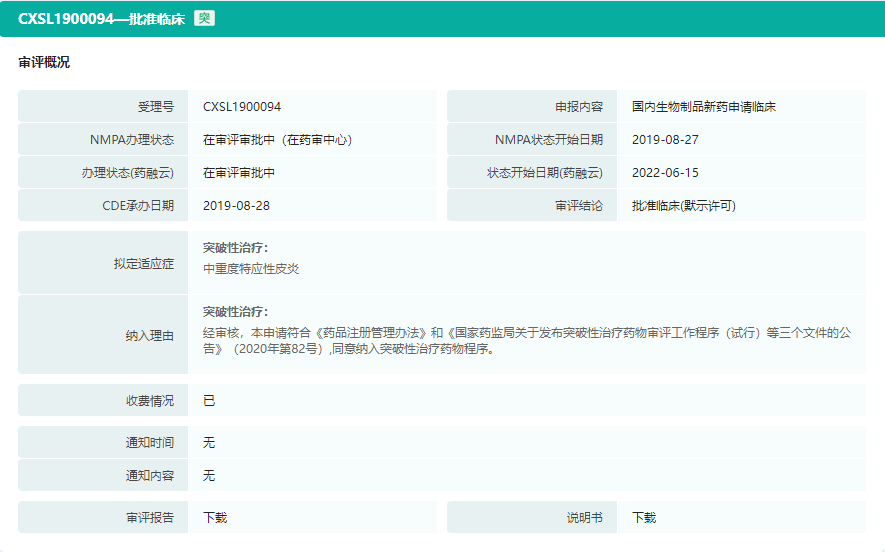
截图来源:药融云中国药品审评数据库
一、IL-4R抗体药物市场
据药融云数据库显示,截至目前,全球范围内已获批上市的IL-4R抗体药物共有4款,分别是甲磺司特、度普利尤单抗、吡美莫司以及Actimmune。临床阶段进展最快的就数康诺亚生物的CM310注射液,全球仅此一家处于临床3期试验阶段,最有望成为全球第5款IL-4R抗体药物。其他还有11款处于临床2期。另外据统计,在IL-4R抗体所有研发的药物里,20%都是针对于呼吸系统疾病领域,其中,哮喘和特应性皮炎适应症布局的较多,分别有16和14款。
已获批上市的IL-4R抗体药物

IL-4R抗体药物适应症研发TOP10
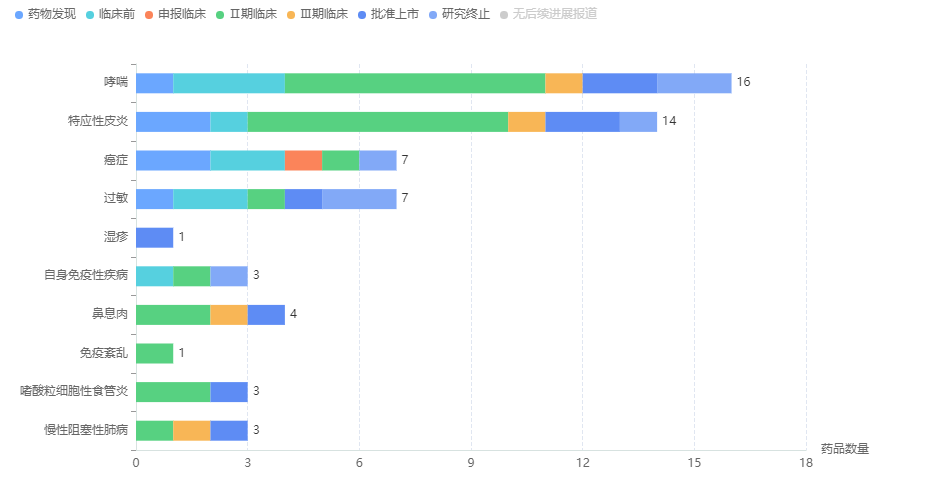
截图来源:药融云全球药物研发数据库
据药融云统计,IL-4R抗体药物在我国院内前几年的销售总体呈现缓慢递增趋势,2018年首次突破亿元大关,2021年突然出现翻红,销售额达3.67亿元,同比增长271.27%,这主要是由于再生元/赛诺菲度普利尤单抗的加持,该药2021全年销售达2.62亿元,占据IL-4R抗体药物的七成市场。IL-4R抗体药物现2022年Q1的销售额已有近2亿元,预计今年还将持续走红,又是一个丰收年。
IL-4R抗体药物院内销售情况
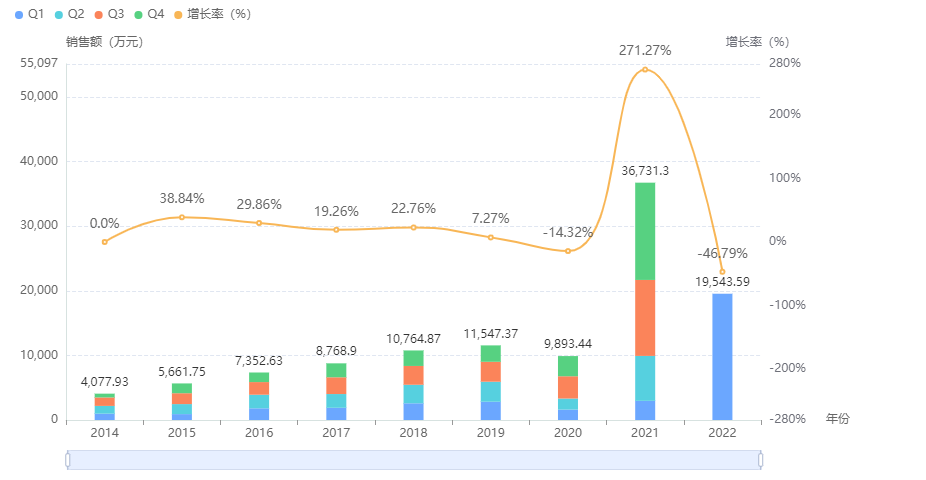
截图来源:药融云全国医院销售数据库
度普利尤单抗不仅在中国市场表现突出,在全球来看都是IL-4R抗体的重磅热门药物。该药是由再生元和赛诺菲开发的一款全人单克隆抗体,2017年3月28日, 度普利尤单抗获美国 FDA 批准首次上市,成为首个治疗中重度特应性皮炎的生物制剂,后又在多国陆续获批上市,2020年6月才获批进入中国市场。
度普利尤单抗各国上市时间轴(部分)
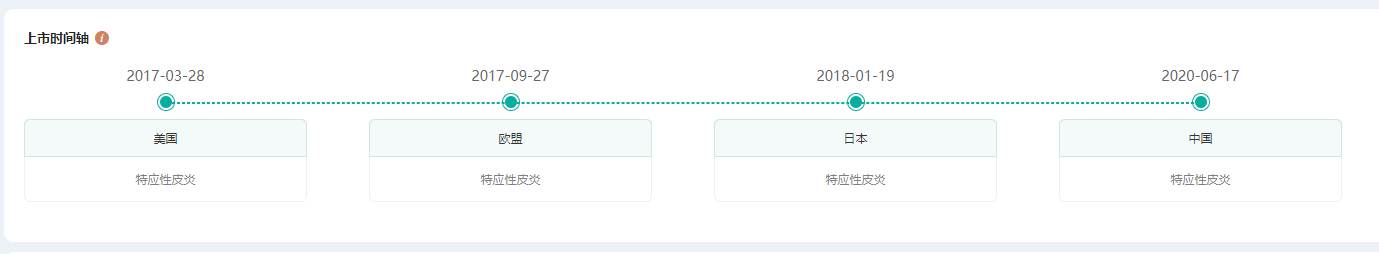
截图来源:药融云全球药物研发数据库
2020年12月底,经国家医保谈判,度普利尤单抗被正式列入《国家基本医疗保险、工伤保险和生育保险药品目录(2020年)》,是新版医保目录中唯一一个治疗中重度特应性皮炎的靶向生物制剂,用于对传统治疗无效、有禁忌或不耐受的中重度特应性皮炎。度普利尤单抗上市仅5个月即被纳入国家医保目录,这个风向标值得国内药企关注;公司将大幅降价。
度普利尤单抗注射液中国批文信息
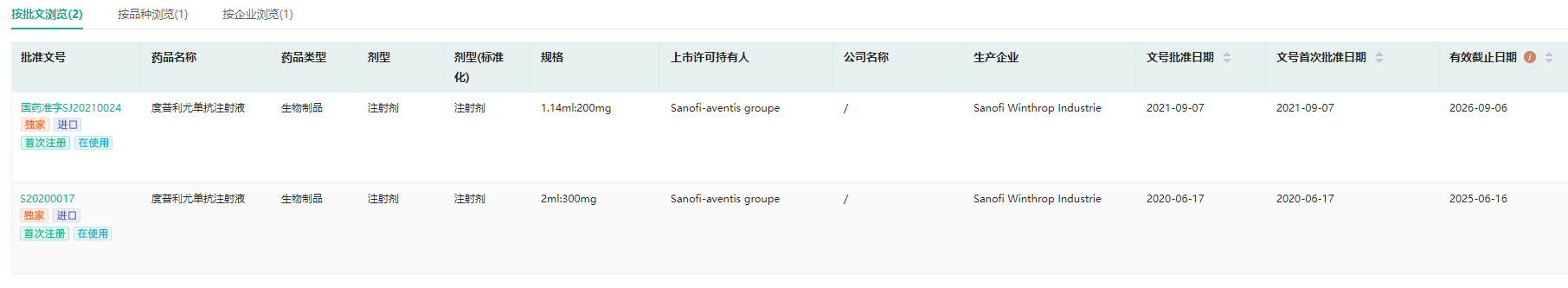
截图来源:药融云中国药品批文数据库
据药融云统计,再生元/赛诺菲的度普利尤单抗自上市后一直备受追捧,2018年销售额首次突破亿元美元大关,2019年首次突破十亿美元大关,2020年同比增长67.67%,2021年全球销售额直达64亿美元。由此可见,随着时间推移,度普利尤单抗市场持续扩张,一步一步成长为IL-4R抗体里的重磅炸弹药物,未来潜力无限。
度普利尤单抗注射液全球销售情况
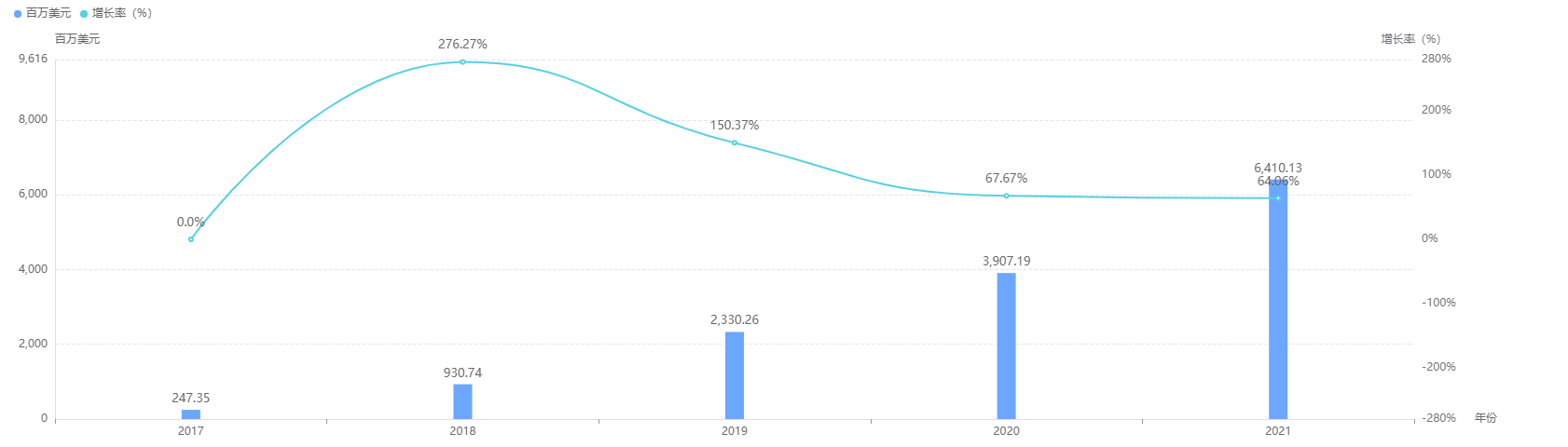
截图来源:药融云全球药物研发数据库
二、IL-4R抗体药物国内研发进展
由于IL-4R抗体药物市场潜力巨大,国内数家企业纷纷争先布局IL-4R,康诺亚生物进度位列第一梯队。在国内原研中,其适应症拓展速度和广度上均处于领跑地位。2021年11月29日,CM310治疗特应性皮炎适应症的临床Ⅱb期获得积极数据结果,基于IIb期临床数据,康诺亚将迅速推进III期临床试验,并预计2023年将向NMPA递交NDA申请。
其他IL-4R抗体药物国内在研企业还有苏州康乃德生物的CBP-201、江苏荃信生物的QX-005-N、宝船生物医药的MG-K10、中山康方生物的AK-120、沈阳三生制药的611。
IL-4R抗体药物国内研发现状(部分)
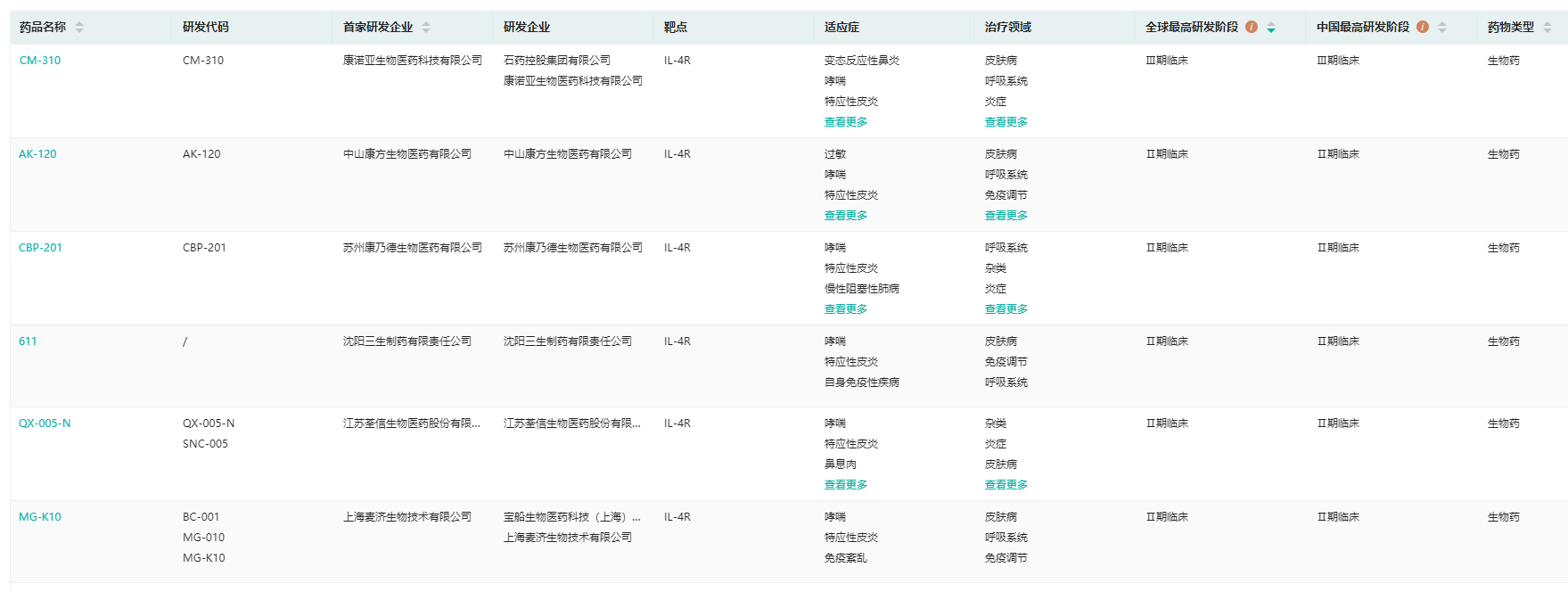
截图来源:药融云全球药物研发数据库
三、IL-4R潜力巨大,挑战与机遇并存
就全球靶点药物研发市场来看,药企在IL-4R靶点的投入相对较少,竞争格局良好,赛道相对宽敞,其市场也随着时间在不断扩张,不失为一个有着巨大潜力的靶点,挑战与机遇并存。据药融云统计,目前全球在研的IL-4R抗体药物大概有60+款,仅4款获批上市,大部分药物都处在前期阶段(药物发现、临床前),IL-4R就像一颗雨后春笋,已冒出点尖尖,处在一个待爆发状态,期待未来厚积薄发,在靶向药物以及涉及疾病领域里发光发热。
IL-4R抗体药物全球研发情况
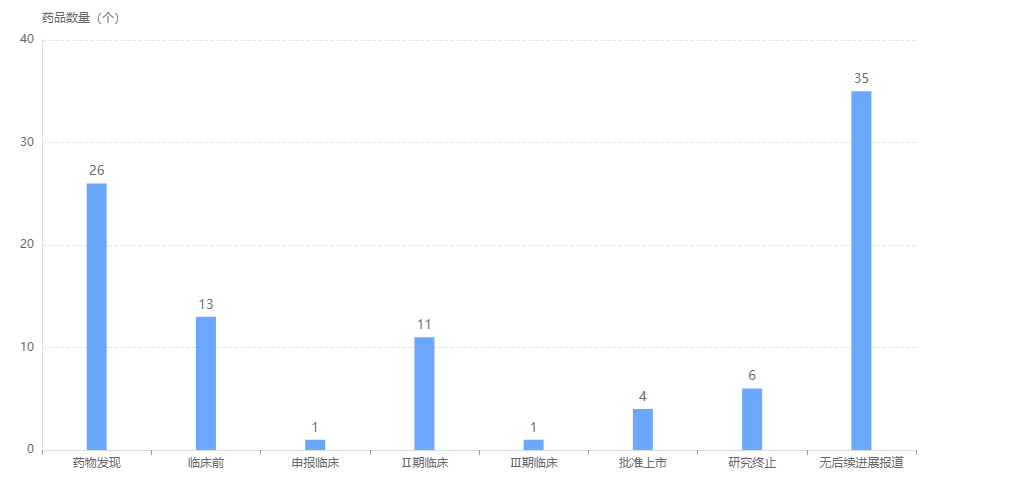
截图来源:药融云全球药物研发数据库
想要解锁更多药物靶点研发信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药物靶点的创新药布局、基本信息、研发阶段、最新进展、竞争格局、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论