
今年以来,创新药行情可谓是热闹得很,BD盛宴未休,浪是一潮高过一潮,行业面曾一度疯涨个不停。纵使BD能点燃行情,但真正支撑行情走得远的,永远是创新本身的含金量。
话说回来了,越是这种时候,大家越想押注确定性较高,且极具想象力的标的公司。毕竟突然这里爆个雷,哪里爆个雷,让投资者总是很恼火。而往往评估创新药企的几大维度,无非是研发立项能力、临床推进能力、BD能力、商业化能力这几大关键。
抛开股价短期浮沉,E药资本界以此标准在筛选诸多标的之际,注意到了康诺亚,这家成立不到十年的药企,目前拥有一款已上市产品普奇拜单抗,直接对标明星自免药王——赛诺菲度普利尤单抗(达必妥),是个名副其实的潜在大药,已获批三个适应证,市场地位均较为靠前,要么是国产首个,要么是全球首个。更关键的是,在不久后的医保谈判,它也在磨拳搽掌,这将成为其未来能否加冕国产自免新王的关键一役。
在研究了这一标的过后,我们觉得难能可贵的是,它总是立项先人一步,而且还做出来了:自免火时,发现它已布局IL-4Rα、TSLP、TLSP×IL-13双抗,且进度国内数一数二;双抗热时,它已是国内CD3双抗布局最全之一;ADC浪潮中,其CLDN18.2ADC(CMG901)已是全球最快进入III期的该靶点ADC,极可能成为首个全球上市产品,还与阿斯利康达成12亿美元BD合作……
与之有些反差的是,目前创新药狂欢下,康诺亚股价从年初20多元/股,涨至而今60多元/股,涨了145%。但相较可比自免标的,估值还不算太高,拉长上市时间战线来看,也还没回到2023年的股价最高点,市值现在200亿左右徘徊。为了更好地研究这家代表着自研实力的一批药企标的,CM10医药研究中心将从行业稀缺值、财务健康度、业务健康度以及综合建议等多个方面,来一一复盘。
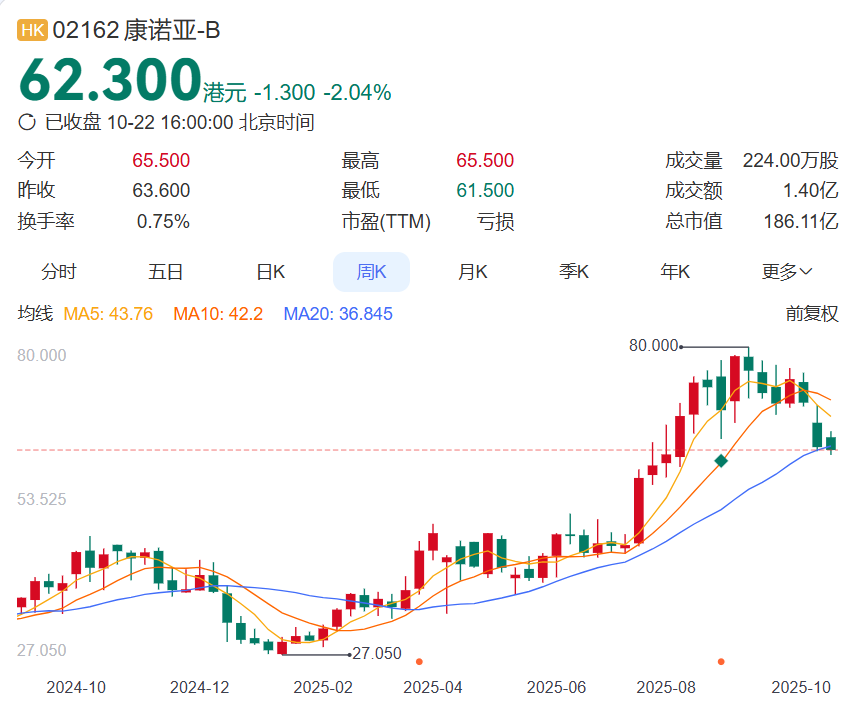
▲康诺亚2025年以来股价表现,数据来源:百度股市通
👀 最先吃到肥肉的国产自免新王
千亿级自免赛道,强手林立,向来拥挤。旧王暮,新王立,已不是什么新鲜事。
而今的“自免新一代药王”已被跨国药企赛诺菲度普利尤单抗徐徐夺下。说起这款药物,产业界并不陌生,作为全球首个获批的靶向IL-4Rα的全人源单克隆抗体,2017年首次获批上市,2024年一举登上自免药王宝座,销售额超140亿美元,让老药王修美乐都望其项背。
无人不想分得这杯美羹。
而在一众强敌环伺的国内外药企中,最先跑出来的是一家国产药企——康诺亚,核心产品司普奇拜单抗(代号:CM310)于2024年上市,这是全球第二、首个国内自主研发并获批上市的IL-4Rα抗体药物。
或是有了度普利尤单抗的铺垫,司普奇拜单抗半年斩获了三个适应证,且都是数以百亿计的大市场,市场对康诺亚这款药物寄予厚望。
- 国内第一、全球第二:2024年9月获批用于成人中重度特应性皮炎,填补了国产特应性皮炎生物制剂的空白,成为全球第二款上市的IL-4Rα药物;
- 国内首个:2024年12月获批慢性鼻窦炎伴鼻息肉适应证,系国内首款针对该病症的生物制剂;
- 全球首个:2025年1月获批季节性过敏性鼻炎适应证,成为全球首个针对该病症的IL-4Rα生物制剂。
这个产品完全遵循大单品的发展逻辑。除了已获批适应证外,其余适应证管线亦在持续拓展,比如治疗青少年中重度特应性皮炎、结节性痒疹、哮喘等,都是相当可观的大市场。
大赛道向来不乏竞争者,康诺亚的先发优势能维持多久?又该如何突围率先耕耘的赛诺菲?成为摆在其当下的两大关键问题。
先对标“自免药王”度普利尤单抗,司普奇拜单抗实现了“局部赶超”。可以看到,司普奇拜单抗首个获批适应证瞄准成人中重度特应性皮炎,与度普利尤单抗刚上市时一致。此外,司普奇拜单抗还涉及了前者未及的鼻科临床空白领域。
- 季节性过敏性鼻炎适应证中,度普利尤单抗临床研究失败,而司普奇拜单抗成为全球首个获批药物;
- 慢性鼻窦炎伴鼻息肉领域,司普奇拜单抗已在国内上市,成功拿下一个“国内首款”,度普利尤单抗仍处于三期临床阶段。
再从市场竞争格局来看。
纵观一众在研管线,IL-4Rα靶点竞争比较激烈,国内多家企业布局IL-4R单抗。但好在,康诺亚先发优势比较明显,不仅是最早申报临床的,也是最早申报上市并进入商业化的IL-4Rα。
这与康诺亚的布局时点息息相关。公开资料显示,2019年5月,司普奇拜单抗首次提交临床申请,成为国产首个进入临床的IL-4Rα单抗,彼时度普利尤单抗全球销售额尚不足10亿美元。凭借早期立项优势,康诺亚最终实现“国产首上市”,抢占先发赛道。
那么,有多长时间的先发优势呢?
查询一众布局者公开进度,IL-4Rα赛道中,其他企业最快需2025年底才能提交上市申请(NDA),获批或延至2026年底甚至2027年。在慢性鼻窦炎伴鼻息肉领域,目前国内仅司普奇拜单抗一款生物制剂获批,而赛诺菲、智翔金泰等企业的同类药物仍在三期临床阶段。
这意味着,康诺亚差不多手握2-3年市场窗口期。无论横看竖看,只要商业化没砸,康诺亚业绩表现应该较为可观。
👀 左手自免右手肿瘤,拿稳了吗?
康诺亚,代表了自研实力突出的一批创新药企。
它成立于2016年,自诞生起就带着光环。康诺亚的两位创始人陈博和王常玉曾分别领导研发了首个国产PD-1特瑞普利单抗、全球首款PD-1纳武利尤单抗(O药),业内知名度可见一斑。
康诺亚自2021年港股上市,一度迎来市值高峰,在融资阶段便获联想控股、高瓴资本、礼来亚洲等巨头加持,这既得益于明星创始人的行业影响力,也源于其管线的高潜力,在研项目早早通过授权变现。
从财务层面来看,尚处投入期,首款产品于2024年下半年才实现商业化,营收未覆盖历史亏损,整体财务结构与多数Biotech相似。
不过,康诺亚创收能力正快速提升,这可从上半年业绩可见一斑。2025年上半年总收入创了历史新高,约5亿元,同比增长超800%。其中核心产品司普奇拜单抗销售净额约1.7亿元;另上半年对外合作收入约3.3亿人民币,主要来源于CM313、CM355及CM336项目对外授权收入。
一切还是得回到基本面来看。
在研究了这一标的过后,E药资本界觉得难能可贵的是,康诺亚作为成立不到十年的创新药企,凭借强大的研发团队和高效的立项策略,一手自免,一手肿瘤,在两大领域均争得一席之地,其价值远不止于一款司普奇拜单抗。
康诺亚的实力不仅体现在现有上市产品上,更在于其管线的强劲延续性。作为国内管线BD覆盖量最高的Biotech之一,同时也是2024年“NewCo”模式热潮中最为活跃的参与者,其在多个领域的布局均展现出前瞻性与竞争力。
在自免领域,康诺亚并非孤军奋战,目前已布局5款产品(1款上市,4款在研),核心管线进展显著,几款稍作举例。
- CM326(TSLP靶点):作为业内关注的热门靶点,TSLP领域此前因恒瑞医药SHR-1905经AiolosBio被GSK收购而备受瞩目,而康诺亚的CM326进度更为领先。该药物于2024年5月启动针对慢性鼻窦炎伴鼻息肉(CRSWNP)的II期临床,目前正推进患者入组,临床进度稳居国产第一梯队。
- CM512(TSLP×IL-13双抗):作为公司下一代自免双抗的核心研发管线,其全球开发进度仅次于赛诺菲的lunsekimig,凭借长半衰期可支持每3-6个月一次的长效给药,有望成为司普奇拜单抗之后的下一代重磅产品。这款产品从管理层公开表态,可以看出对其寄予厚望。研发重点聚焦自免与呼吸科适应证,目前中国1b期特应性皮炎(AD)试验正在推进。海外权益通过NewCo模式授予Belenos,后者已于2025年3月完成海外首例哮喘患者入组,推进海外1期临床。
- CM313 作为国产首款获批临床的CD38单抗,其针对免疫性血小板减少症(ITP)的I期数据已显示出良好的疗效与安全性。
再看肿瘤领域,8款管线布局。
- CMG901:这款靶向Claudin18.2的抗体偶联药物(ADC)是潜在的“全球首创”,已获中国CDE突破性治疗认定、美国FDA快速通道及孤儿药资格,并与阿斯利康达成约12亿美元的全球独家授权协议。
- 目前全球尚无CLDN18.2靶向ADC上市,CMG901的临床进度全球领先:国内已进入III期,与信达生物IBI343、恒瑞SHR-A1904等共同处于第一梯队;海外进度同样领先,远超德琪医药(II期)及恒瑞、科伦博泰等(I/II期),全球先发优势显著。
- 其余肿瘤管线中,康诺亚亦是国内CD3双抗布局最全面的创新药企之一。
康诺亚的自研实力,几乎已经得到验证,不用多说,肿瘤立项一般都是全球前三,自免也至少国内第一。最佳体现是,自主研发的核心产品司普奇拜单抗成人中重度特应性皮炎、慢性鼻窦炎伴鼻息肉、季节性过敏性鼻炎三项适应证已获批上市,其中两项获CDE突破性治疗药物认定,纳入CDE优先审评审批程序。另一款潜在世界首创靶向Claudin18.2的抗体偶联药物CMG901获CDE突破性治疗药物认定、FDA快速通道及孤儿药资格认定,已与阿斯利康达成约12亿美元全球独家授权协议。
结果显而易见。自免领域拿下国内首个IL-4Rα、首个TSLP、首个TSLP×IL-13双抗;ADC领域通过绑定阿斯利康,使CMG901成为首个进入全球III期的CLDN18.2 ADC,且有望成为全球首个获批上市的同靶点药物;在TCE热潮中,其也被证实是国内CD3双抗布局最全面的Biotech之一。这足以证明康诺亚并非盲目跟风,而是具备扎实的创新实力。
👀 决定价值的终极试金石
尽管研发与BD都可圈可点,康诺亚能否真正站稳“自免新王”之位,其市值能否从当前的不足200亿港元向康方生物等港股创新药企看齐,这也是投资者关注的核心问题。
商业化能力和国际大BD是持续打开向上空间的两大。对于康诺亚而言,最迫切需要验证的是商业化,这也是多数Biotech转型期的共性挑战。
摆在康诺亚面前的关键一役,就是司普奇拜单抗2025年下半年的医保谈判与之后市场的打法。
作为国产首款IL-4R药物,司普奇拜单抗已获批3大适应证,且各有差异化特点,这对跨科室销售能力、患者教育水平及旺季快速上量能力提出极高要求。
从对标竞品数据看,达必妥(度普利尤单抗)自2021年纳入医保后,销售额呈爆发式增长,充分证明医保对自免生物制剂的放量催化作用。因此,对司普奇拜单抗而言,进入医保是打开市场的“必答题”。
根据管理层此前路演信息,商业化推进路径倒是较为清晰。
- 团队搭建:现有300余人商业化团队,计划2025年底扩至500人,核心目标是年内完成更多医院及科室医生的“用药破冰”,为明年医保落地后的放量铺路;
- 医保策略:管理层明确表示,非常渴望进入医保,3个适应证均计划参与今年谈判,优先争取特应性皮炎(AD)和慢性鼻炎明年纳入医保,过敏性鼻炎则根据降价幅度灵活决策;
- 市场进展:一季度已完成29个省份挂网,医院准入速度超预期,核心驱动力在于司普奇拜单抗的AD疗效数据优势,以及作为鼻科多年来首款创新制剂的稀缺性;
- 定价:采取“买二赠一”策略后,每针实际价格1208元(原价1812元),较度普利尤单抗低约300元,有性价比。
- 定位上,AD领域瞄准度普利尤单抗无效或医保限额超标的患者;鼻科领域通过C端患者需求倒逼处方,并针对慢性鼻炎围手术期及术后无效患者推广,精准切入细分市场。
在管理层释放的积极信号中,也暗指了增长预期。
- 特应性皮炎需求稳步增长,过敏性鼻炎旺季放量显著,全年5亿元销售指引不变,且下半年占比更高;
- 竞争格局上,司普奇拜单抗领先其他国产IL-4R药物2-3年,且比达必妥多2个鼻科适应证(度普利尤单抗慢性鼻炎适应证预计1-2年后才申报NDA),先发优势明显。管理层对该产品前景持较为乐观态度,给出了2025年司普奇拜单抗5亿元的销售收入指引,并预计长期销售峰值可达50亿元。对比来看,赛诺菲虽未直接公布度普利尤单抗中国区销售额,但据摩熵数据库测算,2023年销售额约18.2亿元,距离预期销售峰值都还有很长一段路要走。
但需注意,当前已有近10款国产IL-4R单抗处于Ⅲ期临床(如康方生物、恒瑞医药等),未来1-2年将密集上市,百亿级市场的竞争将加剧。这意味着,康诺亚这两年的当务之急是,必须凭借先发优势快速抢占份额。
从资本市场表现来看,半年百亿港元的市值增长,初步印证了,市场对其“自免新王”地位的初步认可与更高期待。
👀 硬币的两面:未尽的棋局
任何事情都有两面性。
总体来看,这是一家研发实力很不错的创新药企,比较稳健。虽然刚开始作为一家Biotech,貌似把摊子铺得很大,但是经过几年布局,现在基本上陆续开花结果,随着首款上市产品商业化,有Biopharma潜力,研发策略清晰(聚焦头部靶点)、执行高效、BD频繁验证价值,具备“中国自免之王”的潜质。
但投资的本质是权衡机遇与风险,康诺亚的发展轨迹中,既有亮点亦有一些惋惜之处。比如2024年NewCo热潮中,康诺亚虽以4笔交易将自免双抗(TSLP×IL-13)、CD38及两款TCE双抗等管线授权出去,但首付多为千万美元级别,且核心管线剥离后,2025年缺乏新的重磅BD刺激点,由此在今年这场BD主导的创新药行情中,市场关注度有所回落。
而“自免之王”的头衔最终能否加冕,其商业化能力能否接住巨大的市场预期,正成为决定其成败的终极试金石。短期来看,康诺亚的可确定性还是挺高的。
若将视野扩展至整个自免靶点竞争格局,2024年堪称国产重磅自免药的“获批大年”:除康诺亚的司普奇拜单抗外,智翔金泰的赛立奇单抗与恒瑞医药的夫那奇珠单抗于同日获批,共同成为首款国产 IL-17A 单抗。对于这三款新药而言,2025年都是商业化能力的关键考验期。
这场自免新王的进击战,才刚刚打响。
文章来源:E药经理人
原文链接: https://mp.weixin.qq.com/s/6BGrNh3zzPxiRgWJ97tfiw
扩展阅读:






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论