
随着越来越多的抗癌新技术问世,让人类距离攻克癌症也越来越近。免疫治疗的诞生彻底改变了癌症的治疗方法,以PD-1抑制剂为代表的免疫治疗药物在黑色素瘤、非小细胞肺癌等多个癌种中大获成功,价格也一降再降,越来越亲民。
研究表明,肿瘤细胞可以通过免疫检查点受体有效避免被免疫系统识别和杀伤,因此阻断免疫检查点受体成为肿瘤免疫治疗的新思路。目前研究较为成熟的免疫检查点受体,包括程序性死亡蛋白1及其配体(PD-1/PD-L1)和细胞毒性T淋巴细胞相关抗原-4(CTLA-4),但由于其相关抗体在治疗过程中出现耐受或毒性显著增加等问题,新免疫检查点受体蛋白靶点的寻找与开发成为新的研究热点。
一、LAG-3抑制剂概况
迄今为止,除了PD-1/PDL1和CTLA-4之外,多种刺激性和抑制性辅助受体参与T细胞活化的调节,在这些辅助受体中淋巴细胞激活基因3(LAG-3)有望成为癌症治疗开发中仅次于PD-I的首要靶点。
LAG-3,又称CD223,是一类新的免疫检查点受体,于1990年被发现。LAG-3基因在人体内定位于12号染色体,含有8个外显子,跨度为6Kb,编码生成含525个氨基酸的蛋白质(包含信号肽)。LAG-3为I型跨膜蛋白,与CD4结构相似,由胞外区、跨膜区和胞内区三个部分组成。胞外部分由四个免疫球蛋白样结构域(D1-D4)组成,负责与配体结合,胞内高度保守的“KIEELE”序列与LAG-3分子的功能密切相关。LAG-3在生理条件下主要表达于活化的T细胞(CD4+T细胞和CD8+T细胞)、自然杀伤细胞(NKcell)、B细胞和树突状细胞(DC)等免疫细胞表面。
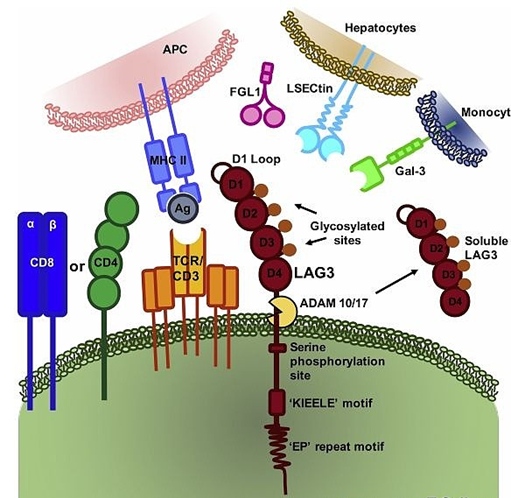
LAG-3的结构及配体
目前研究表明,LAG-3主要与四种配体相互作用,分别为半乳糖凝集素-3(Galectin-3)、主要组织相容性复合体II(MHCII)、纤维蛋白原样蛋白1(FGL1)和肝窦内皮细胞凝集素(LSECtin)。抑制LAG-3可以使T细胞重获细胞毒活性,降低调节性T细胞对效应T细胞的抑制作用,增强对肿瘤的杀伤作用。
LAG-3抑制剂可以直接结合LAG-3分子或其配体,阻断配体与LAG-3的相互作用,下调LAG-3对免疫系统的抑制效果。在以往的研究中表明,针对PD-1的抗体只能激活T细胞,而不能抑制调节性T细胞的活性,而LAG-3抗体不仅能恢复T细胞功能,还能抑制调节性T细胞活性,所以在临床开发中,LAG-3抑制剂常与PD-1/PD-L1抑制剂联合使用。
二、LAG-3抑制剂在研现状
2022年3月18日,美国FDA批准百时美施贵宝的BMS-986213(Relatlimab+Nivolumab)用于治疗不可切除或转移性黑色素瘤。与O药(Nivolumab)单药治疗相比,BMS-986213可将患者的中位无进展生存期增加一倍以上(10.1个月VS4.6个月)。基于此临床数据,LAG-3赛道日趋拥挤。
据药融云全球药物研发数据库统计,目前全球共计134个在研LAG-3抑制剂,涉及86家企业,其中进入到临床阶段的药物共计26个,占比约19%,包括I期临床7个、II期临床14个、III期临床5个。(数据截止2022年10月31日)
LAG-3抑制剂全球在研情况(部分,微信搜索"药融云小程序"进行相关更多数据查询)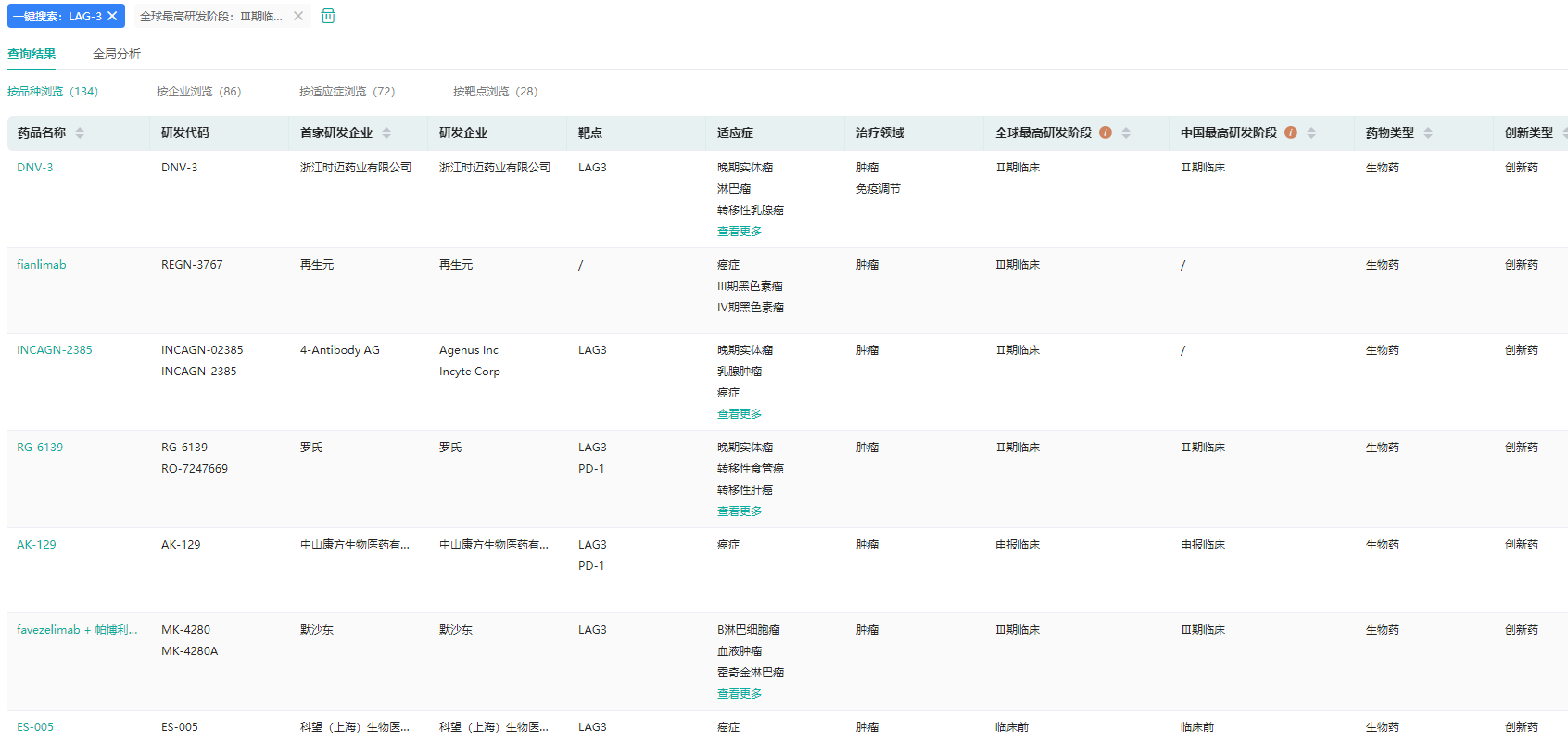
图片来源:药融云全球药物研发数据库
MK-4280A是由LAG-3抗体favezelimab(MK-4280)和PD-1抑制剂Keytruda组成的复方制剂,这两款药物均由默沙东开发。MK-4280A已在21年9月启动III期临床试验,用于治疗PD-L1阳性结直肠癌。
除了上述的一款复方制剂外,还有16款LAG-3单抗进入临床阶段,例如relatlimab(百时美施贵宝)、fianlimab(再生元)、LBL-007(信达生物)、IBI-110(百济神州)、SHR-1802(恒瑞医药)等。
第一个进入临床阶段的单抗是百时美施贵宝的relatlimab,在一项评估relatlimab与nivolumab联合用药耐受性的I-II期研究中,在既往接受抗PD-1或抗PD-L1免疫治疗后肿瘤进展的晚期黑色素瘤患者中观察到客观缓解率(ORR)为11.5%。
此外,在该队列中,肿瘤浸润淋巴细胞表达LAG-3的患者(>1%;18%ORR)的ORR是LAG-3阴性患者(<1%;5%ORR)的三倍以上,且与PD-L1状态无关。这表明肿瘤浸润淋巴细胞上的LAG-3表达可作为临床疗效的预测性生物标志物。
2021年5月,再生元首次公布了LAG-3抑制剂fianlimab联合PD-1抑制剂Libtayo(cemiplimab)治疗晚期黑色素瘤的I期临床数据。结果显示,在先前没有接受过抗PD-(L)1疗法(初治)的晚期黑色素瘤患者中,fianlimab+cemiplimab双重免疫疗法展现出了强劲疗效:ORR达到了64%。目前,fianlimab联合PD-1单抗已于2022年4月进入III期临床阶段。
fianlimab不同适应症的研发现状
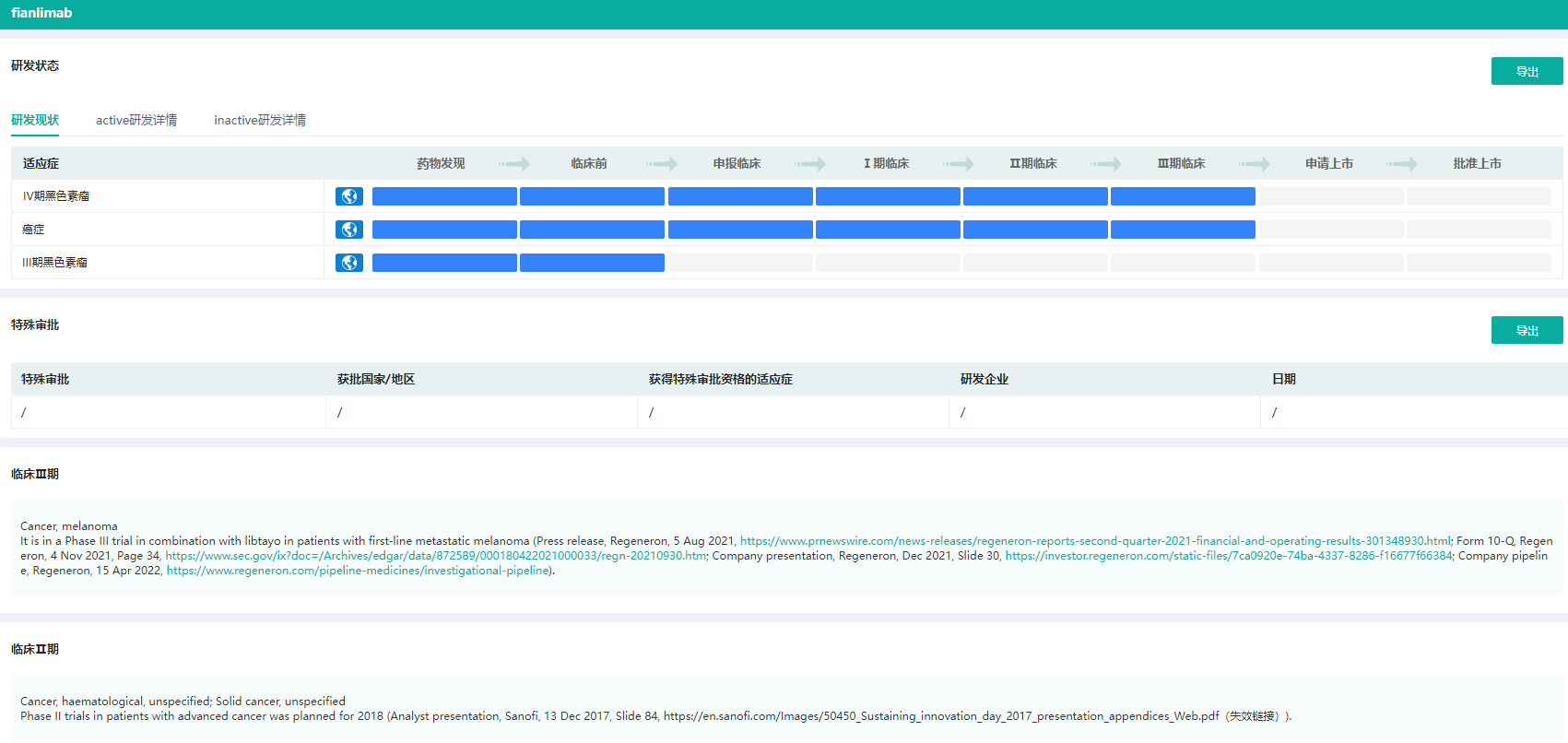
图片来源:药融云全球药物研发数据库
除此之外,诺华、辉瑞、罗氏、GSK、BI等各大制药巨头页纷纷加入战局。例如由BI开发的一种LAG-3单抗(BI-754111),联合BI-754091(抗PD-1)治疗难治性实体瘤目前已进入Ⅱ期临床试验。诺华/Immutep的LAG-525、信达生物的IBI110均已迈进Ⅱ期临床。
三、LAG-3/PD-(L)1双抗
当许多药企火热布局LAG-3和PD-(L)1联合疗法的同时,不少企业选择另辟蹊径,直接研发LAG-3/PD-(L)1双抗。目前国内布局LAG-3双抗的仅有再鼎医药、信达生物、康方生物、岸迈生物四家企业。
其中,再鼎医药是进度最快的。2018年,再鼎医药从MacroGenics公司引进了LAG-3/PD-1双抗Tebotelimab。I期临床试验数据显示,Tebotelimab与HER2单抗联用在晚期一线患者中初步总体缓解率为40%。在安全性方面,Tebotelimab安全性良好,3级不良事件的发生率为19.4%,没有4-5级严重不良反应。目前,Tebotelimab最快的一项临床研究已经进入三期,预计2023年完成。
在AACR2022年会上,康方生物也公布了LAG-3/PD-1双抗AK129的临床前结果。数据显示,AK129能够效阻断PD-1及LAG-3介导的免疫抑制,并且与PD-1和LAG-3的联合疗法相比,AK129双抗可以介导更强的免疫激活。
此外,岸迈生物的双抗EMB-02体内活性研究结果也显示,LAG-3/PD-1双抗不仅比LAG-3单抗要好,也比LAG-3+PD-1联用更好。
信达生物的IBI323则是同时靶向PD-L1、LAG-3的2+2对称型的双抗,在临床前研究中用IBI323双重阻断PDL1/LAG-3通路,能克服原发性和获得性抗PD-(L)1耐药性。
信达生物IBI323临床试验信息(部分)
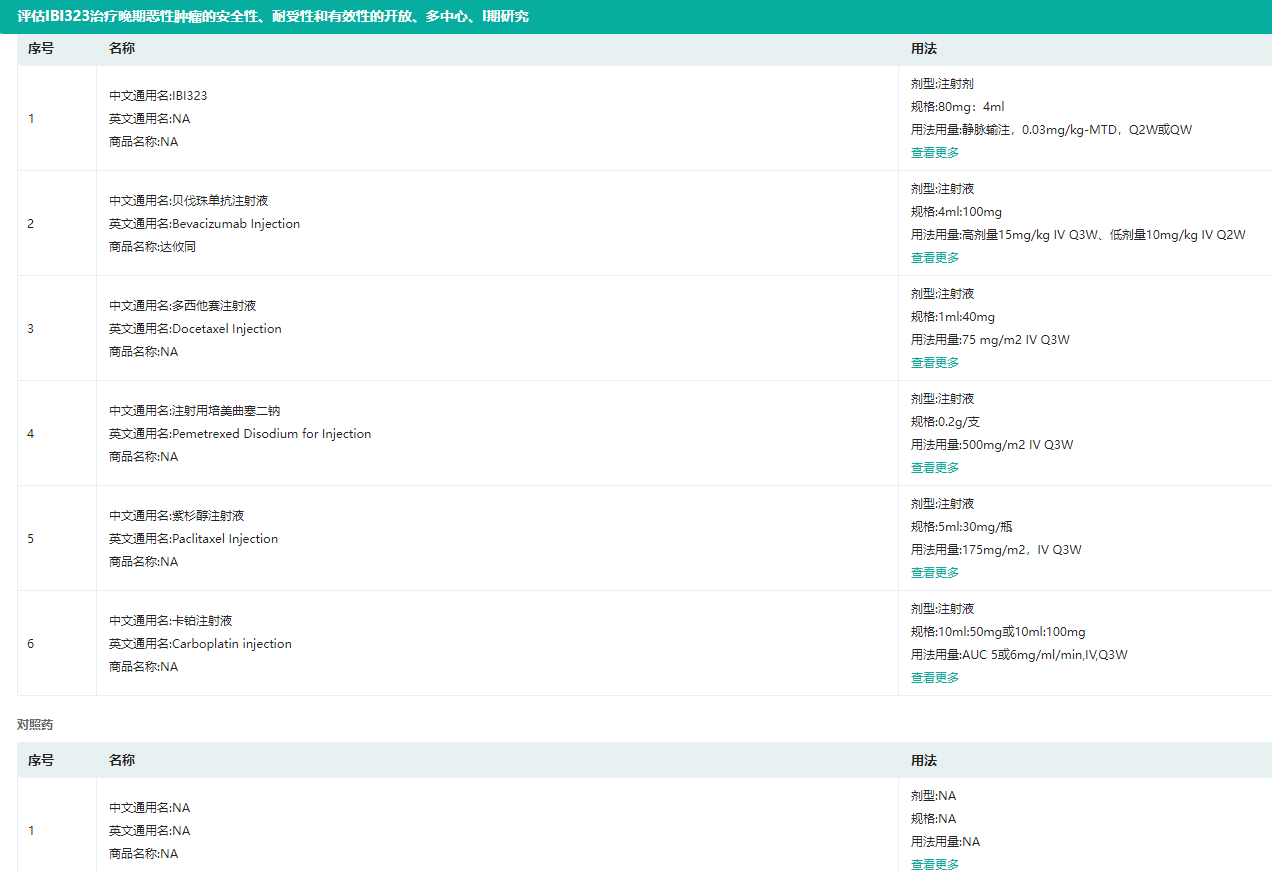
图片来源:药融云中国临床试验数据库
值得一提的是,信达生物是唯一一家,既布局了LAG-3单抗,又布局了LAG-3双抗的企业。由此可见,信达生物对LAG-3抱有很大期望。
目前,在临床试验中已证实联合疗法是可行的,那为何还有不少企业选择研发技术壁垒更高的双抗呢?答案可能是由于双抗的作用更强。
双抗的作用优势主要体现在两方面,一方面,LAG-3/PD-(L)1双抗可以激发更强的抗肿瘤协同作用。LAG3/PD-L1双抗可以桥接PD-L1阳性细胞和LAG3阳性细胞。这种桥接作用可以将表达PD-L1的肿瘤细胞与表达LAG-3的T细胞拉近,从而形成稳定的T细胞抗原受体,进一步激活T细胞,使得T细胞获得更强的免疫激活能力。另一方面,双抗具有对抗耐药性的潜力。
但是上述研究都处于早期阶段,若想进一步明确LAG-3和PD-(L)1双重阻断后协同作用的潜在机制,证明LAG-3双抗优于联合疗法,还需要更多研究。
除了疗效方面,从临床应用的角度出发,相对于联合疗法需要考虑抗体输注时间等因素,双抗的使用更加便捷。目前来看,不管是联合疗法还是双抗的研发进展都不错,相信在不久的将来,会有更多LAG-3抑制剂获批,为癌症患者带来福音。
想要解锁更多药物靶点信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握各药物靶点药物基本信息、上市药物情况、销售情况与各维度分析、药企药物研发进展、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论