
世界卫生组织总干事谭德赛说:“阿尔茨海默病夺走了数百万人的记忆、独立性和尊严,也夺走了我们所熟知和喜爱的那个人。该病不仅在身体上给人带来伤害,还夺走人的记忆,也关乎个体的尊严。”阿尔茨海默病可谓是家喻户晓的疾病之一。
据研究报道,截止目前,全球共有500万病人,每5年增加一倍,预计在2050年,将达到1.5亿人。2024年01月09日,NMPA批准了卫材药业递交的阿尔茨海默病(简称 AD)1类新药仑卡奈单抗注射液(Lecanemab),这意味着给我国阿尔茨海默病患者又带来了新的选择。与此同时,仑卡奈单抗注射液(Lecanemab)是唯一一款针对Aβ蛋白聚集体并完全获批的药物,这药物的获批,也更加证实了Aβ淀粉蛋白假说的有效性。在此之前,aducanumab也被FDA批准,不过其疗效遭到很大的质疑。
仑卡奈单抗(Lecanemab)是一种重组人源化单克隆抗体,对大脑内可溶性Aβ蛋白聚集体有高度的亲和力,通过与早期AD患者脑内异常堆积的可溶性Aβ蛋白聚集体的靶向结合,并将其隔离形成可从循环中除去的免疫复合物,从而促进患者脑部Aβ蛋白的清除,减少Aβ斑块的形成,进而缓解疾病进展。而Aducanumab是一种选择性针对聚集态 Aβ 的重组人源化 IgG1单克隆抗体,通过血脑屏障进入脑内后,该药与脑实质内的Aβ结合,清除脑内可溶性及不可溶性 Aβ 淀粉样蛋白斑块。
两者同样是单克隆抗体,为什么仑卡奈单抗(Lecanemab)可被完全批准,而Aducanumab的效果却遭到很大质疑呢?首先我们先了解这两款药物得临床效果以及药物批准情况,其次我们再来了解下淀粉样蛋白假说及Lecanemab和Aducanumab的作用机制差异。
临床效果
勃健进行了为期18个月的随机、双盲、安慰剂对照、平行组研究(301和302),评估了Aducanumab的有效性、安全性、药代动力学和药效学特性;这两项研究共招募了20个国家248个地区的3285个病人,在这些研究中,纳入了ApoE ε4携带者和ApoE ε4非携带者,结果显示Aducanumab两个研究组在高剂量和低剂量组均能够显著降低Aβ淀粉样蛋白,然而在改善患者认知的临床效果上显示(见下图1),302具有明显的效果,而301却未显示出临床效果;
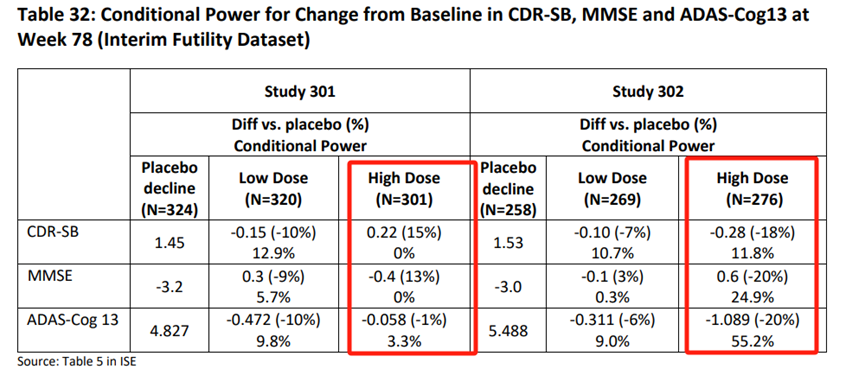
图1 Aducanumab的研究数据[1]
2020年11月06日,aducanumab的研究结果提交给FDA专家委员会,许多成员认为该研究结果不充分。FDA专家委员会针对以下四个问题进行讨论:
(a) “不考虑研究组(301) (ENGAGE) 的研究数据,研究302 (EMERGE) 是否有足够的证据证明aducanumab作为阿尔茨海默氏病治疗的功效?” ;表决结果:1票同意,8票反对,2票弃权;
(b) “PRIME 试验是否提供证据支持 aducanumab 的治疗功效?”;表决结果:0 票同意,7 票反对,4 票弃权;
(c) “PRIME 研究是否为 aducanumab 对阿尔茨海默病病理生理学的药效学功效提供了足够的证据?” ;表决结果:5票同意,0票反对,6票弃权;
(d) “当将试验 301 和试验 302 的探索性分析结果与试验 103 及其对阿尔茨海默病病理生理学的药效学作用一起考虑时,您是否认为试验302的结果证明了 aducanumab 作为治疗药物的功效?阿尔茨海默病的治疗方法?”;表决结果:0 票同意,10 票反对,1 票弃权;由此得知,大部分专家委员认为aducanumab没有足够的证据证明有效。
根据Lecanemab的临床研究(Clarity AD)[2],该项研究共纳入1795 名受试者,其中Lecanemab组898名,安慰剂组897名。两组 CDR-SB 基线水平均约为3.2分;第18个月时,Lecanemab组和安慰剂组较基线分别变化 1.21 分和 1.66 分,改善 0.45 分(P<0.001)。关键次要终点中,仑卡奈单抗组也比安慰剂组表现更优:ADAS-Cog14 减少1.44 分,ADCOMS 减少0.05 分,ADCS-MCIADL增加2.0 分(均P<0.001)。698 名受试者的亚组分析结果显示,仑卡奈单抗组受试者脑内淀粉样蛋白负荷比安慰剂组少59.1 centiloids(P<0.001)。Clarity AD 结果表明,仑卡奈单抗达到了主要临床终点和所有关键次要终点。并且在2023年07月06日,FDA专家委员会全票通过,Lecanemab获得全面批准。
了解完药物的临床效果,接下来,我们来了解下阿尔茨海默病淀粉样蛋白假说的产生机制。
淀粉样蛋白假说
25年以来,淀粉样蛋白假说一直是AD疾病的主流机制,Aβ主要来源于APP,APP通过β-分泌酶和γ-分泌酶分解,形成Aβ,并释放至细胞外;在正常人,Aβ能够被快速分解和清除;然而在老年人或病理状态下的人,Aβ被降解的能力变弱,于是,Aβ多肽被聚集。Aβ多肽聚集的主要成分是两种多肽,一种是Aβ40,另一种是Aβ42,它们分别是含有40个和42个氨基酸的多肽,其中Aβ42的疏水性强于Aβ40,Aβ42的水平或者比例增加,会诱导Aβ淀粉样原纤维的产生;Aβ淀粉样原纤维的进一步累积发展成老年斑。这个老年斑会诱导tau蛋白病理变化,这些将会导致神经元死亡和神经退行性变。
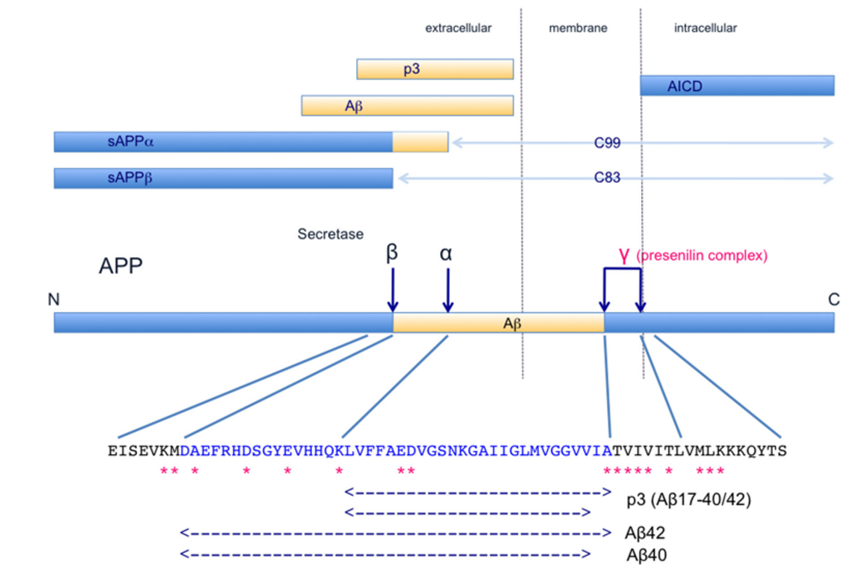
图2 Aβ产生过程[3]
根据早期研究结果显示,在大鼠和猴的大脑皮质中,注入Aβ多肽,发现注射部位坏死,周围神经元缺失及神经角质增生,并与剂量有明显相关性。Aβ对神经系统的毒性作用主要会使血管壁淀粉样变直接导致血管硬化,弹性变差,甚至容易破裂或形成血栓,还诱使神经细胞过早凋亡。动物实验显示,Aβ对神经元的作用与其状态有关。溶解状态的Aβ在短时间内可促使神经元生长,提高神经元的存活率,而沉积状态的Aβ对神经元呈现相反的作用,引起与阿尔茨海默病相似的病理变化—神经退缩和神经元变性,最显著地改变发生在衰老的哺乳类动物大脑。
作用机制差异
由上面的作用机制,我们得知,Aβ多肽的聚集是导致AD的主要原因,然而Aβ多肽的形式多样,包括单体、大小不一的可溶性低聚物(比如低聚物和原纤维)以及斑块中不溶性纤维,另外,不同的药物作用不同形式的Aβ多肽效果将会出现不同的临床效果;根据一项研究显示,Lecanemab和Aducanumab这两种抗体都是针对Aβ聚集形式的单克隆IgG1抗体,Lecanemab是小鼠mAb158抗体的人源化单克隆抗体,主要是针对可溶性聚集体(低聚物和原纤维),在I期临床试验中,Lecanemab显示了明显的斑块清除能力;而Aducanumab是重组人源单克隆抗体,它主要是针对5~7个氨基酸的Aβ多肽,根据其3期临床试验的数据表明,Aducanumab无法满足主要终点后,Aducanumab的开发于2019年停止。根据研究显示,Lecanemab在浓度为10ng/ml或者更高浓度的时候,其原纤维几乎全部耗尽;而Aducanumab在1000ng/ml以上,原纤维被耗尽,也就是说,Lecanemab与可溶性低聚物(原纤维)的结合强于Aducanumab。而Lecanemab和Aducanumab对单体结合几乎是一致的,两者的有效抑制浓度(IC50)>25uM,说明两者与单体结合能力较弱。
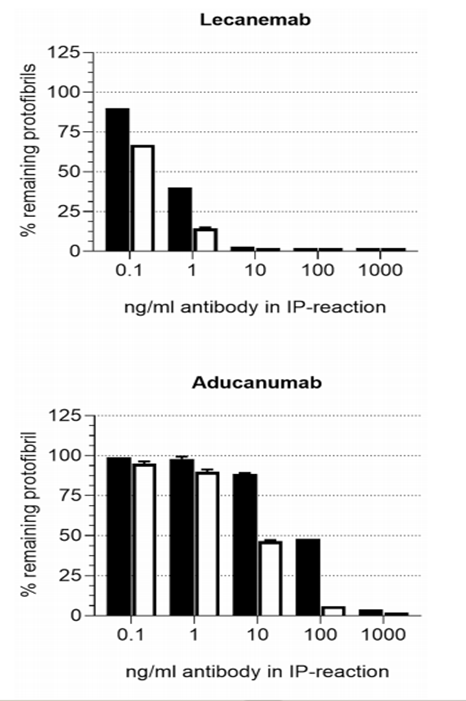
图3 Lecanemab和Aducanumab结合可溶性低聚物[3]
通过使用Lecanemab和Aducanumab去除大脑中的可溶性原纤维发现,Lecanemab的EC50明显小于Aducanumab,进一步证明Lecanemab去除大脑中的原纤维效果更好。也许这就是导致Lecanemab在III期临床效果与Aducanumab差异的原因。
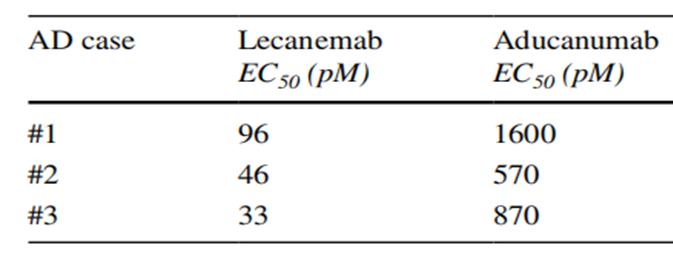
图4 Lecanemab和Aducanumab去除大脑中的可溶性原纤维EC50[3]
另外,根据相关文献报道,Lecanemab不但可以选择性结合Aβ低聚物,同时延缓Tau 病变 ,这一双重作用也让Lecanemab的效果更好。
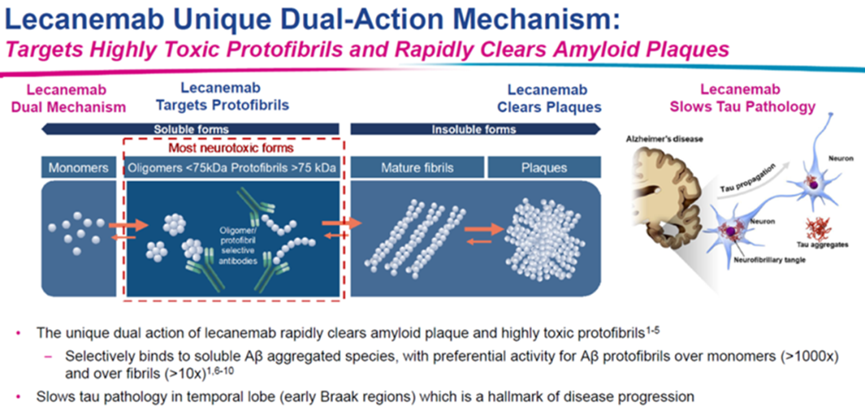
图5 Lecanemab的作用机制[4]
血脑屏障(BBB)
治疗脑部疾病,最大的一项技术挑战是如何突破血脑屏障,特别对于大分子药物,水溶性较好的药物,因为这种类型的药物通常比较难穿过血脑屏障。那么Lecanemab和Aducanumab它们通过如何突破血屏障而发挥作用呢?
有研究表明,Aducanumab可以穿过血脑屏障,主要给出了三个理由;第一,AD患者接受Aducanumab治疗后,淀粉样蛋白确实减少;第二个原因,Aducanumab会导致与淀粉样蛋白相关的大脑影像学异常,这表明了BBB被破环;第三个原因:淀粉蛋白减少与大脑淀粉样蛋白相关的影像学异常成线性关系,这可能是随着抗体治疗后大脑的血脑屏障被破坏,所以导致与淀粉样蛋白相关的大脑影像学异常。
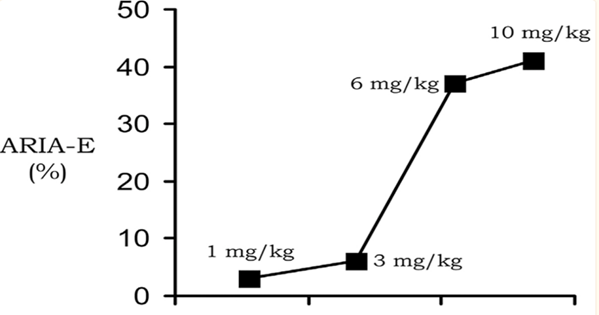
图5 Aducanumab的剂量与ARIA-E关系[4]
然而,有另一项研究认为,Aducanumab的脑体积分布为1微升/Gram,是脑血浆体积的5%,但是对于生物制剂来说,大脑的体积分布与脑血浆体积接近,如果治疗性抗体药物的脑体积分布不大于脑血浆体积,那么该抗体不会通过血脑屏障。
因此,研究认为Aducanumab在大脑中脑浓度几乎可以忽略不计,这就可能是它本身就困在脑血容量中,并没有穿过血脑屏障。那么问题来了,既然它不会穿过血脑屏障,那么它为什么有脑浓度?通过一项研究得知,静脉注射HRP后,小鼠大脑组织化学发现,HRP是一种40kDa的蛋白质,不会穿过血脑屏障,也不会进入大脑,除了大脑的微小区域,即缺乏BBB的室周区域,也就是说,大脑中还存在一种区域,这个区域是位于第三脑室底部的正中隆起处,下图是大脑这一区域对HRP的摄取,也许这就能够解释为什么Aducanumab在大脑中有一定脑浓度。
总体来说,不管Aducanumab是否会突破血脑屏障,Aducanumab在大脑中的脑浓度是相当低的,这也许是Aducanumab的临床效果不好的一大原因。
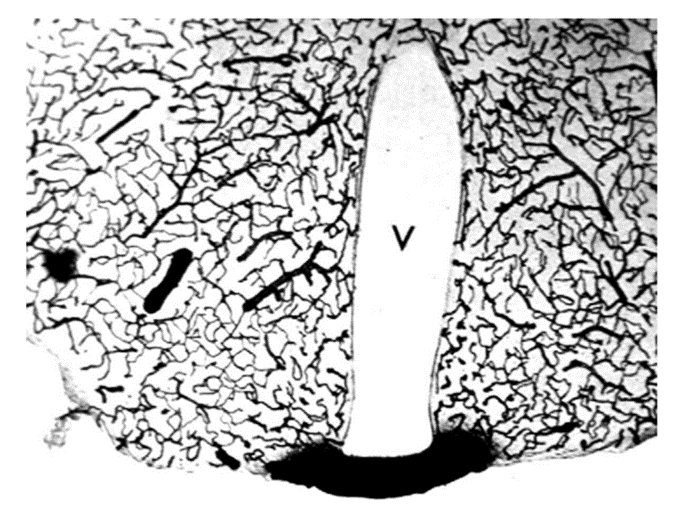
图6 大脑区域对HRP的摄取[4]
综上所述,造成aducanumab与Lecanemab的效果差异主要有几点:第一,两者作用Aβ聚集形式有一定差异,与aducanumab相比,Lecanemab对原纤维结合效果更好;第二,aducanumab在大脑中的脑浓度较低。
参考文献
[1] Food and Drug Administration. Peripheral and Central Nervous System (PCNS) Drugs Advisory Committee Meeting November 6, 2020. https://www.fda.gov/media/143502/download. Accessed June 20, 2021.
[2] 田欣,梅丹治疗早期阿尔茨海默病的新药仑卡奈单抗(lecanemab)药物发现 2023 年第 04 期
[3] Fuyuki Kametani* and Masato Hasegawa* Reconsideration of Amyloid Hypothesis and Tau Hypothesis in Alzheimer's Disease Front. Neurosci., 30 January 2018 https://doi.org/10.3389/fnins.2018.00025
[4] Linda Söderberg Lecanemab, Aducanumab, and Gantenerumab — Binding Profiles to Different Forms of Amyloid‑Beta Might Explain Efficacy and Side Effects in Clinical Trials for Alzheimer’s Disease Neurotherapeutics (2023) 20:195–206 https://doi.org/10.1007/s13311-022-01308-6
[5] Aβ抗体Lecanemab再创里程碑:皮下注射更有效、更安全https://mp.weixin.qq.com/s/7yw1c7X6NC5t-as4zyBNoQ
[6] William M. Pardridge* Receptor-mediated drug delivery of bispecific therapeutic antibodies through the blood-brain barrier Published online 2023 Jul 10. doi: 10.3389/fddev.2023.1227816
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论