
近日,我会按法定程序同意以下企业科创板首次公开发行股票注册:江苏亚虹医药科技股份有限公司。上述企业及其承销商将与上海证券交易所协商确定发行日程,并刊登招股文件。

关于亚虹医药(来自公司官网)
亚虹医药成立于2010年3月,是一家专注于泌尿生殖系统肿瘤及其它重大疾病领域的全球化创新药公司。秉承“改善人类健康,让生命更有尊严”的企业使命,亚虹立志成为在专注治疗领域集研发、生产和商业化为一体的国际领先制药企业,为中国和全球患者提供最佳的诊疗一体化解决方案。
公司坚持以创新技术和产品为核心驱动力,通过打造自有的研发平台和核心技术,深入探索药物作用机理,高效率筛选评价候选药物。通过内部完善的研发体系和全球药物开发经验专长,亚虹致力于在专注治疗领域推出全球首创(First-in-Class)药物和其它存在巨大未被满足治疗需求的创新药物。
同时,亚虹通过自主研发和战略合作,围绕泌尿生殖系统疾病进行产品管线的深度布局,高度关注该领域的技术前沿和治疗发展趋势,洞察并挖掘未被满足的临床需求,前瞻性地进行产品规划和生命周期管理,打造从疾病诊断到治疗的优势产品组合,从而造福更多的中国和全球患者。
产品管线进展情况
截至本招股说明书签署日,发行人正在开展 9 个产品的研发工作,其中,2 个创新产品的 3 项研究已处于 III 期或关键性临床试验阶段。
APL-1202 项目在非肌层浸润性膀胱癌(NMIBC)领域现有两项适应症在国内分别进入关键性或 III 期临床试验阶段:(1)联合化疗灌注二线治疗复发的中高危 NMIBC;(2)单药一线治疗未经治疗的中危 NMIBC。APL-1202 联合化疗 灌注二线治疗复发的中高危 NMIBC 适应症预计于 2022 年向国家药监局提交上市申请。在肌层浸润性膀胱癌(MIBC)领域,发行人于 2021 年 6 月取得美国 FDA 关于 APL-1202 与替雷利珠单抗联合治疗 MIBC 的 I/II 期临床试验的许可,目前正筹备于美国启动临床入组,于 2021 年 9 月末获得中国 CDE IND 批准。
APL-1702 是集药物和器械为一体的光动力治疗产品,主要用于治疗包括所有 HPV 病毒亚型感染所致的宫颈高级别鳞状上皮内病变(HSIL,一种高级别的宫颈癌前病变)。APL-1702 已处于国际多中心 III 期临床试验阶段,发行人预计 将于 2022 年四季度率先在中国提交 APL-1702 的上市申请。
发行人聚焦于泌尿生殖系统肿瘤及其他重大疾病领域,致力于为患者提供诊疗一体化解决方案。目前公司核心产品均处于在研状态,主要产品管线拥有 9 个 产品、12 个在研项目,所处研发阶段如下图所示:
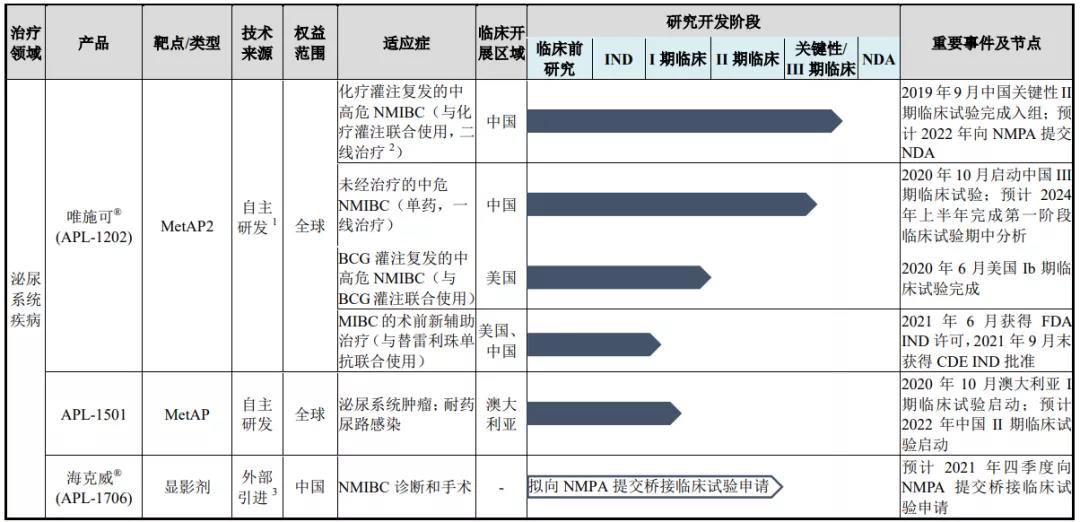

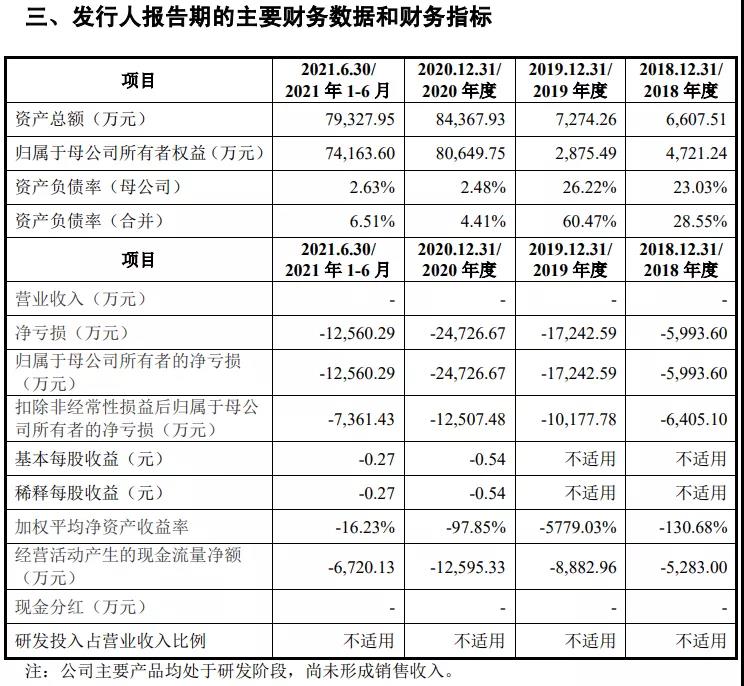
发行人技术先进性、研发技术产业化情况
经过十余年的积累和发展,发行人已经构筑了覆盖药物发现及机制研究、临 床前开发、药学研究、转化科学研究、中国和全球临床试验、法规与注册申报的 完整研发体系。在上述完整、高效的研发体系的基础上,结合多年的药物临床研 发实践,发行人构建了三大核心技术平台,开发出多个新型候选药物并有序推进 至临床阶段。
(1)靶向免疫调节正常化(Targeted Immune and Modulation Normalization, TIMN)技术平台系发行人自主研发构建的集体外、体内模型以及转化科学研究 为一体,同时在药物作用靶点和机制上专注于靶向调节肿瘤免疫微环境及治疗自 身免疫疾病的新药发现平台。基于该技术平台,发行人研究发现 APL-1202 可以 在肿瘤免疫微环境中增强免疫细胞功能,并具有增强 PD-1 单抗药效的作用。据此研究成果,发行人于 2021 年 6 月取得美国 FDA 关于 APL-1202 与替雷利珠单 抗联合治疗 MIBC 的 I/II 期临床试验的许可,目前正筹备于美国启动临床入组, 于 2021 年 9 月末获得中国 CDE IND 批准。此外,发行人基于 TIMN 技术平台及 神经递质调节免疫功能的机理,发现了具有抑制免疫活性作用的化合物 APL-1401,有望成为自身免疫疾病领域具有全新作用机制的新药进入临床试验。
(2)前药和精准药物递送(Prodrug and Accurate Drug Delivery,PADD)技 术平台具备药物前药化学结构改造和药物递送系统改进的双重功能。通过对原药 特定基团进行结构改造,并结合药物缓控释制剂技术,从而获得药效、安全性、 给药途径等方面更优越的新药产品。发行人通过该技术平台开发出 APL-1501、 APL-1901 等在研产品。其中,APL-1501 已于 2020 年 10 月在澳大利亚获批开展 I 期临床试验,后续拟在泌尿系统肿瘤及耐药尿路感染等适应症上进行开发。
(3)基于分子片段组装的靶向蛋白降解(Fragment-Based Assembling & Selectively Targeting Chimeras,FASTac)技术平台系发行人在靶向蛋白降解技术 基础上,通过建立高成药性分子片段库,以提升靶向蛋白降解剂成药性并高效筛 选出目标化合物的技术平台。发行人已利用 FASTac 技术平台筛选出高效的目标 靶向蛋白降解剂 ASN-1764 和 ASN-1780,目前发行人正在积极进行两个化合物 的临床前研究工作。
参考来源:
--证监会发布
--公司官网http://www.asieris.cn/
--上市公司招股书






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论