注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及)。因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。
导 语
肽(peptide)是α-氨基酸以肽键连接在一起而形成的化合物,是蛋白质水解的中间产物。多肽通常是指10-100个氨基酸通过肽键链接而成的化合物,是生物体内天然存在的生物活性物质,广泛参与和调节体内各个系统、器官、组织和细胞的生命活动,具有重要的作用和意义。
多肽由于其日渐成熟的合成纯化技术与制剂技术,市场及患者对其的接受度日渐增高。其中多肽类产品包含用于疾病预防、诊断和治疗的多肽药物或其修饰物,美容多肽,以及非药物领域多肽,包括多肽食品,健康产品,生物材料,兽用多肽等。
全球多肽药物市场情况及多肽CDMO情况
1920s胰岛素在欧美的开发开启了多肽药物商业化的大幕,1970s以Takeda为代表的日本企业开始研发多肽药物,而中国企业自1980s起崭露头角。
目前多肽药物已广泛应用于肿瘤、肝炎、糖尿病、艾滋病等疾病的预防、诊断和治疗,其中主要产品用于治疗糖尿病等代谢疾病。拥有多肽重磅药的厂家普遍是全球Big Pharma。多肽制剂市场集中度高,包括几款最新的胰岛素:德谷、甘精、门冬,以及GLP-1的索马鲁肽、利拉鲁肽,都是多肽类药物,2020年全球这些药物共同组成了超过620亿美元的大市场,并且仍在保持一定的增速。
全球肽类药物市场按地区划分的明细,2016-2030年(估计)
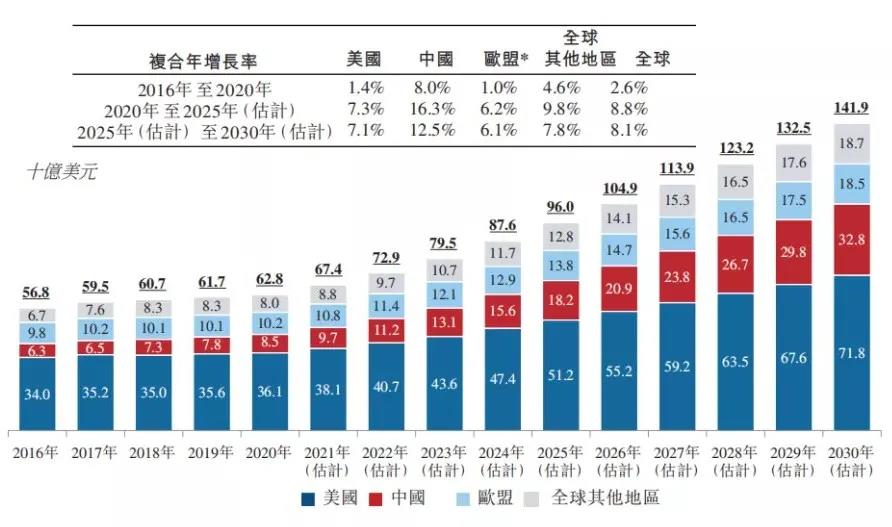
附注:1. 肽类药物包括胰岛素药物和非胰岛素肽药物。2. 欧盟五国包括英国、法国、德国、西班牙及意大利。资料来源:弗若斯特沙利文分析
多肽药物在罕见病、慢性病等领域涌现了不少重磅新药。其特异性和选择性好的优势较为突出,使用很低的浓度就有很高的药效。随着部分产品的生产工艺日渐成熟,欧美等制药企业和创新药企业会选择原料药和制剂的CDMO,目前全球多肽CDMO市场约为20亿美元,并且保持着13.3%的年化增速。
按地区划分的全球肽CDMO市场明细,2016-2030年(估计)
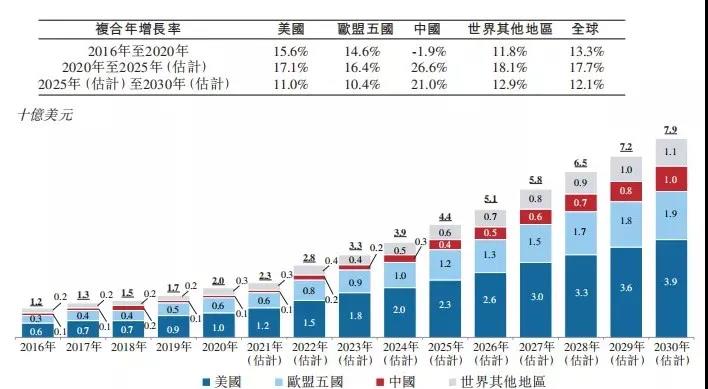
附注:欧盟五国包括英国、法国、德国、西班牙及意大利。资料来源:弗若斯特沙利文分析
近些年,多肽药物作为国内外生物医药创新研发的重点领域,一直保持良好的发展前景。由于多肽药物研发难度高,价格昂贵,生产工艺特殊,为了节约成本和降低研发风险,药企往往在研发早期就会选择与CDMO/CRO企业进行合作。
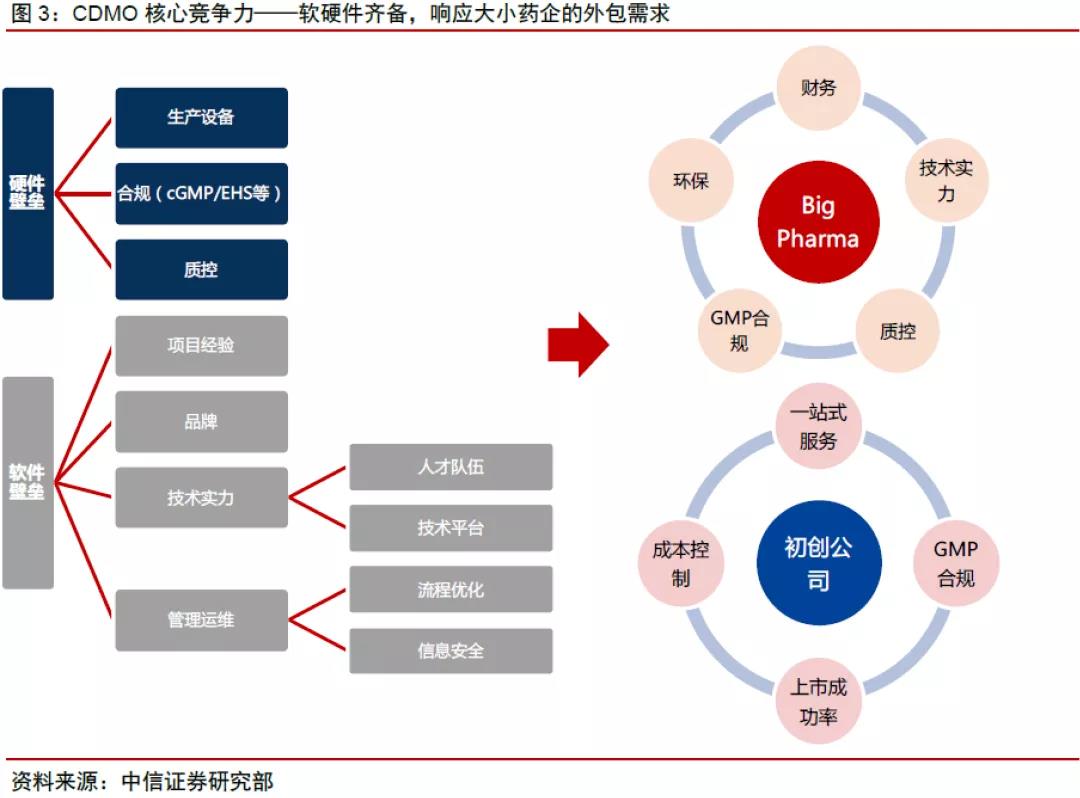
国外多肽主要CDMO供应商
01 瑞士巴亨公司(Bachem):

Bachem由Peter Grogg创始于1971年,总部位于瑞士Bubendorf,专注于肽合成;1978年首次根据cGMP制造了用于医药的多肽;1987年-1993年,先后在美国、德国、法国开展业务;1998年,在瑞士IPO上市。专注于多肽和复杂有机分子的工艺开发和制造,在肽研究方面拥有近50年的经验,在世界合成多肽市场占有垄断地位。
通过收购美国Peninsula Laboratories、瑞士Sochinaz SABachem,Bachem将在治疗用活性肽的强势地位扩展到到免疫学领域;2007年,Bachem收购了Clinalfa品牌的即用型临床试验材料和相关服务;2013年,Bachem与日本GlyTech共同开发了用于工业规模的干扰素β-1a,在糖肽和糖蛋白生产领域携手合作;2015年,Bachem收购了美国Peptide公司,从小规模目录业务和定制合成到cGMP下的大规模制造,再次扩大了制造能力。
02 PolyPeptide:

于1952年在瑞典马尔默建立,曾是辉凌医药(Ferring)的肽类生产基地;1996年,顺应市场需求,PolyPeptide成为独立的生产企业、辉凌的兄弟公司,专注于药用肽合同开发和制造(CDMO)。
目前在美国、法国、瑞典、比利时、印度有6处GMP生产设施,拥有世界一流设备和生产水平,支撑着PolyPeptide 2000kg原料药和公吨级中间体的超级年产能。全球已上市超过90个多肽药物,其中30%的原料药供应来自PolyPeptide,他能够提供多肽原研药和仿制药的GMP标准规模化生产。PolyPeptide致力于发展多肽生产领域新技术,革新现有工艺,推动多肽生产自动化和环保水平。
60年的肽类市场战绩,使PolyPeptide成为全球最大的药用肽合同开发和制造商(CDMO)之一。对大小项目技术需求能灵活配合,对生产和放大技术驾轻就熟,兼具丰富的监管机构审查经历,无论是与小型初创型生物技术公司还是大型制药企业合作,PolyPeptide都能满足客户各阶段的需求。
03 龙沙集团(LonzaGroupLtd.):

1897 年成立于瑞士小镇 Gampel,目前总部位于瑞士的巴塞尔,并在瑞士证券交易所上市。进入 21 世纪,Lonza 已完全定位CDMO 企业,向跨国制药公司和生物制药公司提供综合的医药定制研发生产服务,是全球少数几家能够为生物制品提供定制研发生产服务的医药定制研发生产企业。
2014年后随着全球生物创新药的崛起,相应 CDMO 外包市场迅速扩大,公司前期的一系列布局开始兑现业绩,股价也转而走高。2019 年,公司营业收入达 59.2 亿瑞士法郎,是全球 CDMO 绝对龙头。
国内多肽主要CDMO供应商
相比欧美日企业,各类技术融合应用,技术多元,既符合创新药研发的探索性需求,又符合规模生产的产业化需求,中国企业侧重于生产制造和工艺优化。近几年由于全球疫情的影响,欧美的多肽CDMO产业逐渐向中国转移,小分子CDMO争相进入多肽领域,发展迅速。大量涌入的定制需求推动了国内多肽CDMO企业和生物技术企业的进步。未来中国将出现一批多肽CDMO标杆企业。
由于多肽产业和其发展历程的独特性,多肽CDMO的生产方式呈现多元化。根据药融云资料显示,目前国内多肽的CDMO企业有以下4类:
1. 定制肽服务(CRO)转型多肽CDMO
从事多肽新药发现的研究机构、企业众多,但建设有专业多肽药品开发报批团队和生产设施的少之又少,即使全球跨国大药企一般也是通过委托定制生产的形式获取原料药。因此CRO企业目前在多肽行业中几乎占一半的比重。随着资源的积累和行业经验的加深,以及服务客户逐步进入商业化阶段,为了继续获得更稳定的商业化阶段订单,CRO企业会向CDMO领域拓展延伸。目前中肽生化、中晟全肽、吉尔生化等都是这类模式的标杆企业。
2. 多肽原料药(API)转型多肽CDMO
国内有一批企业以多肽仿制药和API起步,顺利实现原始积累,并进一步对新产品、新制剂技术、国际化、创新药等进行布局,实现跨越发展。同时企业的软硬件实力、研发和生产方面的积累和以及行业经验和资源,可以通过CDMO的方式进行变现。依靠此类模式发展的企业有深圳健元、成都圣诺、江苏诺泰、深圳翰宇等。
3. 直接进入多肽CDMO
一些有丰富多肽行业从业经验和国外客户资源的创业团队通过资本助力,快速进入多肽CDMO领域,这类企业有上海昂博、浙江湃肽等
4. 小分子CDMO拓展多肽CDMO
多肽药物现在已经成为整个药物市场的热点板块,逐渐有越来越多的头部CDMO企业将业务拓展到多肽CDMO。并且由于此类CDMO企业在软硬件的实力和人员配置方面都有过硬的条件,多肽CDMO业务的发展非常迅速。这类企业包括凯莱英、合全药业等。
重点企业介绍
01 健元医药

深圳市健元医药科技有限公司(以下简称健元医药)于2009年创建,致力于多肽及多肽相关产品的研发、生产、销售。健元医药有2个研发中心 + 3大生产基地(20条多肽API生产线,目前12条已投产使用)。其拥有的逐级放大技术,能满足不同批量的需求,从mg级到50kg/批,是国内化学合成多肽原料药生产规模最大的企业之一。
健元医药的核心研发团队已有20多年的多肽经验,曾两次通过FDA检查。健元医药完整高效的多肽产业化体系,为客户提供全方位的多肽产业化服务,包括药物肽、兽用肽、抗菌肽、美容肽的研发及生产,注册以及相关的法规支持。

02 翰宇药业

深圳翰宇药业股份有限公司成立于2003年4月,是专业从事多肽药物研发、生产和销售的“国家高新技术企业”。公司于2011年在深圳证券交易所上市。
公司主营产品包括注射用生长抑素、注射用特利加压素、去氨加压素注射液、注射用胸腺法新、注射用胸腺五肽等产品。作为中国多肽药物研发和生产领军企业,翰宇药业拥有22个多肽制剂批准文号、9个新药证书和17个临床批件,是国内拥有多肽药物品种最多的企业之一。
03 中肽生化

中肽生化有限公司成立于2001年,总部位于浙江杭州,专注多肽行业近20年,是值得信赖的全球一体化多肽CRO/CDMO合作伙伴。中肽在国内和美国硅谷均设有研究基地,并坚持遵循高效、优质、专业、创新的理念和为客户创造“优秀价值”的服务宗旨,多年来致力于多肽类新药和仿制药的原料药研发、申报及大规模商业化生产。
中肽提供了从早期研发到商业化生产包括方法开发及验证、工艺开发及验证、稳定性研究、杂质研究、制剂研发及国内外法规支持的一站式服务。
结 语
多肽药物近年来可谓是风头正劲,虽然在全球生物医药市场中占比较小,但发展迅速。目前我国创新药研发热度与日俱增,医药投资也在蓬勃发展,多肽合成技术和多肽药物设计理论的成熟将增强我国多肽创新药研发的国际竞争力,同时也将持续推进多肽CDMO行业的快速发展。
参考资料:
1. 药融云数据
2. 必读:多肽药物行业市场现状及发展趋势分析
3. 各公司官网
4. 《多肽药物企业竞争分析》
5. 国内外主要多肽制药企业简况
6. 多肽药物的江湖 | 创仿药/API/CDMO齐发力
7. 多肽药物市场研究与分析
8. 700亿多肽药物市场,欧洲原料药企倾巢而来-Polypeptide能力
9. 瑞典多肽类药物供应商,和它的新技术
10. 多肽药物原料药市场-CRO\CMO\API三机梯队
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论