
在将药物输送到人体的各种途径中,由于患者的顺应性,口服途径是最优选的。可以使用不同的剂型,例如片剂、液体(溶液、混悬液等)和胶囊,实现通过口服途径的药物递送。固体剂型约占所有可用剂型的三分之二。新药开发中制剂剂型的选择更是以普通口服固体制剂居多。制粒是药物剂型生产中最重要的单元操作之一。在制药行业中,制粒是指将粉末混合物(通常由药物和辅料组成)混合并通过干压法或通过使用粘合剂溶液,分别称之为干法制粒和湿法制粒。除了常见的制粒工艺,随着辅料种类的不断丰富,粉末直压/粉末直灌工艺也活跃起来;当然,随着药物不良的理化性质的出现,对于革新的技术也提出了要求,比如对于难溶性药物需要喷雾干燥或者热熔挤出造粒以制备无定形固体分散体。根据API的理化性质,如何选择合适生产工艺,生产分类系统MCS或许就是用来回答这个问题的。根据生产分类系统(MCS)可知,MCSⅠ-Ⅳ的生产工艺步骤(如图1所示),复杂性以及成本逐步增加,但是承受API不良物理性质(机械性质)能力逐步增加,同时承受API不良化学性质(湿热稳定性)能力降低,对于API物理化学稳定性带来风险的可能性越来越大。
生产分类系统(MCS):
- (Ⅰ)Direct Compression(DC)
- (Ⅱ)Dry Granulation(DG)
- (Ⅲ)Wet Granulation(WG)
- (Ⅳ)Other Technologies(OT)
粉末直压/直灌:粉末直接压片或者粉末直接灌胶囊,仅仅包含两个主要步骤,指的是原料药与合适辅料(填充剂,崩解剂和润滑剂等)混合均匀后制剂进行压片或者灌胶囊。与干法制粒和湿法制粒相比,工艺简单。此种类型的工艺对API性质的依赖性最强,API的性质不仅仅是需要可以接受,而是这些性质能够保持一致性,特别是API的粉体学性质,如API的颗粒大小,形态以及密度等性质在各批次间发生变化,将对混合颗粒的混合均匀性产生影响,进而可能造成产品出现含量及含量均匀性问题。如有必要,需要对API的粒径及粒度分布制定标准,以保证生产产品的一致性。当然,如果API的其他性质,如形态,对于产品的质量(中间体的流动性、混合均匀性)造成影响,也需要进行表征和控制。以上标准的制定依赖于各个项目中API的实际的性质以及其对于产品COAs的影响,进而建立API及辅料CMAs的限制。有些情况下,辅料的粒度,形态,密度等性质也需进一步的限制,具体情况具体分析。
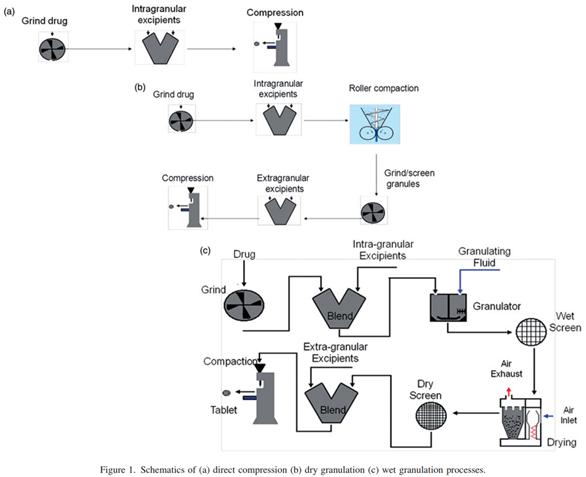
图1三种主要的通用口服固体制剂工艺路线(参考文献1)
粉末直压绝对优势分析:
- 节省资源
采用粉末直接压片法不仅能保证产品质量稳定,同时能降低生产成本,提高企业经济效益。
- 助力片剂的崩解
采用粉末直接压片法制备片剂时,其崩解剂不会由于前期接触水分而降低崩解性能,从而保证了良好的崩解特性。另外,由于没有进行制粒压片,片剂崩解后不会形成大团状颗粒,而是形成比表面积相对较大的细粉,可以较好地分布在体内,有助于药物的释放、吸收。
- 增溶作用
采用粉末直接压片工艺,选用亲水性好的辅料(例如乳糖)作为填充剂,在保证片剂迅速崩解的前提下,药物连同乳糖粉末在水中分散均匀,继而乳糖溶解并在药物表面借助范德华力和水形成氢键,从而降低药物的疏水性,有助于提高药物的溶出度。
- 提高稳定性
化学性质不稳定的药物在湿法制粒过程中易发生水解,或在干燥过程中受热破坏,采用粉末直接压片法制备过程无需制粒干燥,药物不受湿热影响,更好地保护了药物的稳定性。
虽然粉末直压/直灌具有那么多的优势为什么仍旧没有被更多的企业所采用呢?
首先,粉末直压所选用的辅料需要其具有良好的粉体学性质,需要特殊复杂的工艺制备,一般比较贵,有些公司及其领导可能碍于投入的管控,把粉末直压/直灌作为最后选择的工艺;一旦选择了直接压片/直接灌胶囊,如果后续开发中出现了工艺的变更,需要做重大变更处理,可能需要做临床的桥接研究,对于工艺不够自信;根源可能在于技术问题,对于原辅料自身的粉体学控制(如可压性、流动性、稀释潜力、含量均一性、润滑敏感性等),生产效率(如压片速度)和生产线利用率等。
干法制粒:首先将药物粉体与辅料混合,然后将混合物加入螺旋进料机构,粉体经过螺旋进料机构的输送到达辊压区域,在辊压区域内被压制成片体,出料片体在整粒机构中被旋转刀片打碎成为符合标准的药物颗粒,完成整个干法制粒生产过程。
进料机构、辊压机构、破碎机构、整粒机构等是干法制粒机的主要工作部件,其中进料机构和辊压机构是干法制粒机的核心部件。药物粉体经过进料机构被输送到辊压机构,在辊压机构中被压制成片体,出料片体的密度和硬度决定了片体质量的好坏,进而决定了药物颗粒收率的高低。研究粉体在进料机构中的运动过程和在辊压机构中的受压成型过程有助于了解操作参数、几何参数和摩擦系数对药物粉体辊压成型的影响,从而指导干法制粒机的设计生产和操作参数选择,提高干法制粒机的生产效率。

图2干法制粒粉体碾压成型示意图(参考文献2)
Johanson将粉体在辊压机构中的运动划分为三个阶段,分别是Slip区(滑移区)、Nip区(啮合区)和Release区(释放区),粉体的压片过程主要是在Slip区和Nip区实现的。药物粉体通过螺旋进料机构被运送到辊压机构,粉体在刚进入辊压机构时运动速度小于轧辊轮表面线速度(此时粉体位于Slip区),粉体被轧辊轮带动前进,前行一段距离后,靠近轧辊轮表面处的粉体运动速度与轧辊轮表面线速度达到一致,粉体进入Nip区,粉体在Nip区中受压为片体,出料片体进入Release区,完成压片过程。细化干法制粒碾压的成型过程,找到影响终极那颗粒关键理化性质CQAs的关键工艺参数CPPs。
干法制粒常用于热敏性物料、遇水易分解的药物以及容易压缩成型的药物的制粒。较湿法制粒,干法制粒的优势是工艺过程中不涉及水分和热量,适合湿热敏感物料制粒。同时,干法制粒占用空间较小,适合连续化生产。大部分适用于粉末直压的理想性质同样适用于干法制粒,除了与流动性或堆密度相关的性质。与粉末直压/直灌相比,干法制粒提供额外的压制步骤,API与其他辅料部分致密化而形成粒子,对于API的性质具有更大的容忍度。
当然,干法制粒也有一些小问题:干法制粒不适用于可压性或二次可压性较差的物料;由于高压制粒,颗粒密度较高,可能减缓产品的溶出;对于压力不稳定的API(如压力转晶),也不能使用干法制粒工艺。
湿法制粒:在湿法制粒过程中,通过在粉末混合物中添加液体/干粘合剂来生产颗粒。该药物与辅料混合,并使用溶剂(水性或有机溶剂)进行加工,随后进行干燥和研磨以生产颗粒。混合到粉末中的溶剂可以在粉末颗粒之间形成足够强的结合,从而将它们锁定在一起。然而,在液体干燥后,一些粉末可能会散开。在这种情况下,需要含有粘合剂的液体溶液。当涉及对水敏感的药物或需要快速干燥颗粒时,使用有机溶剂,例如乙醇。此外,可以使用稳定剂,例如与药物紧密接触的pH调节剂,这可以最大限度地提高产品稳定性。除去或干燥溶剂后,粉末混合物形成更稠密的团块。在传统的湿法制粒方法中,软材被强制通过筛子以产生预先确定大小的湿颗粒,然后将其干燥。随后的后干燥、筛选/研磨步骤将附聚物破碎成具有所需粒度和分布的颗粒。
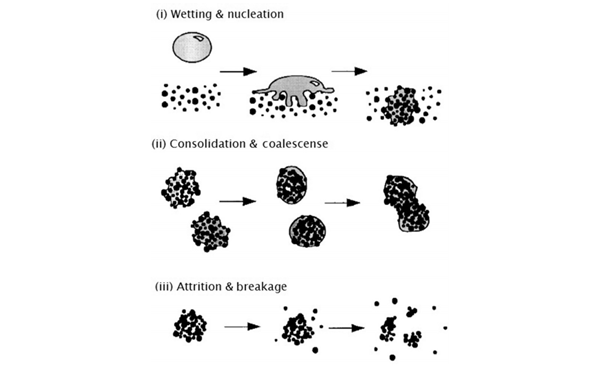
图3 湿法制粒机理(参考文献3)
湿法制粒颗粒形成的机制涉及以下三个过程:
a.润湿和成核(Wetting and Nucleation)
液体粘合剂与干粉床接触并通过干粉床分布以产生颗粒核心。这种机制被认为是造粒过程中的一个重要阶段,然而,它很少被识别并与其他影响(如聚结和磨损)分开。
在成核区有两个重要的过程。第一阶段是成核,它是润湿热力学和动力学的函数。第二阶段是粘合剂在粉末混合物中的分散,以确保粉末和粘合剂的有效混合,这是工艺变量的函数。选择粉末和粘合剂的不良组合(例如,高接触角)或使用低效的粘合剂分散方法(例如,高液体流速或差的喷雾特性)会产生难以控制和复制的产品。
b.固结和增长(Consolidation and Growth)
在这个阶段,两个颗粒,颗粒和辅料粉末,或一个颗粒和设备之间的碰撞导致颗粒的压实和增长。每当造粒机中的物料碰撞并粘在一起时,就会发生颗粒生长。对于两个大颗粒,这个过程传统上被称为聚结(coalescence),而将细材料粘附到大的预先存在的颗粒表面上通常被称为成层(layering)。
这些生长过程可以在将液体添加到搅拌的粉末中时开始(即与润湿和成核阶段同时),并且可以在液体添加完成后继续进行。两个颗粒之间的碰撞是否会导致永久性聚结取决于多种因素,包括颗粒的机械性能和颗粒表面或附近的液体粘合剂的可用性。
c.破损和磨损(Attrition and Breakage)
在这个阶段,湿的或干燥的颗粒由于在造粒机中或在随后的产品处理过程中的冲击、剪切或压实而破碎。湿颗粒的破碎会影响最终的颗粒尺寸分布,尤其是在高剪切制粒机中。在某些情况下,破损会限制最大颗粒尺寸或有助于分散粘性粘合剂。另一方面,干颗粒的磨损导致产生粉尘状细粒。
从理论上去理解湿法制粒的机理,可以更好的解释小试阶段润湿剂以水柱般或者滴加加入与中式甚至商业化阶段润湿剂以雾化形式加入颗粒形成机理的差异,以雾化液滴加入,nuclei的大小由液滴大小控制,每一个液滴形成一个nuclei;当溶液以倾倒的方式加入时,瞬间形成的松散的湿料团,在剪切力作用下,被打散为小颗粒,形成nuclei。这仅仅是一个对于湿法制粒机理的一个解释,更多的内容与应用需要深入挖掘,这不是本文的重点。
湿法制粒主要有三种方式:高速剪切制粒,低速剪切制粒和流化制粒,最常用为高速剪切制粒。高速剪切混合制粒技术是由搅拌桨使物料有规律地立体运动,同时经高速旋转的剪切刀多次切割,从而形成细密、均匀、圆整的颗粒。高剪切湿法制粒是目前制粒工艺中最常用的方法,与其他制粒技术相比,其工艺易于放大,颗粒易混合均一。为便于粒径生长,高剪切湿法制粒的载药量≤50%。
但是,与粉末直压/直灌,干法制粒相比,湿法制粒所涉及的步骤更多,且引入了润湿剂(水或者乙醇,丙酮等有机溶剂),这种工艺一般需要添加大量的水,例如20~50%。湿法制粒后,制备的软材需要干燥,这样有带来了热,湿热的引入带来了诸多的物理化学不稳定性。虽然水分在干燥过程中可以除去,但是这个生产过程仍旧带来了巨大的风险,特别对于水敏感的药物。
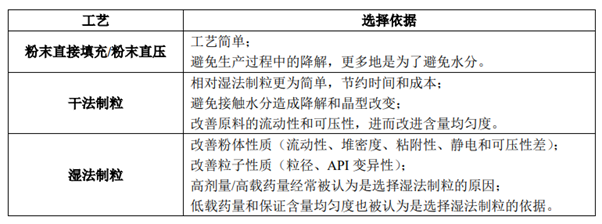
表1工艺选择的原因(参考文献4)
小结:固体剂型开发仍旧是目前医药工业中主流的药物载体,固体剂型的最终实现离不开制剂稳健的制剂工艺,包括粉末直压/直灌,干法制粒,湿法制粒以及其他。如果把制剂开发比作一场大战,如何合适的制定战斗的战略与战术决定着最终谁能获得胜利。老祖宗的古老智慧告诉我们:知己知彼,百战不殆。就像是我们需要开发一固体制剂,清楚的知道我们API的相关的性质以及所掌握的工艺技术,并把API的性质及可选的工艺进行配对,这是“知己”,知道自己所掌握,了解自己的任务目标,科学进行分析,最终在实施中完善,在完善中逐步成长。以上小文,以告大家!如有不妥,还请告知!
相关阅读:
参考文献:
1.基于原料药性质的口服固体制剂生产工艺路线选择
2.干法制粒技术的试验与数值研究
3. Handbook of Pharmaceutical Wet Granulation Theory and Practice in a Quality by Design Paradigm (2018)
4.基于原料药性质的口服固体制剂生产工艺路线:欧盟审评报告的分析
5. Practical application of roller compaction process modeling
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论