
湿法测定:系指选择适宜的分散方法使供试品分散成稳定的混悬液,通常可采用物理分散方法如超声、搅拌等,通过调节超声频率、时间和搅拌速度,必要时可加入适量的化学分散剂或表面活性剂,使分散体系成稳定状态,均匀稳定的通过检测窗口,以得到准确测定结果[1]。
混悬液体取样要求:样品容器应能密闭、方便超声或二次取样等,常用的配制容器如西林瓶、容量瓶等。二次取样的取样器要求较准确可用移液管或移液枪,一般也可用滴管,对于混悬液体样品,在取样过程中必须保证样品的均一性,可一边搅拌一边取样,防止大颗粒聚集在容器底部。
光学参数要求:颗粒大小和散射光强之间的关系常用米氏理论阐述,应用米氏理论常需要引入三个光学参数,分别是分散介质的折射率,样品物质的折射率,样品物质的吸收率,其中样品物质的折射率及吸收率与干法测定的要求相同,绝大多数原料都可以通过查找资料获得数据,必要时可进行考察,湿法测定值得注意的是分散介质的折射率,分散介质往往不是一种纯物质,必要时可加入适量化学分散剂或表面活性剂,折射率可采用主要背景介质的折射率,必要时可进行考察。
残差:与干法测定(《浅析原料药粒度分析方法开发思路(干法篇)》)相同,湿法测定的数据拟合同样用残差值来判断。残差可以帮助评估参数拟合的情况,即实际测量结果与理论计算是否一致。数据拟合一般被应用作判断光学参数是否合适的依据,但最好的数据拟合并不总是意味着正确的测量结果。
残差是理论光强数据与实际测量所得光强数据的最小二乘拟合差值,通常小的残差意味着测量结果准确可靠。在粒度分布正确的前提下,残差越低越好。
分散介质的要求:选择原料在其中能几乎不溶且充分分散的溶剂,或者采用原料药的饱和溶液作分散介质,可以保证原料药均匀分散。根据物料的溶解度,加入过量的待测物,保证溶液达到饱和,同时应保证溶液的制备和测定过程温度的基本一致,避免产生过饱和溶液。样品加入分散介质后,观察原料颗粒间是否聚集,是否吸附,必要时可以加入表面活性剂如卵磷脂、十二烷基硫酸钠等。
分散方法的要求:通常可采用物理分散方法如超声、搅拌等,使聚集颗粒可以充分分散。值得注意的是,超声可以使聚集的颗粒分散开,但是也可以使原始颗粒破裂,使粒径测定结果偏小,因此需考察是否需要超声,并考察超声时间和超声频率,通过测定结果判定并选择能充分分散原料的超声时间与频率。
背景测定:数据就是由被测量样品生成的散射光强,质量好的数据需要洁净、稳定的背景,在数据图上直观的显示就是散射光强随着检测器序号的增加递减,在第一号检测器的光强不超过100,背景随时间波动较小,随着检测器序号的增加,散射光强逐渐递减。
样品量:样品量通过加入样品后的遮光度变化来反映,与加入分散样品的体积和浓度有关。①如果样品颗粒较精细,较低的遮光度更合适,大约5-10%的遮光度就可以有很好的信噪比;②若样品的颗粒较粗,遮光度可以适当提高到5-12%;③若样品颗粒粒径分布较广,为了实现正确取样,15-20%较合适;④遮光度过高可能会导致多重散射。
湿法测定案例:
某原料B,可选择湿法进行粒度测定,湿法测定的前提是有合适的分散介质对其进行分散,分散介质是保证分散均匀的关键,在选择适宜的分散介质后对超声时间进行考察。通常选择能稳定分散样品的超声时间与超声频率搭配,频率不宜过高或过低,固定一个合适的频率,对超声时间的考察:根据物料的性质,观察物料在分散介质中随超声时间的变化状态,超声考察的时间从几秒到几分钟不等。
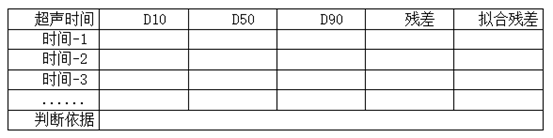
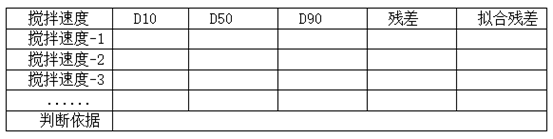
搅拌速度的考察:指进样装置内搅拌速度,控制合适的搅拌器循环速度可以避免大颗粒沉降,使不同粒径的样品均匀穿过检测池。可根据选择获得稳定粒度分布结果的搅拌速度。
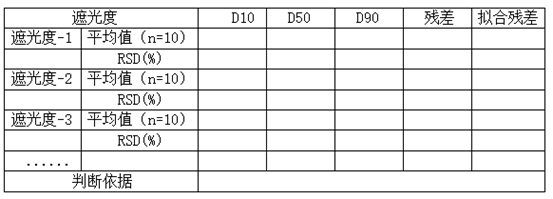
遮光度范围的考察:根据样品的粒度分布范围选择合理的遮光度范围,如不确定样品合适的加入量,可对遮光度范围进行考察,连续测定10次,取平均值,计算RSD%。
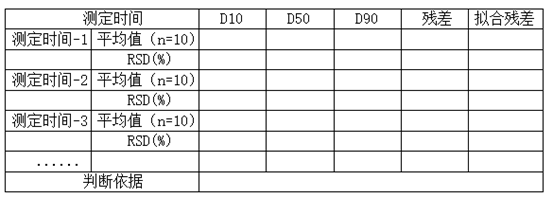
测定时间的考察:根据样品性质,选择关键参数进行考察,必要时对测定时间进行考察,连续测定10次,取平均值,计算RSD%。
方法验证:验证方法重复性,通常重复测定6个样品,取平均值,计算RSD%,应符合要求。
中间精密度:由另一名实验员重复测定6个样品,取平均值。与重复性的6次试验结果一起计算12次结果的RSD%,应符合要求。
如何提高湿法测定数据质量
样品分散:①关注样品的分散状况,确保样品良好分散,必要时可在显微镜下观察;②取样时确保样品均匀,取样应具有代表性。③超声分散的样品大多易再次聚集,样品可现配现测,避免二次聚集。
背景数据: ①确保样品池玻窗上没有物质黏附;②确保分散剂洁净无污染;③确保分散剂不存在温度梯度;④确保系统正确对光
参考资料
[1]中国药典2020年版四部通则0982粒度和粒度分布测定法
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论