非酒精性脂肪肝病(NAFLD)是一种常见但易被忽视的肝脏疾病,其病理表现类似酒精性肝病,但患者无过量饮酒史。NAFLD的疾病谱主要包括干脂肪变性(NAFL)和非酒精性脂肪肝(NASH)。其中,NASH为NAFLD的进展期,可向肝纤维化发展,甚至进展为肝硬化和干细胞癌(HCC)。NAFLD与胰岛素抵抗、高血压、血脂异常、肥胖等代谢疾病密切相关,故其发生会加剧糖尿病等代谢综合征的进程。
中国的NAFLD患病率在2008-2018年间快速增长,速度达西方国家的两倍。2030年,中国的患病人数预计将超3亿,医疗需求巨大。然而,由于NAFLD/NASH的发病机制较为复杂,相关治疗药物研发进展十分缓慢。
药融咨询《全球NAFLD/NASH治疗市场格局与研发进展深度洞察报告》,对这一领域的全球及中国药物研发动态进行了权威详尽的分析。报告揭示了NAFLD/NASH发病机制及主要治疗方法、治疗药物研发的最新趋势、关键靶点竞争格局以及市场前景预测等,为业界提供了极具价值的参考依据。本文基于报告部分内容,来分析NAFLD/NASH治疗领域全球及中国药物市场格局。
一、NAFLD/NASH新药上市进展
1. 首款获批药物:Saroglitazar
药融云数据库显示,2020年3月,ZydusCadila的PPARα/PPARγ双重激动剂-Saroglitazar获印度药物管理局批准,成为全球首个获批上市的NASH药物。此药目前在印度已获批了包括非酒精性脂肪肝病和非酒精性脂肪肝炎在内的共计5个适应症(2型糖尿病、高甘油三酯血症、糖尿病血脂异常)。但目前该药物未在美国,欧盟和日本等国家地区获批。
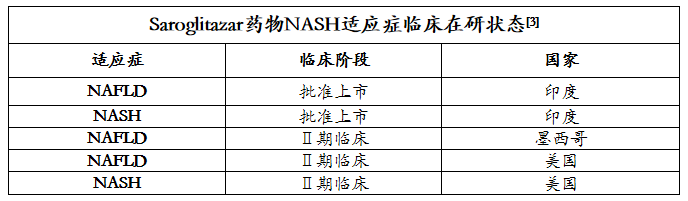
Saroglitazar是一款PPARα/PPARγ的双重激动剂,属于过氧化物酶体增殖物活化受体(PPAR)家族的两名成员,该靶点与脂肪代谢、氧化应激作用有关,已经多款用于治疗代谢性疾病的药物上市。
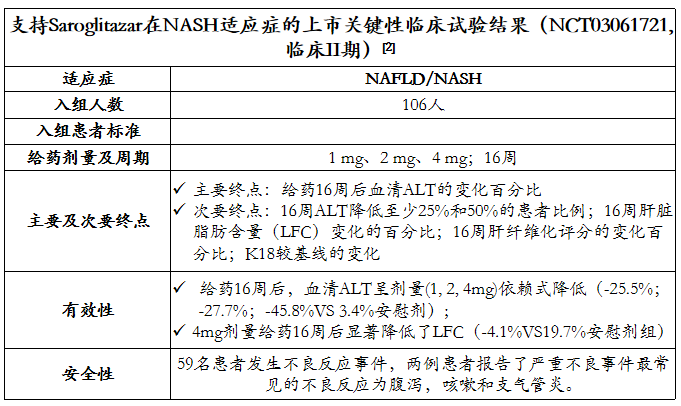
Saroglitazar的历年销售额

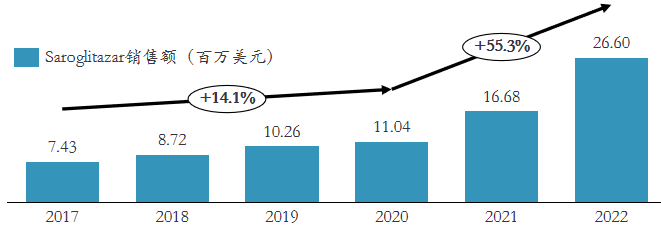
图片来源:《全球NAFLD/NASH治疗市场格局与研发进展深度洞察报告》
尽管患者群体庞大,然而截至2024年2月,全球仅一款药物saroglitazar(赛格列扎)在印度获得批准治疗NASH,FDA尚未批准任何NASH治疗药物上市,大量NASH患者面临无药可医的窘境。
2. 新药加速获批:Resmetirom
直到2024年3月,MadrigalPharmaceuticals开发的Resmetirom(商品名:Rezdiffra)获FDA加速批准上市,用于联合饮食和运动,治疗患有中重度肝纤维化(F2至F3期)的非肝硬化非酒精性脂肪性肝炎(NASH)成人患者(NASH,现称为代谢功能障碍相关脂肪性肝炎MASH),这是FDA批准的首个治疗NASH的创新药物,标志着该领域的一项重要里程碑。
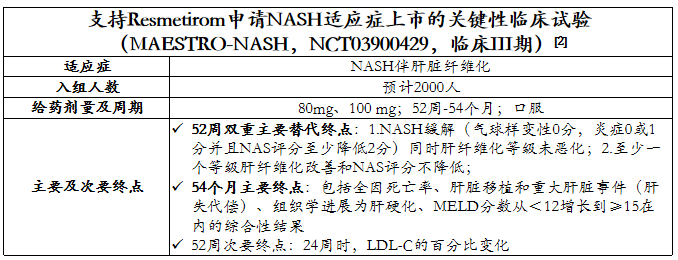
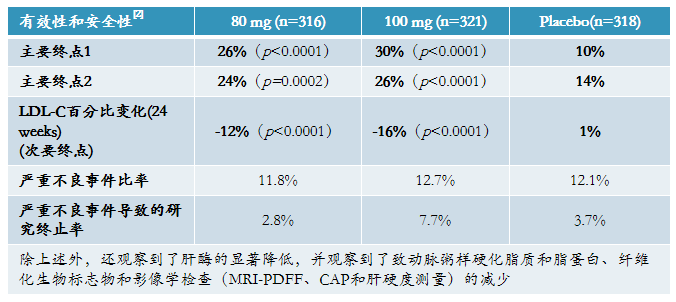
目前,Resmetirom(NASH适应症)在欧盟处于申请上市阶段;其次,其他适应症(代偿期肝硬化、NAFLD)在美国处于III期临床阶段。

二、NAFLD/NASH药物市场规模预测
由于目前NASH的药物治疗方案稀缺,以及其巨大的市场潜力,无疑注定了药企对于NASH药物研发的前仆后继。
1. 全球市场规模及预测
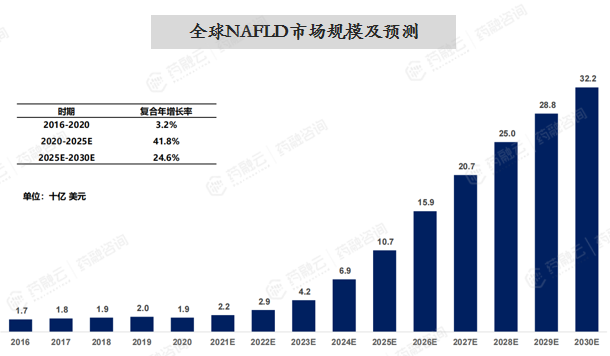
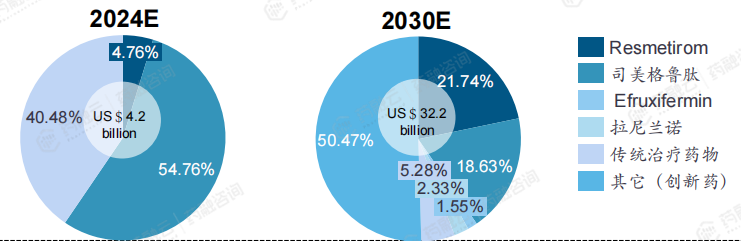
全球NASH市场从2016年的17亿美元增至2020年的19亿美元,复合年增长率为3.2%。预计未来会呈现快速增长的趋势,到2025年将达到107亿美元,并于2030年达到322亿美元,期间复合年增长率为41.8%和24.6%。
2. 中国市场规模及预测
国内NASH药物市场从2016年的5亿人民币增至2020年的7亿人民币,复合年增长率为5.5%。未来随着创新药走向大众化,会呈现明显的增长,到2025年预计NASH药物市场将达到32亿人民币,并于2030年达到355亿人民币,期间复合年增长率为37.0%和61.4%。
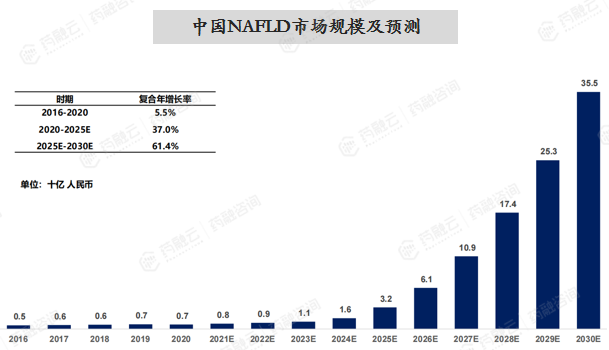

图片来源:《全球NAFLD/NASH治疗市场格局与研发进展深度洞察报告》
三、NAFLD/NASH患病人数增长与市场驱动因素
在肥胖、糖尿病等疾病因素的作用下,NAFLD/NASH患病人数持续上升。
1. 全球患病趋势
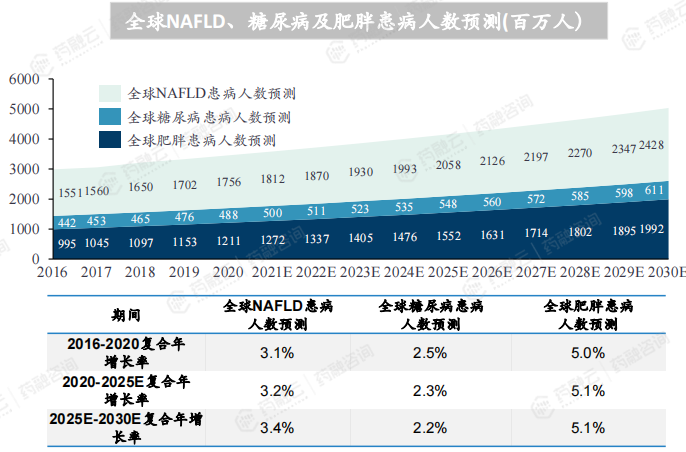
全球糖尿病患病人数从2016年的4.4亿人上升到2020年的4.9亿,复合年增长率为2.5%,全球糖尿病患病人数将在2025年接近5.5亿,并于2030年超过6亿;全球肥胖患病人数从2016年的10.0亿人上升到2020年的12.1亿,复合年增长率为5.0%,全球肥胖患病人数将在2025年接近15.5亿,并于2030年接近20亿;全球NAFLD患病人数从2016年的15.5亿人上升到2020年的17.6亿,复合年增长率为3.1%;在肥胖、糖尿病等疾病因素的作用下,2021-2030年,全球NAFLD患病人数将以稳定的速度持续增长,2030年将达到24.3亿人。
2. 中国患病趋势
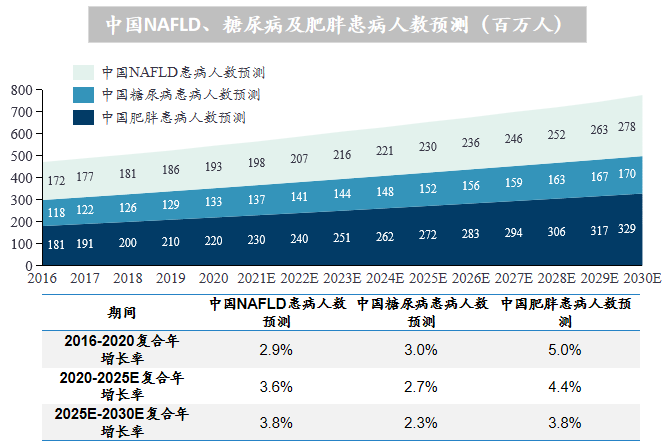
中国糖尿病患病人数从2016年的1.2亿人上升到2020年的1.3亿,复合年增长率为3.0%,中国糖尿病患病人数将在2025年接近1.5亿,并于2030年超过1.7亿;中国肥胖患病人数从2016年的1.8亿人上升到2020年的2.2亿,复合年增长率为5.0%,中国肥胖患病人数将在2025年接近2.7亿,并于2030年超过3亿;中国NAFLD患病人数从2016年的1.7亿人上升到2020年的2.0亿,年复合增长率为2.9%;在肥胖、糖尿病等疾病因素的作用下,2021-2030年,中国NAFLD患病率会以更快的速度增长,将于2030年达到2.8亿人。

四、NAFLD/NASH药物开发趋势
1. NASH在研管线进展
据药融云数据库统计,目前全球有超过500个NASH新药项目在研,超过200个处于临床开发阶段。从国外来看,吉利德、礼来、诺和诺德、Intercept、艾尔建等多家企业均加紧布局NASH 新药的研发。在国内,近两年内中国生物/正大天晴、歌礼制药、众生药业、石药集团、信达生物、瑞博生物等企业频繁更新NASH药物动态,助力该领域进一步发展。
预计未来10-15年内,将有10余种NASH药物获批。其中,进展最快的THR-β激动剂Resmetirom2024年3月14日获FDA加速批准上市。
FGF21类似物Efruxifermin改善NASH患者肝脏纤维化水平为对照组2倍,并且显著改善NAS评分,具有同类最优(Best-in-class)潜力,FDA已授予其突破性疗法资格认定(临床Ⅱ期)。目前,Efruxifermin已进入III期临床。
中国生物制药/正大天晴在NASH布局的靶点最多,涵盖全球进展最快的主要靶点;通过合作引进方式,在PPAR 及FGF-21 两个靶点的产品正在开展临床试验,其他靶点产品仍处于临床1 期或临床前。其引进的PPAR激动剂拉尼兰诺(Lanifibranor)为首个同时能改善纤维化和炎症的口服NASH新药,美国FDA已授予该药用于NASH的突破性疗法认定和快速通道资格(临床Ⅲ期)。
歌礼制药则主要布局FASN抑制剂、THR-β激动剂,上述靶点药物(ASC40、ASC41)均已推进至临床2期。众生药业的PDE抑制剂ZSP1601,已经进入临床2b期,是国内首个获批临床用于治疗NASH的1类口服小分子创新药。
通过药融云数据库可实时追踪ZSP1601审评动态
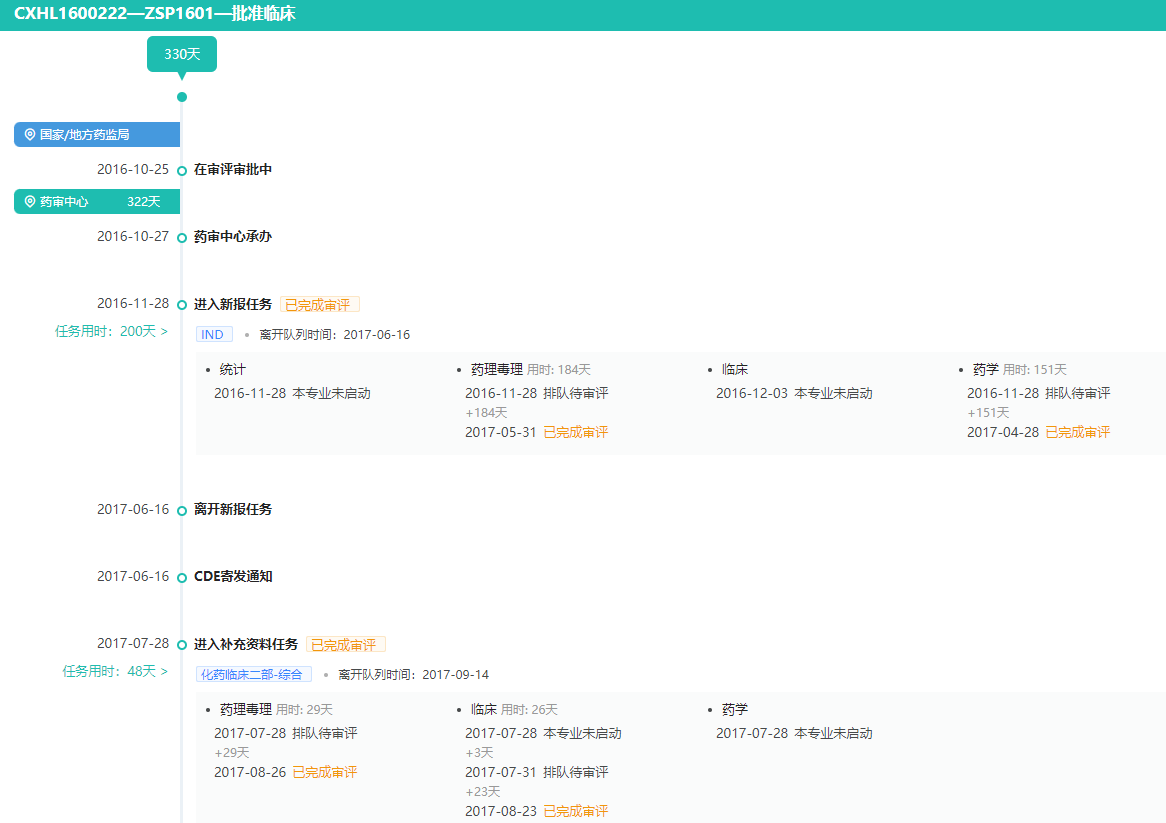
图片来源:药融云中国药品审评数据库
2. 联合疗法探索
联合疗法或为NASH治疗带来新希望。由于NASH是一种机制复杂、多风险因素的慢性进行性疾病,业内认为单药治疗并不是唯一的途径,理论上讲,如果几个机理互补的药物联合使用,就更有可能提高有效率和患者依从性,同时还可能降低副作用。因此,联合疗法成为关注NASH的企业在不断探索的路径之一。目前最具前景的疗法是将FXR激动剂与GLP-1R激动剂、THR-β激动剂联用。
3. 非侵入诊断技术推动
NASH非侵入诊断方式推动药物开发。长期以来,在NASH临床试验中,需要通过肝活检来筛选受试者和作为疗效终点。但由于其高侵入性,存在着患者依从性较低的问题。由于肝活检的局限性,目前已经开发出一些非侵入性诊断方式,以影像学为主。如FibroScan评估肝脏脂肪变性和纤维化,MRI-PDFF对肝脏脂肪进行定量,ARFI利用超声波监测肝脏纤维化程度。其中,MRI-PDFF或可用于2a期研究的主要终点。
结语:
NAFLD/NASH的发病作用机制复杂,与多种并发症具有密切联系,因此,相关治疗药物研发进展缓慢,仅有2款上市药物上市,且副作用较为明显。NAFLD/NASH患病率的逐步提高催生了巨大的市场空间,许多企业正在加速布局这一领域。随着新药研发的不断推进、治疗策略的创新探索以及诊断技术的革新应用,未来将在疾病防控、患者管理以及市场满足等方面取得更为显著的成果,为NAFLD/NASH患者带来更为有效的治疗方案和更高的生活质量。
扩展阅读:
1.2024年NAFLD/NASH概览及背景介绍:定义、患病率、病理进程及发展趋势
2.2024年NAFLD/NASH的发病机制与主要治疗方法探析
3.2024年NAFLD/NASH治疗领域新药全球及中国药物研发格局
4.2024年NAFLD/NASH药物研发:热门靶点、在研产品与临床进展深度解读
以上内容均来自{NAFLD/NASH治疗领域市场和研发格局分析报告},如需查看或下载报告,可点击!
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论