导读:
- CDE一致性评价承办受理号达2943个,本周新增19个
- 本周40个品规通过一致性评价,涉及26个品种
- NMPA发布三批药品批件通知,4款药品首过评
- 企业通过概况,正大天晴、齐鲁、上药…添新品
第五批集采来袭,4款药品新增过评企业
CDE一致性评价承办受理号达2943个,
本周新增19个
截止2021年05月13日,CDE共承办一致性受理号2943个(689家企业的605个品种);其中1348个受理号(348个品种)通过一致性评价。本周(2021.05.07-2021.05.13)新承办19个受理号,包括14个品种,10款注射剂。(不含视同通过)
图1:本周CDE一致性评价承办一览
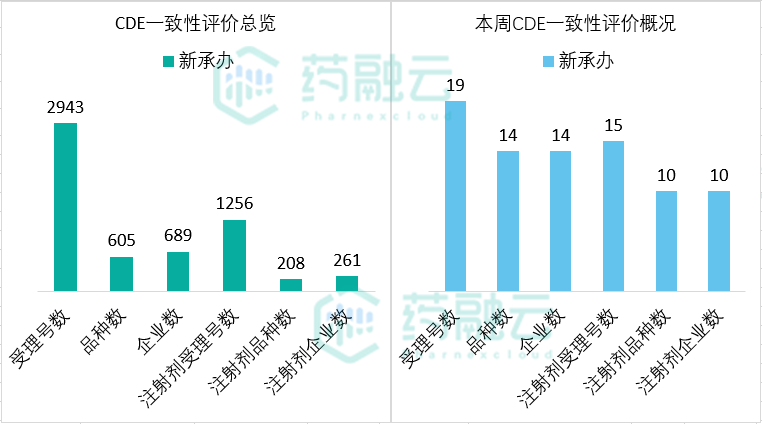
数据来源:药融云中国药品审评数据库
本周40个品规通过一致性评价,
涉及26个品种
根据药融云数据库显示,截止2021年05月13日,全国共2413个品规过评,涉及548个品种。随着大批通过一致性评价的药品批件信息的发布,一致性品规过评数不断攀升,本周(5月07- 13日)发布三批通知件,其中包括多个通过(含视同通过)一致性的药品。本周新增40个品规(26个品种)通过或视同通过一致性评价,包括8个注射剂品种,具体如下表:
表1:本周通过一致性评价情况汇总表
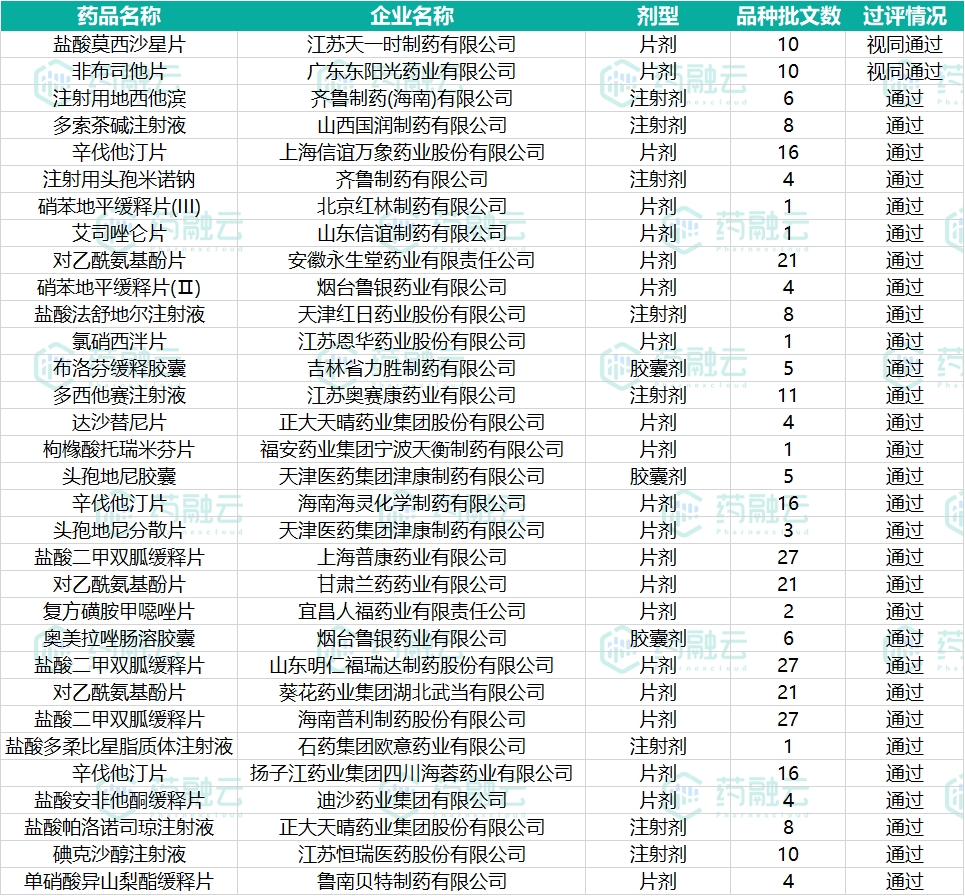
数据来源:药融云一致性评价数据库
注:图为各企业通过药品品种
NMPA发布三批药品批件通知,
4款药品首过评
本周,国家药监局发布的三批药品批准证明文件待领取信息分别是5月7日、10日、12日,其中包括多款通过一致性评价和视同通过一致性评价的药品批件信息。
表2:NMPA发布药品批件通知一览表
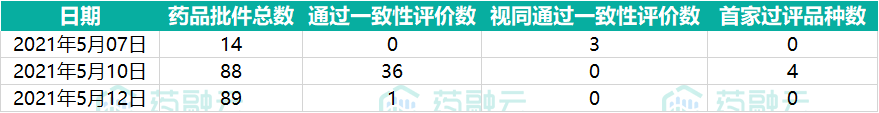
数据来源:药融云中国药品审评数据库
药融云一致性评价数据库
在本周通过的一致性药品中,包含4款药品为首家通过,具体如下表:
表3:本周首家通过一致性评价品种
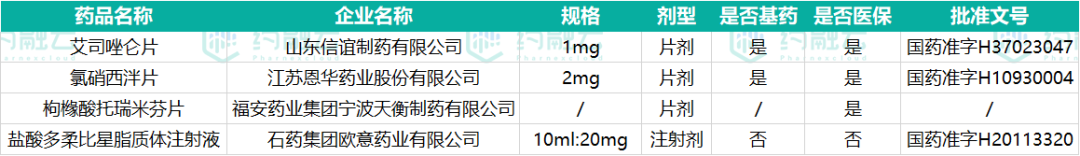
数据来源:药融云一致性评价数据库
注:表中的首家过评以品种计
企业通过概况,
正大天晴、齐鲁、上药…添新品
在通过一致性评价的40个药品品规中,涉及到27家企业。根据药融云一致性评价数据库统计,本周通过一致性评价数企业概况如下表。正大天晴药业通过一致性评价的品规数最多,达4个,有达沙替尼片和盐酸帕洛诺司琼注射液;紧随其后的是齐鲁制药、上药集团和海南海灵化学制药等。
表3:本周企业通过数量概况表
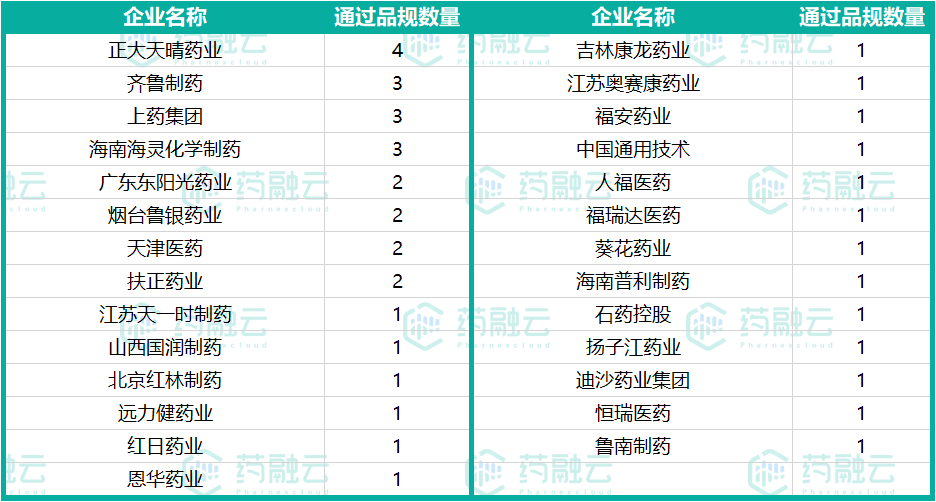
数据来源:药融云一致性评价数据库
第五批集采来袭,
4款药品新增过评企业
5月8日,上海阳光医药采购网发布《关于开展第五批国家组织药品集中采购相关药品信息收集工作的通知》,涉及202品规。文件中指出,自2021年5月10日起,联合采购办公室开展第五批国家组织药品集中采购相关信息申报工作。并公布了在此处申报范围内的药品品规名单。
根据药融云一致性评价数据库统计,本周通过一致性评价的药品品种中,包括4款第五批国家集采申报范围内的药品:齐鲁制药(海南)的注射用地西他滨、江苏奥赛康药业的多西他赛注射液、江苏恒瑞医药的碘克沙醇注射液和鲁南贝特制药的单硝酸异山梨酯缓释片。根据药融云一致性评价数据库统计,第五批国家集采申报范围内的药品通过一致性评价厂家数具体情况如下表:
表4:第五批国家集采申报范围内品种
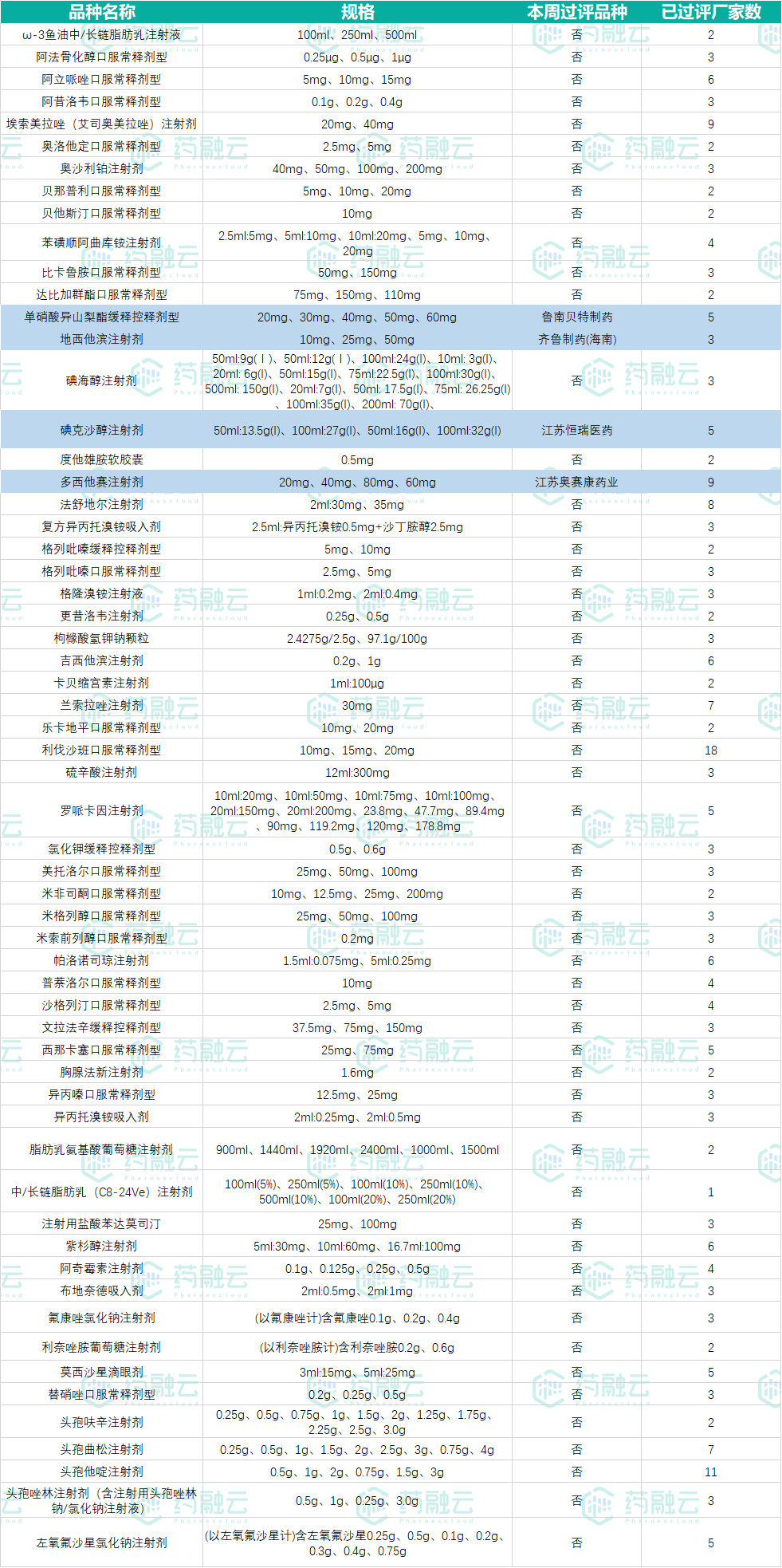
数据来源:药融云一致性评价数据库


































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论