
药融圈旗下药融云数据监测显示:2023年12月6日,诺华制药(Novartis)的Fabhalta® (Iptacopan)(研发代码:LNP023)获美国FDA批准上市,作为治疗成人阵发性夜间血红蛋白尿症(PNH,paroxysmal nocturnal hemoglobinuria)的首个口服单药疗法。
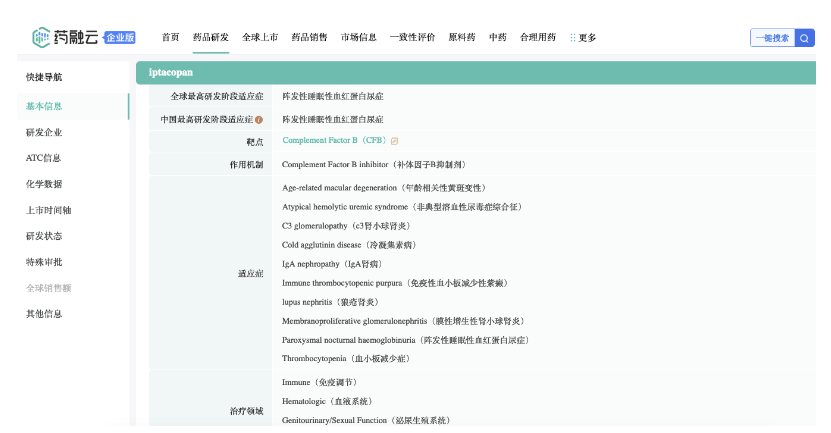
截图来源:药融云全球药物研发数据库
Iptacopan/Fabhalta®是一种补体B因子抑制剂,作用于免疫系统的补体旁路途径中的近端通路,可全面控制血管内外的红细胞(RBC)破坏(血管内和血管外溶血[IVH和EVH])。
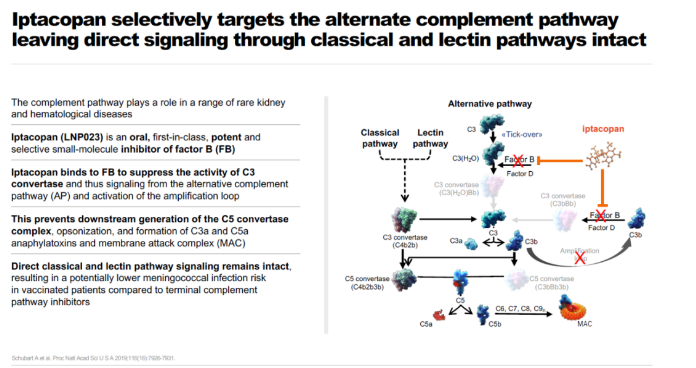
在临床试验中,大多数接受Fabhalta治疗的患者提高了血红蛋白水平(在没有RBC输注的情况下,血红蛋白水平与基线相比提高≥2g/dL),并且几乎所有接受Iptacopan治疗的患者未接受输血。
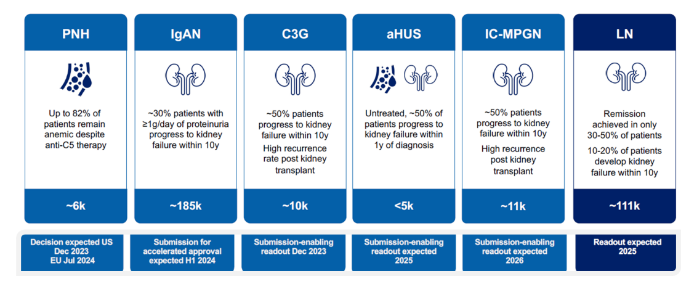
此外,Iptacopan目前也处于其他许多补体介导疾病的研究阶段,包括免疫球蛋白A肾病(IgAN)、C3肾小球疾病(C3G)、免疫复合物膜增殖性肾小球肾炎(IC-MPGN)和非典型溶血性尿毒症综合征(aHUS)。相关化合物专利,WO-2015009616。
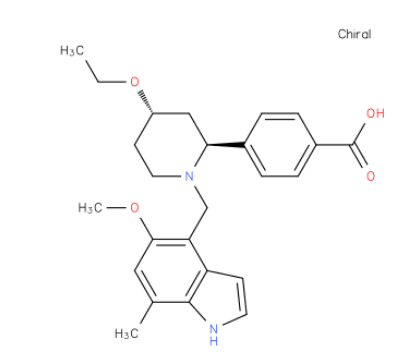
▲ 化合物结构
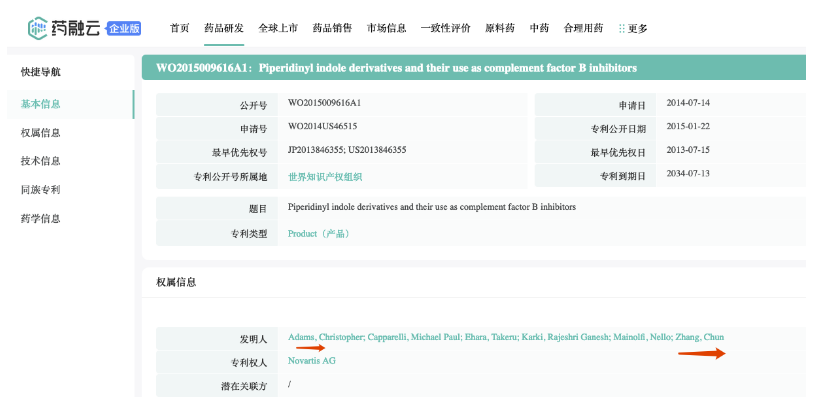
▲ 化合物发明人同样也有华人科学家身影
美国FDA的首次批准基于3期临床试验(APPLY-PNH)。该临床试验纳入血红蛋白<10 g/dL且此前接受过抗C5补体疗法治疗但仍有残余贫血的患者。结果显示,Fabhalta在提高血红蛋白水平和避免输血方面优于继续使用抗C5疗法治疗的患者。批准还依靠3期临床试验APPOINT-PNH的数据支持,该研究针对未接受过补体抑制剂治疗的患者。APPLY-PNH和APPOINT-PNH试验24周的主要发现包括:
82.3%接受过抗C5疗法治疗的患者在无输血的情况下,接受Fabhalta治疗后血红蛋白水平持续增加≥2 g/dL,继续接受抗C5疗法治疗的患者这一数值为0%(P<0.0001)。未接受过补体抑制剂治疗的患者中,77.5%的患者接受Fabhalta治疗后达到了这一结果。
在无输血的情况下,67.7%接受过抗C5疗法治疗的患者血红蛋白水平持续≥12 g/dL,继续接受抗C5疗法治疗的患者这一数值为0%(P<0.0001)。
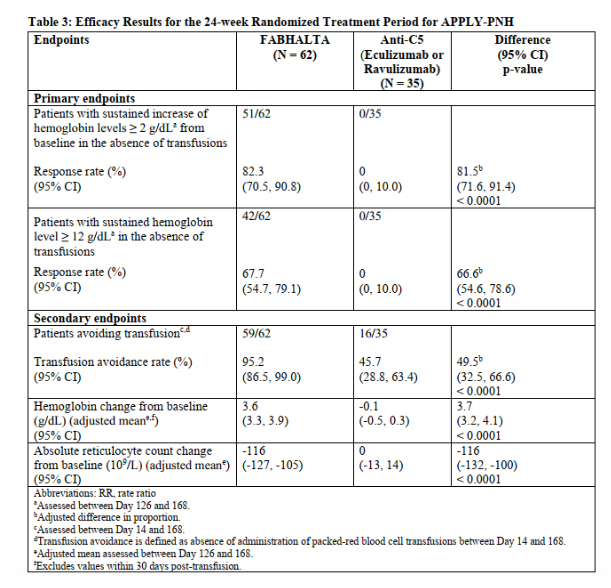
对于接受过抗C5疗法治疗的患者,接受Fabhalta治疗后避免输血率为95.2%,而抗C5疗法组患者这一数值为45.7%(P<0.0001)。
PNH(paroxysmal nocturnal hemoglobinuria)患者具有一种获得性突变,使得红细胞容易被补体系统过早破坏。PNH的特征是溶血、骨髓衰竭和血栓形成,其组合和严重程度各不相同。现有的C5抑制剂治疗以输注的方式给药,并且可能无法控制PNH症状。高达88%的抗C5治疗患者可能患有持续性贫血,其中超过三分之一的患者每年至少需要输血一次。Iptacopan/Fabhalta®预计就在12月推向美国市场。
在中国,Iptacopan(LNP023)伊普可泮胶囊的新药上市申请已经被纳入纳入优先审评程序。
参考来源:
NMPA/CDE;
药融云数据库;
FDA/EMA/PMDA;
相关公司公开披露等等。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论