
01研究概述
随着全球肿瘤治疗费用的逐年攀升,如何降低患者用药负担、提高药品可及性成为摆在各国面前的重大课题。近年来,生物类似药凭借其与原研药在质量、安全性和有效性上的高度相似性,以及相对更低的价格,成为了市场的新宠。而在中国,这一趋势更是愈发明显。
近日,清华大学药学院杨悦课题组在权威期刊《JAMA Network Open》上发表了一项重要研究,肿瘤生物类似药相比于参照药物的临床获益、价格和市场替代的评价分析》(Clinical Benefit, Price, and Uptake for Cancer Biosimilars vs Reference Drugs in China:A Systematic Review and Meta-Analysis)。该研究系统评价分析了中国肿瘤生物类似药与参照药物在临床获益、价格和市场替代方面的差异。

截图来源:JAMA Network Open
本文文中涉及价格、销售额及市场替代率等部分的数据引自药融云数据库,在顶级期刊成功发表,为行业提供了有力支撑。

02图文导读
自2015年审评审批改革以来,我国已批准超200个新分子实体药物,显著提升患者用药可及性,其中生物制品占近三分之一。面对日益增长的医疗负担,NMPA发布多项生物类似药研发评价指导原则,推动其发展。至2023年2月,我国已批准超20款单抗类生物类似药上市,包括多款肿瘤生物类似药,有望减轻患者经济压力。
至2023年2月中国获批上市的单抗类生物类似药品种表
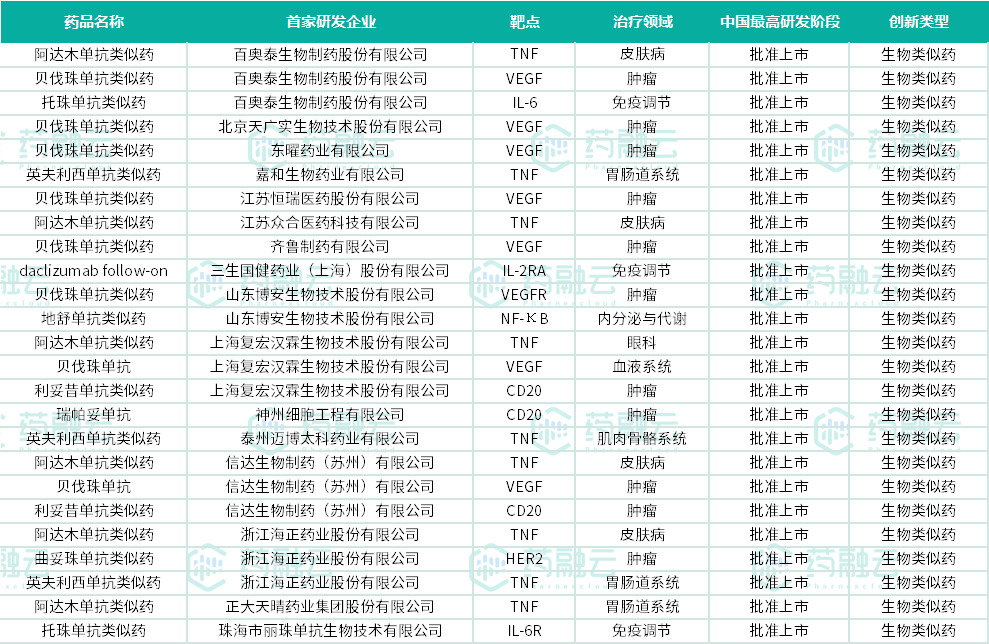
数据来源:药融云全球药物研发数据库
由于生物类似药具有分子量大、空间结构和理化性质复杂、异质性大等特点,在实际诊疗中,有不少医生和患者对其临床获益(安全性和有效性)是否与原研药等效持有怀疑态度,这也直接影响到生物类似药在全球各国的替代成效。因此,本研究基于已发表的随机对照临床试验以及真实诊疗环境下的队列研究对肿瘤生物类似药的临床获益进行定量评估(时间截止至2023年2月),并结合我国的生物类似药价格和销量的变化,为我国及全球肿瘤生物类似药的替代与合理使用提供证据支持。
该研究共纳入39项RCT和10项队列研究,包含了FDA批准的12款肿瘤生物类似药、EMA批准的16款肿瘤生物类似药、PMDA批准的9款肿瘤生物类似药和NMPA批准的11款肿瘤生物类似药。研究结果显示肿瘤生物类似药在有效性、安全性和免疫原性方面与原研药无显著差异。与FDA、EMA、PMDA相比,我国已经建立严格的肿瘤生物类似药审评制度,生物类似药的临床试验包括纳入的患者人数、试验设计、试验质量等方面,均达到了国际标准。在价格和市场替代率方面,该研究显示2015年-2022年肿瘤生物类似药及其参照药物的加权平均价格中位数。肿瘤生物药类似药的价格在2017年后出现显著下降。(详见图1以及补充表14)
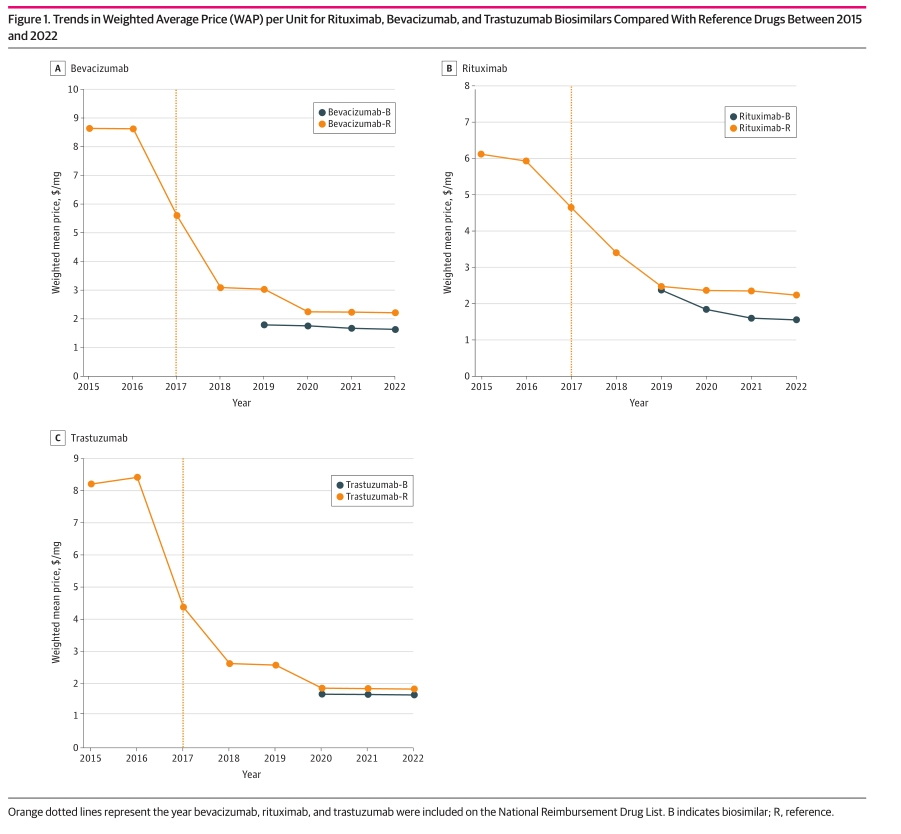
图1:2015年-2022年利安昔单抗、贝伐单抗和曲妥珠单抗生物类似药与参比药物的单位加权平均价格趋势。
表14:2015年-2022年利安昔单抗、贝伐单抗、曲要珠单抗及其生物类似药的单位加权平均价格
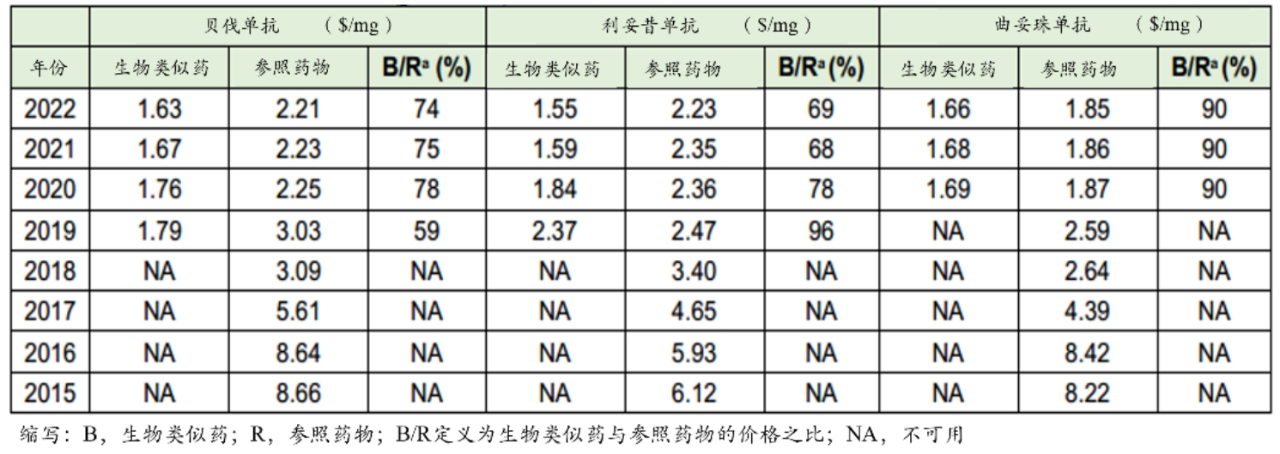
图片数据来源:整合药融云数据库
2022年,贝伐单抗生物类似药的加权平均价格中位数约为参照药物的74%,而利妥昔单抗生物类似药为69%,曲妥珠单抗生物类似药为90%。肿瘤生物类似药的市场替代率随时间呈上升趋势(详见图2及补充表15)。
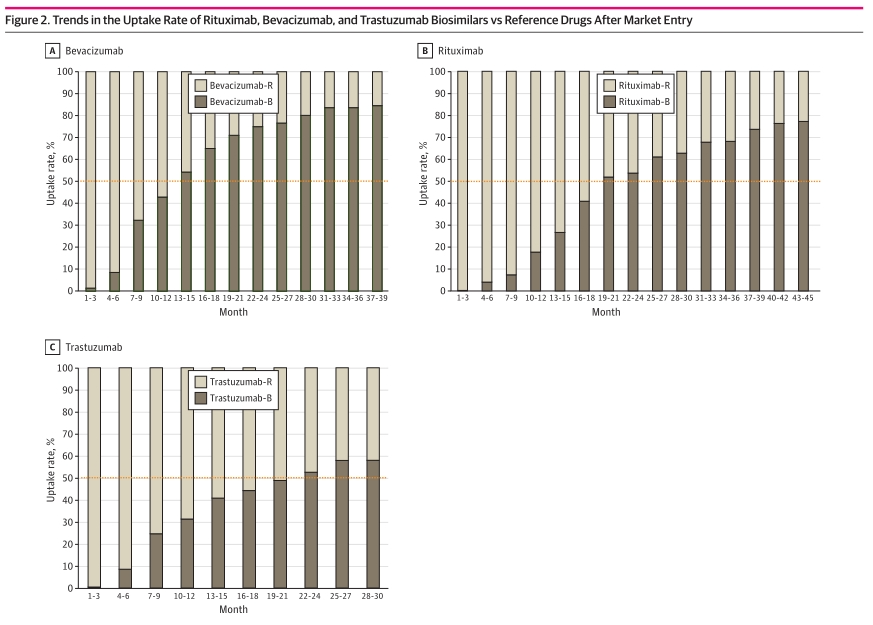
图2:利安普单抗、贝伐单抗和曲要珠单抗生物类似药与参比药物的市场替代率趋势
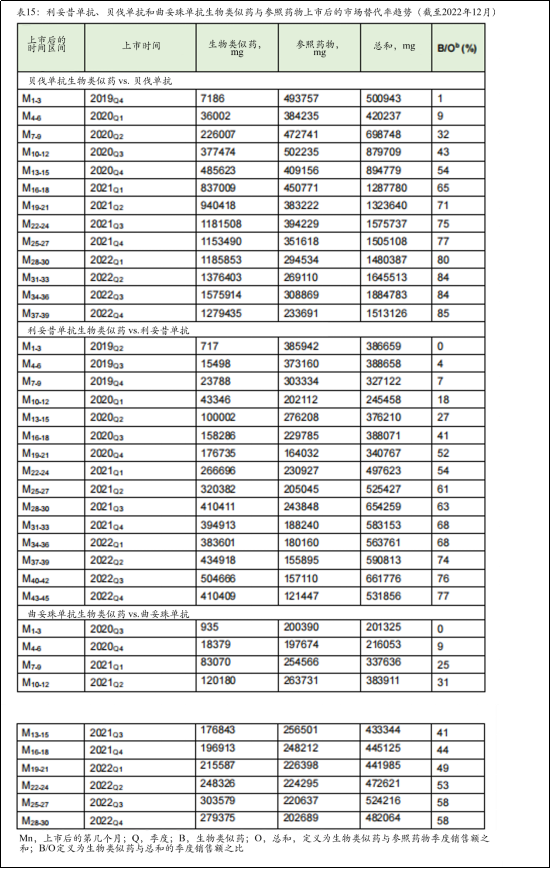
3种肿瘤生物类似药在上市后第一年、第二年以及2022年市场替代率。这3种肿瘤生物类似药的市场替代率在上市后第一年及第二年有显著差异(详见补充表16)。
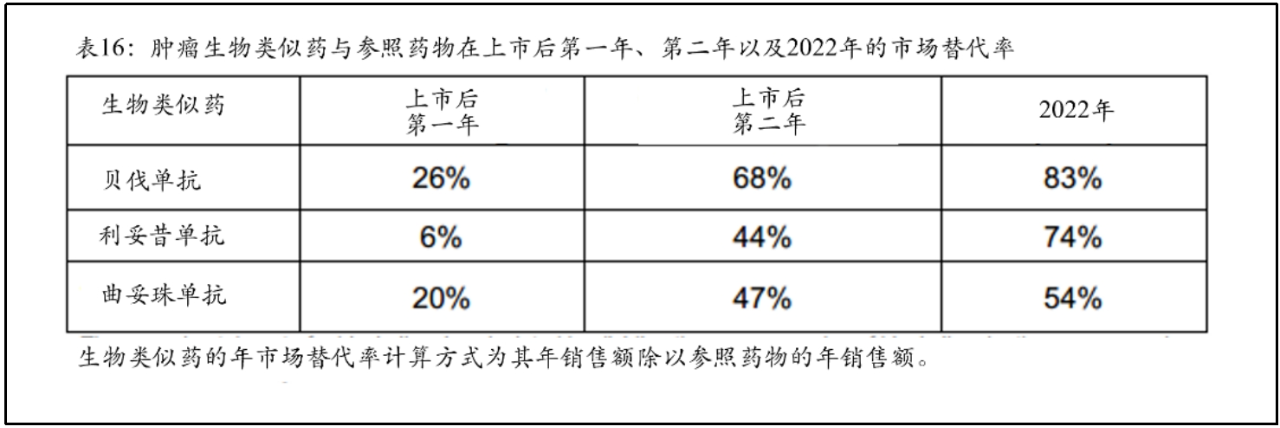
贝伐单抗生物类似药在上市后的第一年和第二年的市场替代率最高(分别为26%和68%),其次是曲妥珠单抗生物类似药(20%和47%)和利妥昔单抗生物类似药(6%和44%)。2022年,贝伐单抗、利妥昔单抗和曲妥珠单抗生物类似药的市场替代率分别为83%、74%和54%。
肿瘤生物类似药的价格是一个全球性问题,因为它直接影响到患者用药负担以及公共卫生支出。通常,生物类似药价格为原研药的70%-85%,而仿制药的价格可能仅为原研药的20%。该研究团队的研究结果表明,在中国,肿瘤生物类似药的价格相比于参照药物价格有不同程度的下降。2022年,利妥昔单抗生物类似药相比于参照药物的价格最低(为69%),其次是贝伐单抗生物类似药(74%)和曲妥珠单抗生物类似药(90%),这和其他国家的情况类似。
从全球范围来看,欧洲肿瘤生物类似药的价格通常折扣率为30%,美国为10% - 33%,日本为30%。按目前的情况,生物类似药及其参照药物的医保报销政策是相同的。有趣的是,2022年曲妥珠单抗生物类似药的降价幅度最小(为参照药物价格的90%),利妥昔单抗生物类似药(69%),贝伐单抗生物类似药(74%),可能因为只有曲妥珠单抗生物类似药在中国获批。
结语
综上所述,中国肿瘤生物类似药市场正处于一个蓬勃发展的阶段。价格的大幅下降和市场替代率的飙升,使得更多患者能够享受到高质量、低成本的肿瘤治疗服务。同时,严格的审评制度和临床获益的无显著差异,也为生物类似药的市场地位提供了有力支撑。未来,我们期待看到更多优秀的生物类似药涌现,为肿瘤患者带来更好的治疗选择和希望。
参考来源:
Luo X, Du X, Li Z, et al. Clinical Benefit, Price, and Uptake for Cancer Biosimilars vs Reference Drugs in China: A Systematic Review and Meta-Analysis[J]. JAMA Network Open, 2023, 6(10): e2337348-e2337348.
推荐阅读:
2.中国生物类似药集中“爆发” 两年内7款获批 正迈向国际化发展
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论