导读:
与常见的生物科技型企业不同,四川百利天恒药业股份有限公司(以下简称百利天恒)以化学仿制药和中成药起步,经过 25 年的发展,已建立了完整的制药企业研产供销体系,有着较为稳定的收入。形成了化药制剂与中成药制剂业务板块和创新生物药业务板块。
2011 年,百利天恒开始布局全球创新生物药领域,基于免疫学的最新科学进展,致力于研发具有突破性疗效、具备全球专利和权益的创新大分子生物药。截至本招股说明书签署日,百利天恒拥有全球权益的核心创新生物药在研品种 16 个,其中双特异性抗体候选药物 SI-B001 已陆续开展 6 个 II 期临床试验,另有 6 个候选药物处于 I 期临床研究阶段。

创始人:朱义博士

截图自:招股书
百利天恒业务构成
百利天恒以化学仿制药和中成药业务起步,经过 25 年的发展,已建立了完整的制药企业研产供销体系,形成了化药制剂与中成药制剂业务板块和创新生物药业务板块,并依靠化药制剂与中成药制剂业务板块为公司带来较为稳定的收入。截至本招股说明书签署日,公司主要销售品种有丙泊酚中/长链脂肪乳注射液、丙泊酚乳状注射液、盐酸右美托咪定注射液、中/长链脂肪乳注射液等多种化学仿制药,以及黄芪颗粒、柴黄颗粒等中成药制剂。报告期内,公司制剂业务的销售收入分别为 110,852.92 万元、120,450.50 万元、101,104.88 万元及 42,217.98 万元, 占公司主营业务收入的比例为 100%。
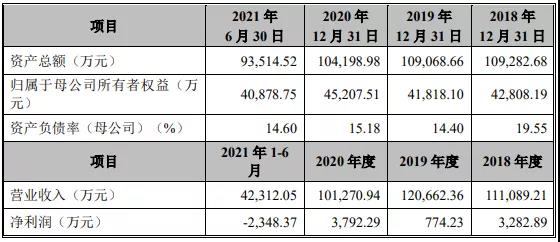
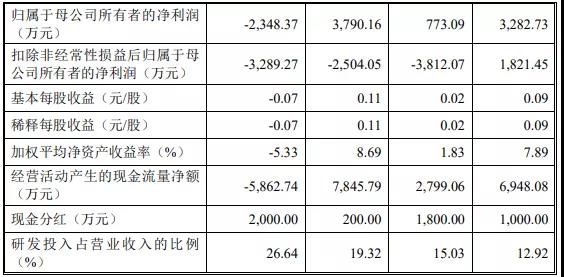
截图自:招股书
截至本招股说明书签署日,百利天恒重点化学药在研项目 26 个,其中 6 个处于申报上市阶段,6 个处于申报临床或临床研究阶段。公司的丙泊酚乳状注射液、中/长链脂肪乳注射液(C8-24)2 个品种 6 个规格已向 CDE 提交仿制药一致性评价申请,目前处于审批中。
2011 年,百利天恒开始布局全球创新生物药领域,基于免疫学的最新科学进展,致力于研发具有突破性疗效、具备全球专利和权益的创新大分子生物药。公司运用化药制剂与中成药制剂业务所产生的现金流支持和反哺于公司创新生物药的研发,以实现良性的内生发展正循环。经过 10 年的积累,公司创新生物药板块已经颇具规模,且有着具备全球竞争力的阶段性成果。截至本招股说明书签署日,百利天恒拥有全球权益的核心创新生物药在研品种 16 个,其中双特异性抗体候选药物 SI-B001 已陆续开展 6 个 II 期临床试验,另有 6 个候选药物处于 I 期临床研究阶段,但尚未产生销售收入。
百利药业研发机构以及生物创新药管线
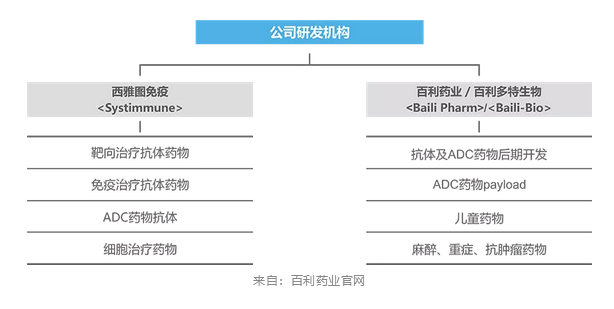
创新生物药相关的核心技术平台:
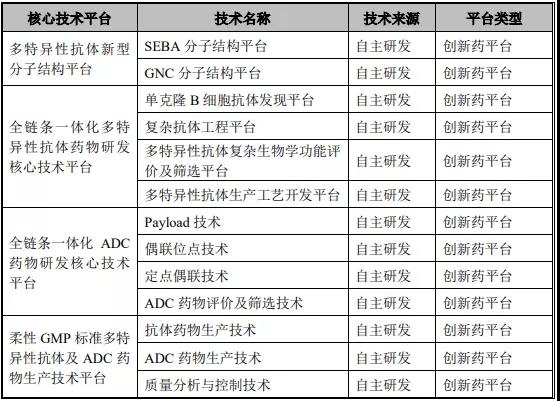
截图自:招股书
截至本招股说明书签署日,百利天恒已自主研发了 16 个创新生物药,其中 7 个 已进入临床研究阶段,9 个候选生物药已进入临床前药理、毒理等研究阶段。药物涵盖双/多特异性抗体、ADC 药物、融合蛋白等不同类型,聚焦于肿瘤治疗等 领域,用于治疗非小细胞肺癌、乳腺癌、胃癌、头颈鳞癌、结直肠癌、非霍奇金 淋巴瘤、脑胶质瘤等临床亟需解决的重大疾病。
公司创新生物药研发管线的整体进展情况
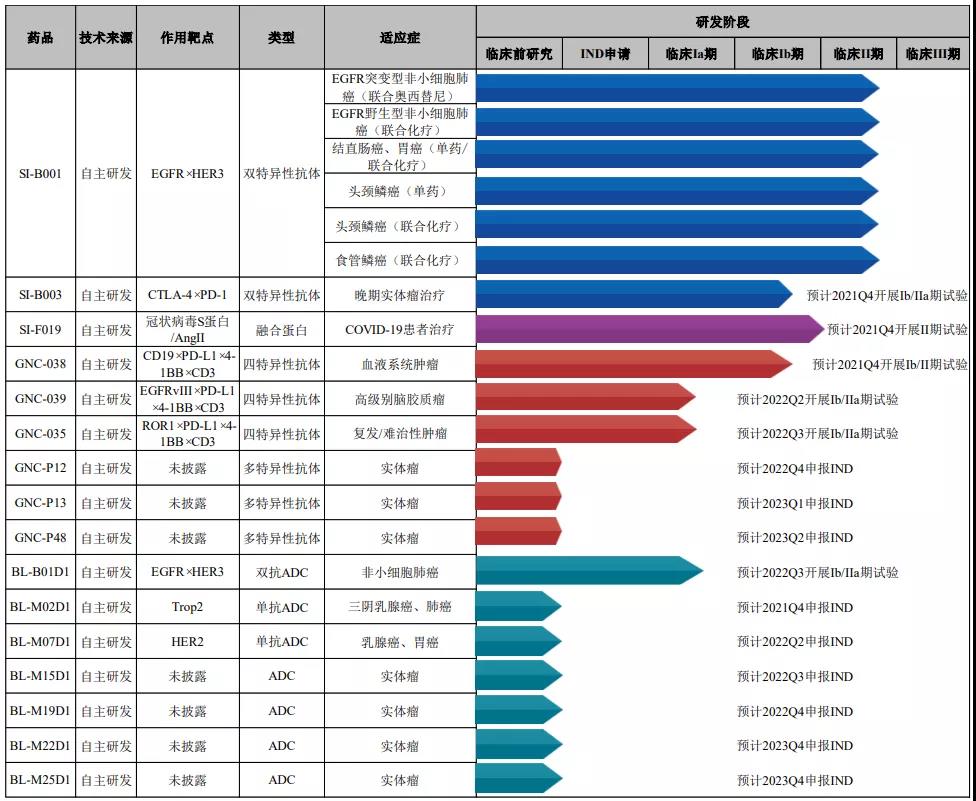
截图自:招股书
SI-B001
SI-B001 为发行人基于自主建立的 SEBA 平台,独立研发的具有完全自主知 识产权和全球权益的双特异性抗体分子,目前已在非小细胞肺癌、结直肠癌、食 管鳞癌、头颈鳞癌等多个上皮肿瘤上开展 6 个 II 期临床研究。SI-B001 可同时靶 向 EGFR 和 HER3 两个肿瘤治疗相关靶点,拟用于非小细胞肺癌、结直肠癌、头 颈鳞癌、食管鳞癌及其他 EGFR 基因驱动型肿瘤的治疗。I 期初步的临床结果显 示,SI-B001 药物安全性良好,PK/PD 特征良好,在 EGFRwt(EGFR 野生型) 驱动的上皮肿瘤中体现出较明显的抗肿瘤活性,临床疗效有望优于现有的非小细 胞肺癌 2 线多西他赛治疗方案。目前正在进一步评估其安全性、耐受性、药代动力学特性以及初步药效学特征。
ErbB(受体酪氨酸激酶)家族包括 EGFR、HER2、HER3、HER4 四个成员, EGFR 和 HER2 的扩增和突变在不同肿瘤中驱动肿瘤的发生发展,HER3 通路为肿瘤治疗中肿瘤逃逸的主要机制之一,HER4 在肿瘤发生发展和逃逸机制中的研究相对较少。 SI-B001 是具有抗肿瘤活性的重组人源化双特异性抗体药物,可同时结合肿 瘤细胞上的 EGFR×EGFR 同源二聚体和 EGFR×HER3 异源二聚体,阻断 EGFR 及 HER3 与其各自配体的结合,从而进一步阻断 EGFR 和 HER3 及其下游通路 (如 RAS-MAPK、PI3K-AKT、JAK-STAT 通路等)的药理活性,实现抑制和杀伤肿瘤的目的。
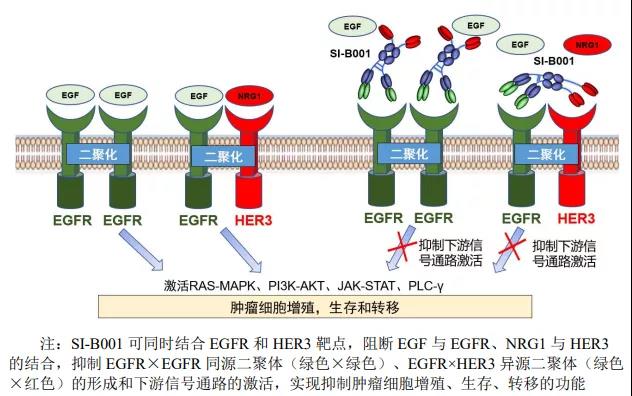
临床试验情况:截至 2021 年 9 月 9 日,SI-B001 已完成 49 例患者的给药。SI-B001 临床用 药安全性较好,不良反应大多较轻微。初步的临床试验结果显示,SI-B001 在 EGFR/ALK 野生型非小细胞肺癌的肺鳞癌后线(中位 4 线)治疗中表现出积极 的疗效,疾病控制率 DCR 为 87.50%(7/8),其中 PR 为 12.50%(1/8);非小 细胞肺癌 2 线化疗药物多西他赛的历史数据,疾病控制率 DCR 为 48.54% (50/103),其中 PR 为 5.82%(6/103)。
其他产品详见招股书
参考来源:
[1] 百利天恒官网
[2] 百利天恒招股书























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论