
新冠疫情爆发,让mRNA疫苗凭借优异的技术登上历史舞台。与其他疫苗相比,mRNA疫苗用于预防新型冠状病毒感染,具有安全、高效、易生产等优点。12月,新冠病毒变异株mRNA疫苗喜报频传,小编汇总如下:
一、沃森生物

12月24日凌晨,沃森生物在互动易上回复称,公司已进入III期临床研究阶段的新冠病毒变异株mRNA疫苗(S蛋白嵌合体)已开展的临床试验方案覆盖了当前流行的主要毒株,抗原整合了Alpha变异株全部突变位点及Beta变异株关键突变位点,其中已覆盖Omicron变异株7个突变位点。另外,公司与蓝鹊生物合作研发的双价苗RQ3025采用两条mRNA设计,编码嵌合S蛋白抗原,临床前研究表明对当前流行的主要毒株能够产生有效的中和抗体,目前公司正在推进该候选疫苗的临床申请准备工作。
二、瑞科生物
12月23日,瑞科生物在港交所公告,公司重组双组分新冠肺炎疫苗ReCOV的菲律宾II期序贯加强临床试验取得积极结果。该临床研究旨在已完成灭活疫苗基础免疫的人群中,比较ReCOV与辉瑞mRNA疫苗COMIRNATY®加强免疫的免疫原性和安全性。研究结果显示,ReCOV序贯加强诱导的针对奥密克戎变异株BF.7和BA.2.75的中和抗体水平均显著优于mRNA疫苗组(差异有统计学意义)。
三、艾博生物
12月22日,艾博生物科技有限公司宣布,旗下新冠疫苗研发管线中奥密克戎变异株(以下简称“奥株”)BA.4/5 mRNA疫苗于近日先后在菲律宾、阿联酋两地启动三期临床研究受试者入组。
应对不断变化的新冠疫情,艾博生物mRNA技术平台迅速开发奥株BA.4/5mRNA疫苗。作为公司新冠疫苗研发管线中的第三代疫苗,该款新冠病毒变异株mRNA疫苗在公司此前于印尼上市的mRNA疫苗ARCoV的技术上进行了工艺优化,进一步提高了疫苗的安全性和有效性,并于2022年10月首先在阿联酋获批并顺利开展一期临床。盲态下的安全性数据显示,接种一剂BA.4/5 mRNA疫苗后不良事件发生率低且级别轻微,均为1级,无2级或以上不良事件,展现出良好的安全性和耐受性。
四、BioNTech和复星医药
12月22日,BioNTech和复星医药共同宣布,由两家公司供应的约1.15万复必泰mRNA新冠疫苗,已于2022年12月21日运抵中国北京,具体包括针对Omicron BA.4/BA.5变异株的复必泰二价疫苗和复必泰单价疫苗BNT162b2。由此,北京、上海、广州、沈阳和成都在华常住德籍公民将可接种复必泰二价疫苗和复必泰单价疫苗BNT162b2。
五、斯微生物
12月8日,斯微(上海)生物宣布其自研的新型冠状病毒mRNA疫苗(商品名:斯维尔克)获得老挝人民民主共和国卫生部食品药品监督管理局授予的紧急使用授权(EUA),用于18周岁及以上人群通过主动免疫来预防新冠病毒肺炎。这是第一个在老挝获批的国产新型冠状病毒mRNA疫苗,也是中国第一个获得紧急使用授权的新冠病毒变异株mRNA疫苗。
斯微生物的新冠病毒变异株mRNA疫苗在研发设计中包含了德尔塔、奥密克戎等多种新冠病毒变异株均有的D614G突变,对当前全球范围最主要流行的新型冠状病毒株具有保护效力,有一定的广谱性,这款疫苗在-20±5℃的条件下稳定性良好,有效期长达24个月。斯微生物称,该款疫苗远优于国外的同类疫苗。目前,斯微生物已完成了在老挝当地的土地投资,并已启动建设疫苗生产基地,该工厂计划年产能2000万剂次。这是老挝的第一个疫苗生产基地,也是斯微生物第一个海外疫苗生产基地。
除此之外,我国布局mRNA疫苗研发企业还有深信生物、智飞生物、石药集团、康希诺等。
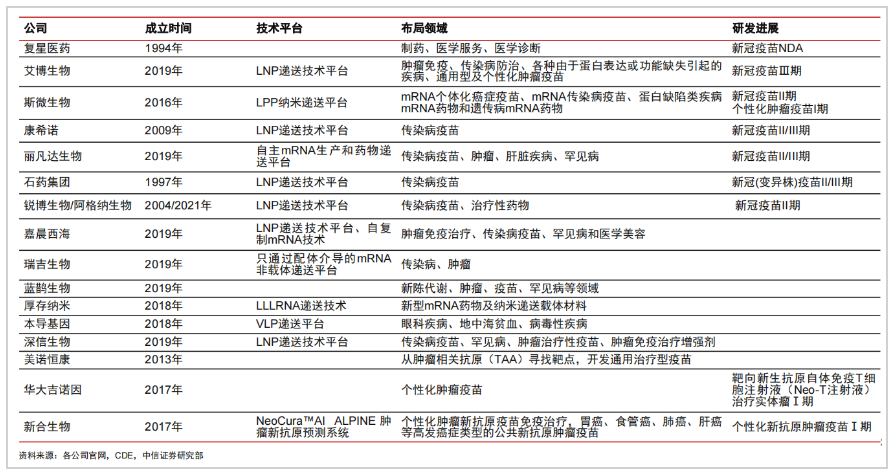
来源:财联社
目前,全球人口数量近80亿,为达到群体免疫效果,新冠疫苗接种率需要达到60%-80%,取中间值70%来计算,全球约56亿人需接种新冠疫苗。而新冠病毒变异株mRNA疫苗相较于传统其他技术路径疫苗优势明显,具备发展潜力。由此可见,mRNA疫苗市场空间巨大。除新冠疫苗外,mRNA疫苗还可以制备其他传染病疫苗、抗肿瘤疫苗、罕见病疫苗等。
参考资料:
[1]各公司公告
[2]财联社
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论