
随着新冠感染人数的攀高,网络上对新冠“特效药”的关注和购买需求也是有增无减。不少人加入了购买“新冠特效药”的队列中,据报道称,原价为2300元/盒的Paxlovid,黄牛价格被炒至15000元,关键还买不到,大都“一药难求”。
一时之间,“P药”(奈玛特韦/利托那韦片,Paxlovid)成为热词,牵动受困于新冠疫情民众的神经。人们对新冠“特效药”的评价也呈现两极分化态势。但无论外界的争议如何,大家需要了解的是,Paxlovid不是神药,且为处方药,使用时应谨遵医嘱、避免盲从用药。
经药融云数据库查询,目前我国已批准新冠治疗的药物有:奈玛特韦片/利托那韦片组合包装(Paxlovid)、安巴韦单抗/罗米司韦单抗注射液(BRII-196/BRII-198)、阿兹夫定片。
一、安奈玛特韦片/利托那韦片组合包装(Paxlovid)
Paxlovid是由美国辉瑞公司研制的一款治疗新型冠状病毒肺炎感染(COVID-19)的口服抗病毒药物。2021年12月率先在美国获批上市,用于12岁以上且体质量至少为40kg的轻度至中度新冠肺炎感染人群,使其成为美国首个获批的口服小分子新冠病毒治疗药物。
2022年2月,国家药监局附条件批准Paxlovid进口注册,用于治疗成人伴有进展为重症高风险因素的轻至中度新冠肺炎患者,例如伴有高龄、慢性肾脏疾病、糖尿病、心血管疾病、慢性肺病等重症高风险因素的患者;随后3月被纳入国家卫健委发布的《新型冠状病毒肺炎诊疗方案(试行第九版)》中。
Paxlovid新冠适应症研发详情(部分)(微信搜索"药融云小程序"进行相关更多数据查询)
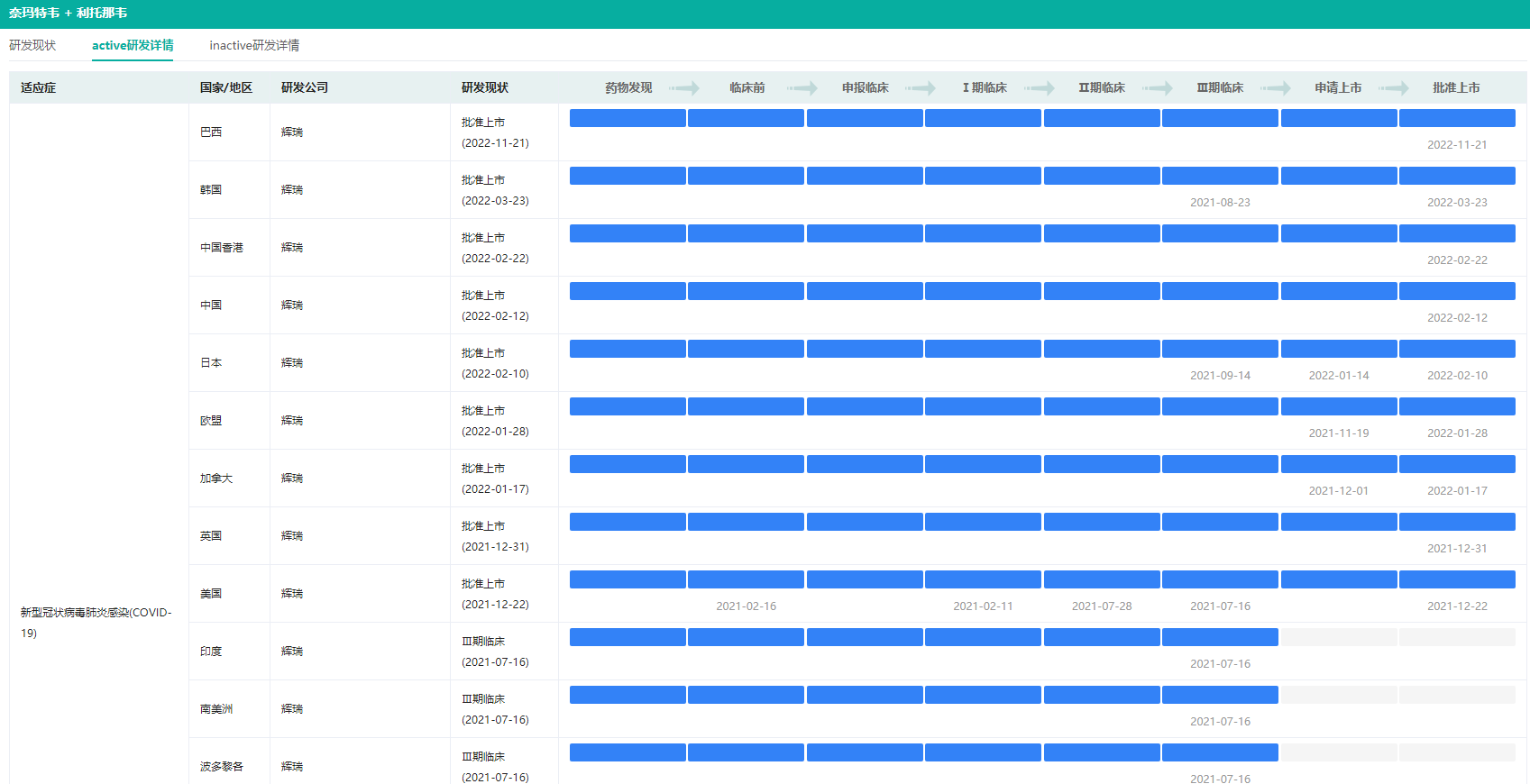
图片来源:药融云全球药物研发数据库
1.Paxlovid的作用机理
Paxlovid是由利托那韦(Ritonavir)和奈玛特韦(Nirmatrelvir)组成的复合药。其核心组分奈玛特韦能够阻止病毒复制,而利托那韦能减少奈玛特韦代谢(相当于承担了“延长攻击时间”的角色),从而提高奈玛特韦血药浓度,两者要一起用,否则奈玛特韦的血浆水平可能不足以达到所需的治疗效果。
奈玛特韦是一种SARS-CoV-2主要蛋白酶Mpro(也称为3C-样蛋白酶,3CLpro)的拟肽类抑制剂,抑制SARS-CoV-2Mpro可使其无法处理多蛋白前体,从而阻止病毒复制。利托那韦抑制CYP3A介导的奈玛特韦代谢,从而升高奈玛特韦血药浓度。
其临床研究表明,Paxlovid能降低89%的住院死亡风险。但值得关注的是,由于包含CYP3A4酶抑制剂利托那韦,造成其与很多药物存在相互作用,并影响肝肾功能,所以很大程度上限制了其用药人群,增加了有基础疾病和老年人群的用药风险。
奈玛特韦+利托那韦III期临床试验结果(部分)
图片来源:药融云临床试验结果数据库
2.Paxlovid的适用人群
Paxlovid是治疗新冠的处方药,在医疗机构在医生的指导下使用,不是预防新冠的药物。据国家卫健委发布第九版《新型冠状病毒肺炎诊疗方案》中关于Paxlovid的适用人群描述是:适用于发病5天以内的轻型和普通型且伴有进展为重型高风险因素的成人和青少年(12-17岁,体重≥40kg)。
也就是说,并没有把这个药推荐作为危重症新冠患者最后兜底的具备力挽狂澜能力的“神药”。只是把它作为一个阻止病程发展药物,阻止高风险患者的新冠病程向危及生命的重症去进展。也就是说,已经进入到重症、危重症阶段的新冠患者,用它是不对症的。而非高危人群,使用的效果很有限。
二、安巴韦单抗/罗米司韦单抗注射液
2021年12月,国家药品监督管理局应急批准了中国首个自主知识产权新冠病毒中和抗体联合治疗药物——安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198),用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12-17岁,体重≥40kg)新型冠状病毒感染(COVID-19)患者。其中青少年(12-17岁,体重≥40kg)适应症人群为附条件批准。
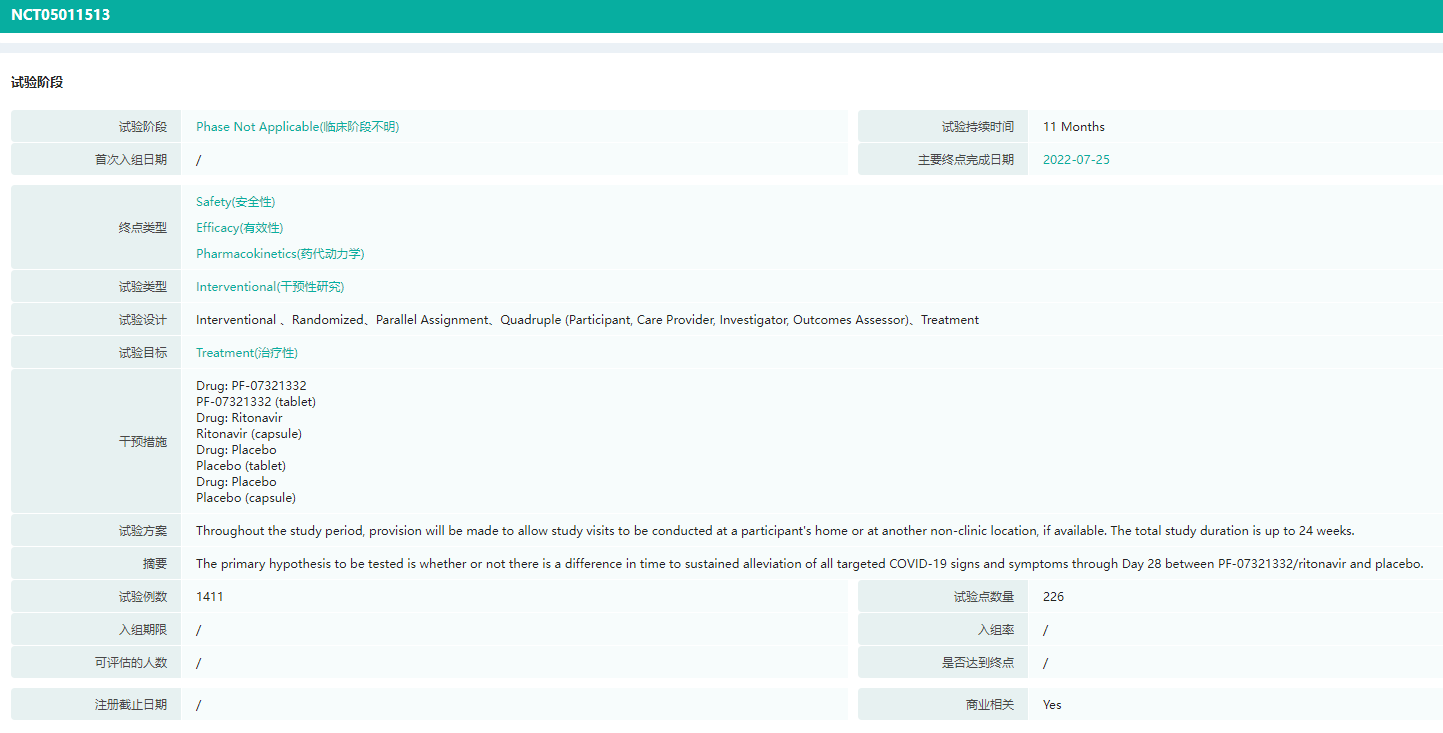
安巴韦单抗+罗米司韦单抗新冠适应症研发详情(部分)
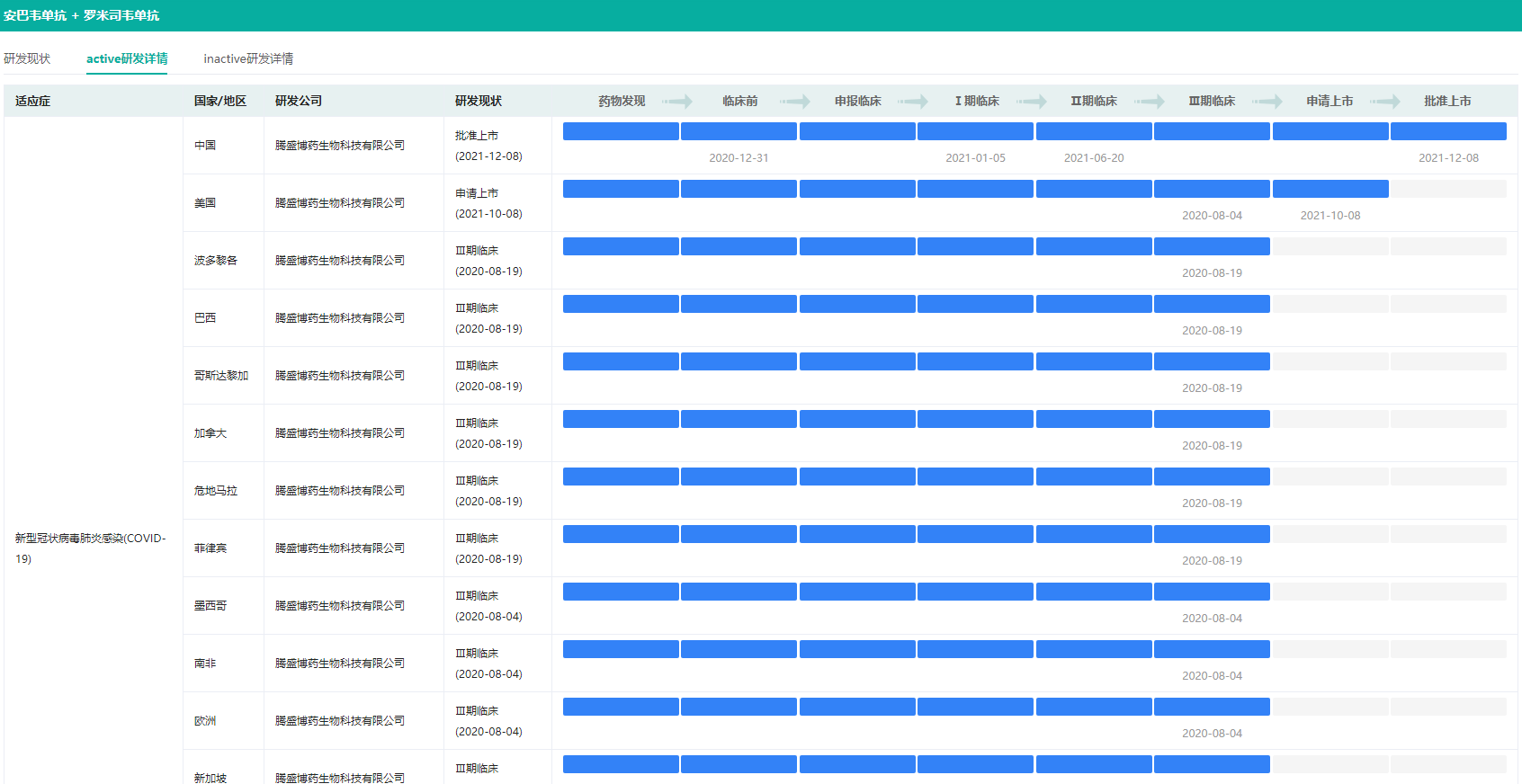
图片来源:药融云全球药物研发数据库
安巴韦单抗/罗米司韦单抗注射液是腾盛博药与清华大学、深圳市第三人民医院共同研发的单克隆抗体药物,于2022年3月获国家卫生健康委员会批准纳入《新型冠状病毒肺炎诊疗方案(试行第九版)》。此后,多个省市医疗保障局将其临时性纳入本省份医保基金支付范围,包括湖南、北京、上海、浙江、江苏、四川、山西、贵州、辽宁以及安徽等。
其临床试验结果显示,与安慰剂相比,安巴韦单抗/罗米司韦单抗联合疗法使临床进展高风险的新冠门诊患者住院和死亡风险降低80%。同时,无论早期即开始接受治疗(症状出现后5天内)还是晚期才开始接受治疗(症状出现后6至10天内)的患者,住院和死亡率均显著降低,为新冠患者提供了更长的治疗窗口期。
目前,腾盛博药已与国药控股达成战略合作,共同推进该药物在中国的商业化进程。
三、阿兹夫定片
据药融云数据库统计,目前国内已上市的针对新冠肺炎的口服小分子药物有2款,辉瑞的Paxlovid和真实生物的阿兹夫定。
其实,阿兹夫定(Azvudine)是一种艾滋病毒逆转录酶(RT)抑制剂,于2013年获批开始进入临床试验,2021年7月作为抗艾滋病药物获批上市。2022年7月,阿兹夫定老药新用,获得国家药监局紧急附加条件批准,成为中国紧急批准授权使用的唯一一款国产新冠口服药。
同年8月,阿兹夫定片被正式纳入《新型冠状病毒肺炎诊疗方案(第九版)》,用于治疗普通型新型冠状病毒肺炎(COVID-19)成年患者,患者在医师指导下严格按说明书用药。
阿兹夫定合成路线
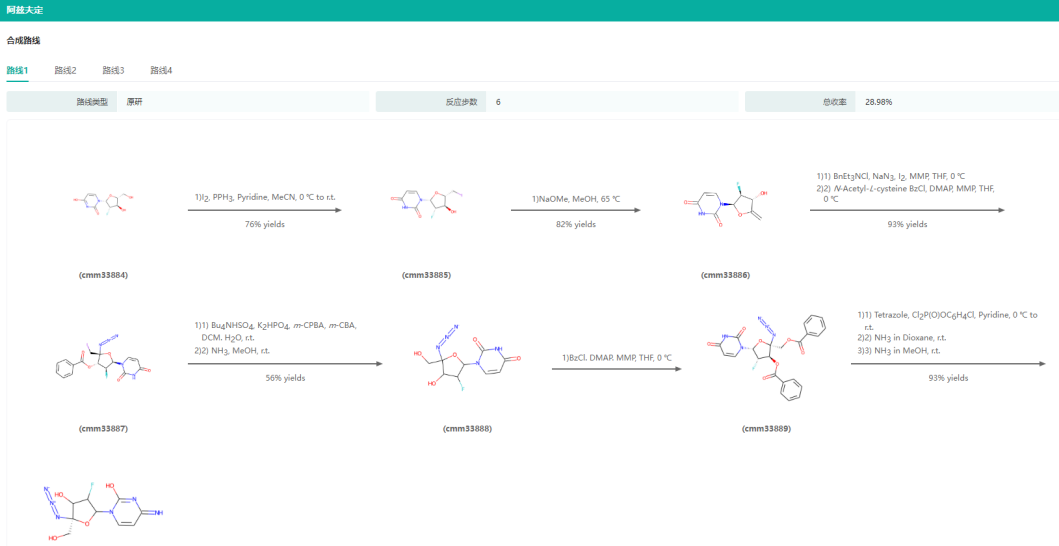
图片来源:药融云合成路线数据库
1.阿兹夫定的作用机制
为什么治疗艾滋病的药物,会被列为新冠的治疗药呢?这是因为,新冠病毒同艾滋病毒一样,也属于RNA病毒。阿兹夫定是一种广谱RNA病毒抑制剂,作为一种人工合成的病毒RNA依赖的RNA聚合酶(RdRp)的核苷类似物,在细胞内代谢成具有抗病毒活性的5’-三磷酸盐代谢物(阿兹夫定三磷酸盐),能特异性作用于新冠病毒聚合酶(RdRp),在新冠病毒RNA合成过程中嵌入病毒RNA,从而抑制新冠病毒复制,达到治疗新冠病毒感染的作用。
目前,阿兹夫定片已纳入医保支付范围,在全国31个省、市、自治区完成医保挂网,已覆盖全国2000多家医院,挂网价为270元/瓶。值得注意的是,阿兹夫定也并非预防药,不存在预防效果,且是治疗新型冠状病毒肺炎的处方药,不适合自行服用,需要在医生的指导下使用!
四、国产热门在研新冠口服药——3CL蛋白酶抑制剂
新冠病毒的RNA依赖性RNA聚合酶、PLpro、3CL蛋白酶及解旋酶等病毒蛋白酶是主要的抗病毒的靶点。据药融云数据库统计,目前国产在研新冠口服药的开发中,3CL蛋白酶抑制剂是在研品种最多、且被业内最为看好的小分子药物。
国内已有十多家医药企业和科研机构在进行3CL靶点抗新冠病毒药物研发。进度较快的有先声药业的SIM-0417和众生药业的RAY -1216,目前SIM-0417已完成III期临床全部患者入组,成为国内3CL靶点口服小分子药物首个II/III期临床研究入组完成的项目。RAY -1216当前也正在开展III期临床研究。
SIM-0417临床试验信息(部分)
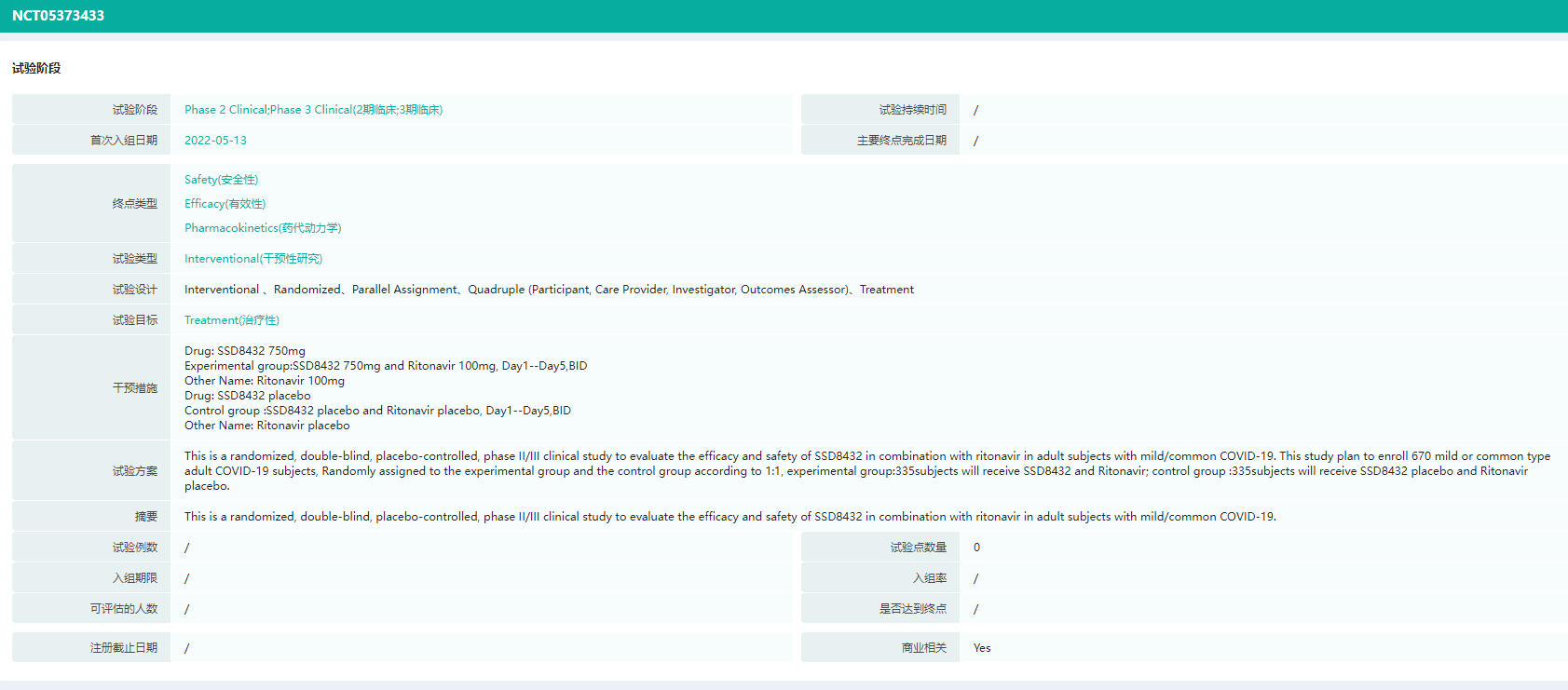
图片来源:药融云全球临床试验数据库
国产口服抗新冠病毒3CL蛋白酶抑制剂谁能最先“撞线”,值得关注。除此之外,还有君实生物、歌礼生物、豪森药业、瑞阳制药等企业也在积极进行相关药物的研发。
想要解锁更多疾病领域信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握疾病领域涉及药物信息、销售情况与各维度分析、市场竞争格局、创新药研发情况、仿制药布局情况、最新进展、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论