ROCK抑制剂新药
2021年12月7日,来自日本的参天制药株式会社(总部位于大阪,以下简称“参天”)宣布了其与Aerie Pharmaceuticals(总部位于北卡罗来纳州达勒姆,以下简称“Aerie”)达成了针对Rhopressa® / Rhokiinsa®(Netarsudil ophthalmic solution,奈塔舒地尔滴眼液)和Rocklatan® / Roclanda®(Netarsudil and latanoprost ophthalmic solution,奈塔舒地尔和拉坦前列素滴眼液)的独家开发和商业化协议,以扩大产品的全球部署,双方达成一项新协议,将目光投向更多地区,包括欧洲、中国等目标市场。此前在2020年10月,参天制药与Aerie签署了针对日本和其他亚洲国家/地区的产品独家开发和营销协议。

经药融云数据库查询,这两款滴眼药都是ROCK抑制剂,除此以外还共同拥有NAT、TGFB2靶点,都是用于治疗降低开角型青光眼或高眼压患者的高眼压。Rhopressa® 最早于2017年12月在美国获FDA批准上市,Rocklatan®最早于2019年在美国上市。且据药融云估计,Rhopressa®在2018年的全球销售额达2亿4千万美元。
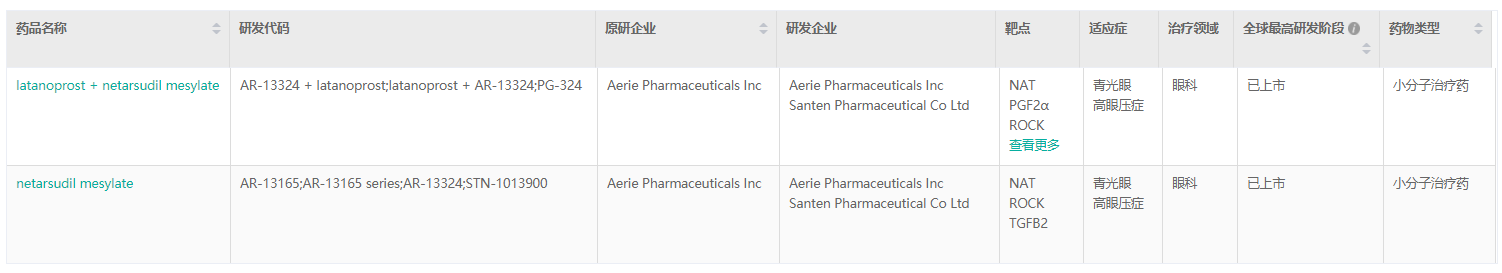
截图来源:药融云全球药物研发数据库
通过这项新的合作协议,参天制药将把ROCK抑制剂的优势推广到全球其他地区,进一步加强其全球青光眼产品组合。根据新协议的条款,Aerie将收到8800万美元的预付款,还有后期的阶段性付款和专利权使用费。
Aerie是一家眼科制药公司,专注于发现、开发和商业化治疗原发性开角型青光眼、眼表疾病和视网膜疾病的首创疗法。Rhopressa®0.02%和Rocklatan®0.02%/0.005%已通过Aerie批准并在美国销售。Aerie还分别获得了Rhokiinsa®和Roclanda®这两款产品在欧盟和英国的市场授权。日本2020年11月开始的Rhopressa®的III期临床试验,在第4周眼压(IOP)测量的主要终点,每日滴用一次0.02%奈塔舒地尔(Netarsudil)优于每日滴用两次0.4%利帕舒地尔(Ripasudil)。此外公司还有AR-215在临床前开发阶段。
眼科大市场
青光眼是一种导致视神经损伤,从而导致视野丧失的疾病,是许多国家视力下降和失明等视力损伤的主要原因。由于该疾病通常是进展性和不可逆的,早期发现和治疗以控制此类损害和视野缺损的进展在治疗中至关重要,同时降低眼压是避免青光眼损害的最有效手段。
据中华医学会眼科学分会发布的《中国青光眼指南(2020)》显示,2020年全球原发性青光眼患病人数超过7600万,我国达到了2100万,其中40岁以上人群的患病率达到3.05%。预计到2030年,全球患者将增加到9500万。
眼科学会表示,有5类人群属于青光眼高风险人群:600度以上的高度近视或远视;有青光眼家族史;患有心血管系统疾病;患有糖尿病;40岁以上人群。以上5类人群应定期到医院做青光眼的相关检查,以排除或早期发现青光眼,及早治疗。
药融云数据显示,眼科领域本靶点新药,中国在研企业有维眸生物(VVN539);成都先导(HGC-245);四川大学等等。其中,维眸生物是专注于眼科治疗领域的临床阶段创新药公司,成立于2016年;公司由国际一流的眼科药物研发专家团队组建,已经建立起独特的眼科创新药研发平台,自主研发的多个创新药产品已经或即将进入临床阶段。其中,针对干眼症的VVN001进展最快,现已处于临床2期研发阶段。
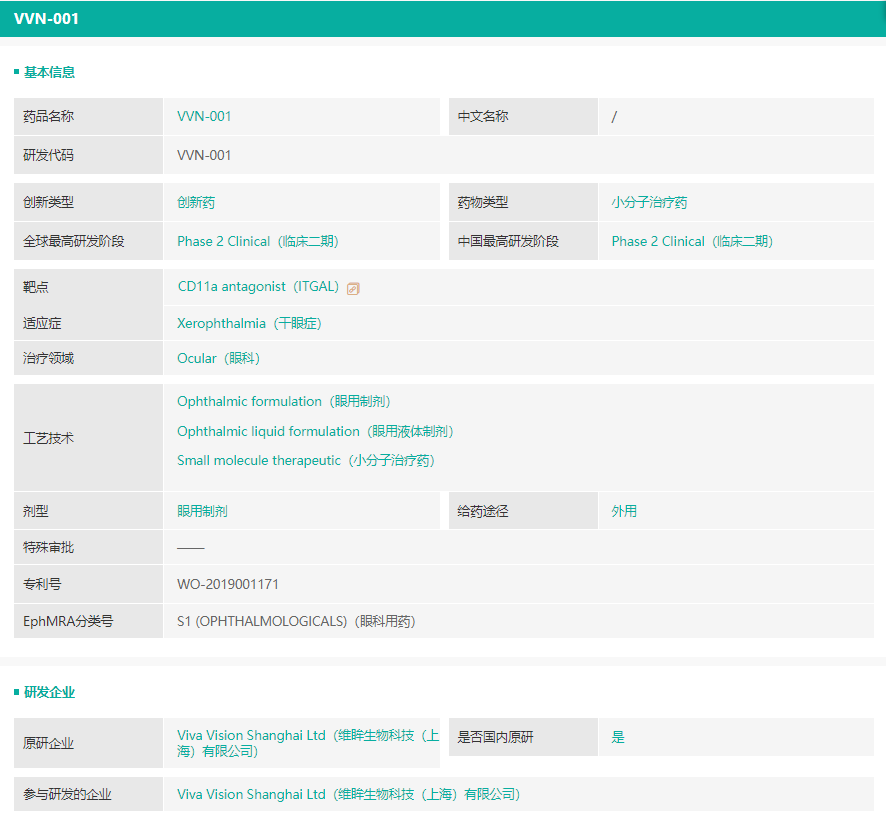
截图来源:药融云全球药物研发数据库
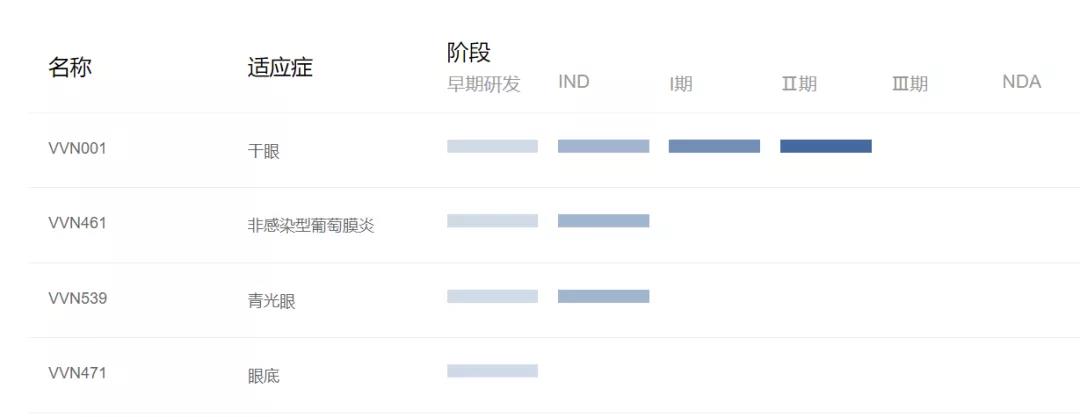

来源:维眸生物企业公告
参考:
NMPA/CDE;
药融云数据 www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露;
Aerie Concludes Exclusive License Agreement With Santen for Rhopressa® and Rocklatan® in Europe and Several Other Regions | Aerie Pharmaceuticals, Inc;
中华医学会眼科学分会发布的《中国青光眼指南(2020)》;
维眸生物科技有限公司 (vivavisionbio.com);
小分子药物发现-成都先导官网 (hitgen.com);等等。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论