
2025年8月22日,苏州血霁生物科技有限公司(以下简称“血霁生物”)所提交的“巨核细胞注射液”新药临床试验申请(IND)获得美国药品监督管理局(FDA)的正式批准!这是全球首个巨核细胞注射液的正式临床试验申请,为血霁生物自主研发的使用造血干细胞分化获得的巨核细胞产品,适应症为肿瘤治疗引起的血小板减少症,这将是现有的升板药治疗和血小板输注的巨大补充,有望为每年几千万人次的血小板减少症人群带来新希望,具有重要的社会价值和经济价值。
这是血霁生物重磅推出的“隐身管线”——全球首个用于血小板数量回升的巨核细胞注射液,这也是血霁生物自主研发的无任何基因编辑的细胞治疗产品,将以全球首款细胞新药进入全球百亿美金的升板药市场的竞争。巨核细胞是产生血小板的前体细胞,一方面在其回输回体内后可以迅速、稳定、且持续产生血小板细胞,另一方面使血小板功能成熟、完备,解决了iPSC技术存在的成熟度低及生命周期短等问题;此外该注射液对比其他升板药,可以实现无毒副,高效且长效的作用。血霁生物将持续通过不同的产品品类覆盖用血人群的不同需求,带来第二次输血革命。
关于血霁生物
血霁生物于2021年6月成立于苏州工业园区生物医药产业园,是由海归专家创立的体外再生造血世系(包括血液细胞和免疫细胞)的新型细胞治疗企业,具有独特的干细胞重编程、编辑和分化技术,据摩熵医药数据库可得,血霁生物以血小板的体外再生作为做优先和核心发展的方向,切入成体干细胞和iPSCs细胞定向分化的细胞治疗领域。
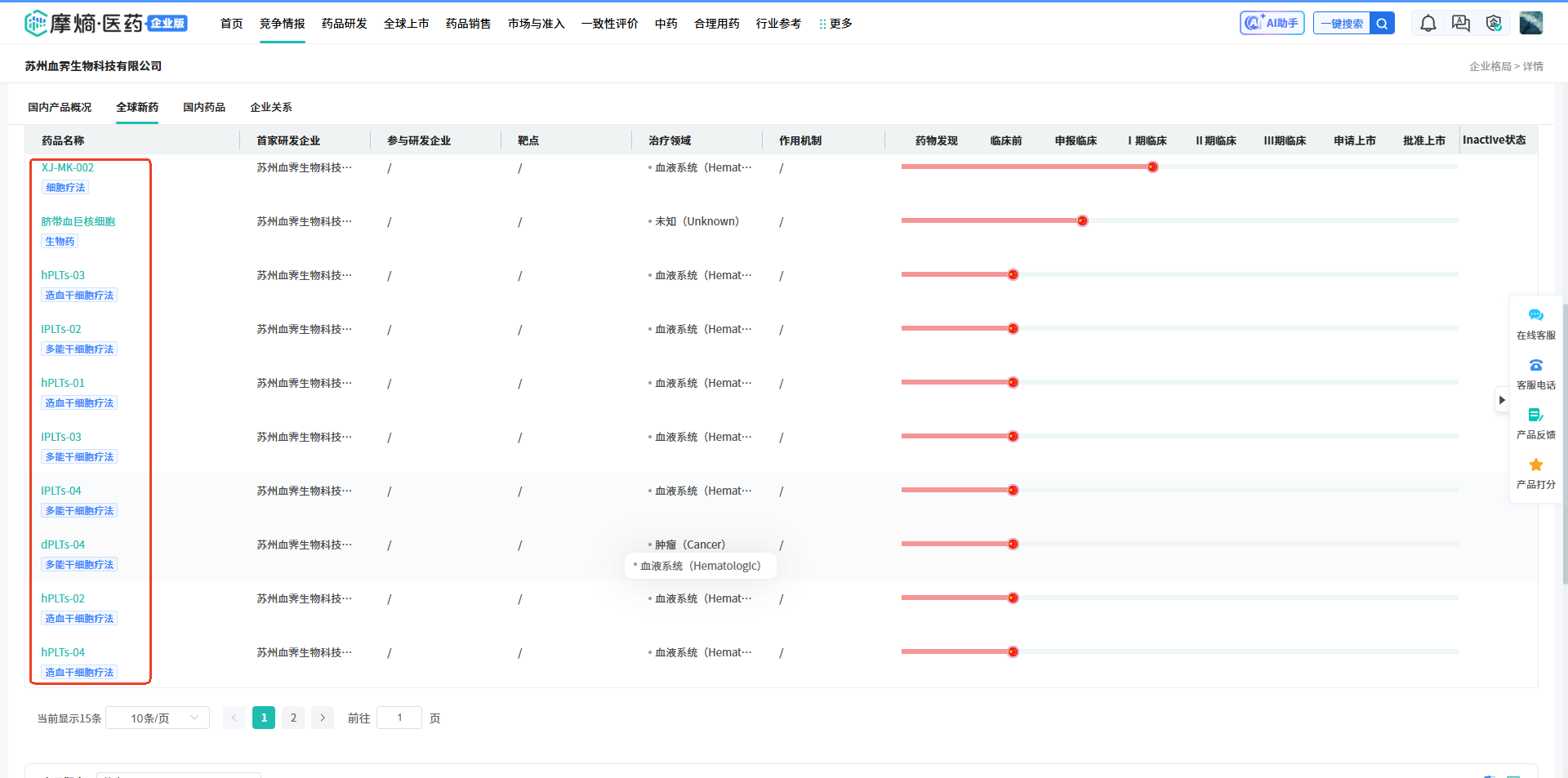
截图来源:摩熵企业格局数据






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论