
作为今年最受瞩目的决定之一,FDA预计将于12月8日公布对Vertex 和CRISPR用于治疗镰状细胞病(SCD)的基因编辑疗法 exagamglogene autotemcel(exa-cel)的裁决,如果获得批准,exa-cel将成为美国首款CRISPR编辑基因疗法。11月17日,exa-cel已经获得英国有条件上市许可,用于治疗12岁及以上镰刀型细胞贫血病(SCD)伴复发性血管闭塞危象(VOCs)患者,以及无法获得人类白细胞抗原(HLA)匹配造血干细胞移植治疗的输血依赖性β地中海贫血(TDT)患者。
距离FDA裁决还有几天,CRISPR Therapeutics正在放弃其“第一代”同种异体CAR-T候选药物。根据12月4日市场收盘后发布的消息,CRISPR Therapeutics正在削减两种CAR-T候选药物,称为CTX110和CTX130,并转向其“下一代候选药物”。

具体如下,CRISPR Therapeutics宣布更新免疫肿瘤学管道并扩展到自身免疫性疾病。
(1)基于正在进行的临床试验的初步数据,重点是下一代CAR - T候选产品,靶向CD19的CTX112和靶向CD70的CTX131
(2)除了正在进行的b细胞恶性肿瘤临床试验外,将CTX112扩展到自身免疫性疾病的试验,计划于2024年上半年启动
(3)除了正在进行的实体瘤临床试验外,将CTX131扩展到血液系统恶性肿瘤,包括T细胞和b细胞恶性肿瘤
(4)在内部GMP工厂生产的下一代候选产品具有更高的制造稳健性和可扩展性
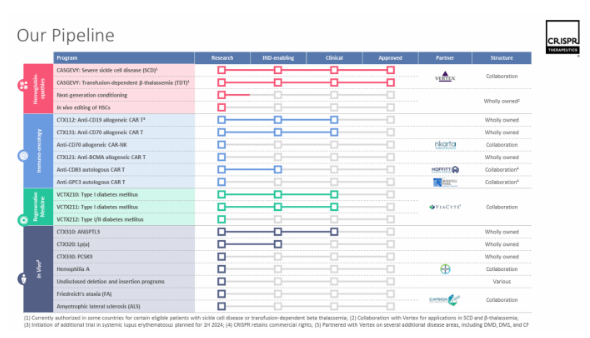
CTX110被设计用于靶向CD19,针对b细胞恶性肿瘤,而CTX130被用于实体瘤和某些血液系统恶性肿瘤的检测。根据新闻稿,这两个项目为公司“证明了异体CAR-T细胞在标准淋巴细胞消耗方案后可以产生持久缓解的概念”。
但CRISPR Therapeutics认为下一代候选CTX112和CTX131可以做得更好。这一决定是基于正在进行的临床试验的早期数据,这些数据表明,较新的药物可以提高早期候选药物的疗效。根据该公司的说法,与早期的候选药物相比,对CTX112和CTX131进行的基因编辑导致患者体内更高的CAR-T细胞扩增和功能持久性。此外下一代候选产品也有更好的生产概况,每批生产的CAR-T细胞数量更高、更一致。
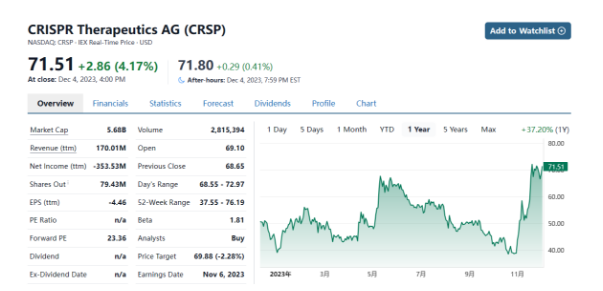
CRISPR Therapeutics目前市值57亿美元,近一年股价涨幅37%。,截止到三季度末,在手现金及等价物5亿美元。
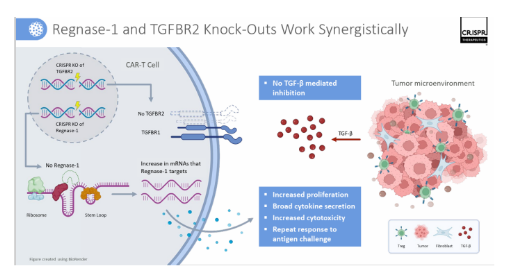
基于这些考虑,公司正专注于CTX112和CTX131的开发,并将在必要时将CTX110和CTX130治疗的患者转为长期随访。目前备受关注的是靶向CD19的CTX112,目前正在b细胞恶性肿瘤患者的1/2期临床试验中进行研究。与此同时,CTX131靶向CD70,正在实体肿瘤的1/2期临床试验中进行测试。这两种资产包括Regnase-1编辑,它被认为可以去除T细胞功能的“刹车”,以及TGFBR2编辑,旨在删除T细胞抗肿瘤活性的“刹车”。
CRISPR Therapeutics首席执行官兼董事会主席Samarth Kulkarni博士说:“我们的下一代同种异体CAR - T候选药物反映了我们的使命,即不断创新,尽快为患者带来潜在的变革性药物。“我们对下一代CAR - T平台感到兴奋,将我们的努力集中在这些候选药物上,将使我们能够更有效、更快速地推进这些潜在的一流CAR - T疗法。“我们对下一代候选药物的进展和早期临床数据感到非常鼓舞。
CRISPR Therapeutics首席医疗官PK Morrow医学博士说:“虽然我们看到了CTX110巩固剂量的好处,但我们相信CTX112可以为患者带来更好的结果。”“我们感谢参与CTX110和CTX130临床试验的患者、家属和研究人员,并期待从这些项目中吸取教训,加快CTX112和CTX131的开发。”
CRISPR Therapeutics还计划在明年上半年启动CTX112在系统性红斑狼疮中的临床试验,随后有可能扩展到其他自身免疫性适应症。该公司引用早期临床研究表明,cd19导向的自体CAR-T疗法可导致几种自身免疫性疾病的持久缓解。
所有这些变化都发生在FDA即将决定合作伙伴Vertex的exa-cel的时间之前,该药已经提交了镰状细胞贫血的批准申请,将于12月8日决定。
尽管早些时候获得了英国监管机构的批准,并且在10月31日的FDA顾问会议上收到了相当积极的反馈,CRISPR Therapeutics仍然不得不在今年11月进行裁员。三位熟悉这一决定的消息人士告诉Fierce Biotech,裁员通知是在11月7日发出的,其中两位消息人士称大约有50名员工被解雇,占公司员工总数的约10%。
CRISPR Therapeutics
CRISPR Therapeutics是一家领先的基因编辑公司,专注于使用其专有的CRISPR/Cas9平台开发针对严重疾病的变革性基因药物。CRISPR/Cas9是一项革命性的基因编辑技术,它允许对基因组DNA进行精确、定向的改变。CRISPR Therapeutics已经在广泛的疾病领域建立了一个治疗项目组合,包括血红蛋白病、肿瘤学、再生医学和心脏代谢疾病。
研发管线(部分)

截图来源:药融云全球药物研发数据库
为了加速和扩大其努力,CRISPR Therapeutics已与包括拜耳、顶点制药和ViaCyte在内的领先公司建立了战略合作伙伴关系。CRISPR Therapeutics AG总部位于瑞士楚格,在美国拥有全资子公司CRISPR Therapeutics, Inc.,研发部门位于马萨诸塞州波士顿和加利福尼亚州旧金山,在英国伦敦设有业务办事处。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论