
12月13日,日本卫生部官员表示,阿尔茨海默病的新药lecanemab在日本定价298万日元(20,500美元)/年,该药将于12月20日在日本正式上市。

大部分费用将由公共医疗保险支付,接受治疗的人将根据他们的年龄和收入自掏腰包支付10%至30%的费用。预计该药物还将被日本的一个医保系统所涵盖,该系统为患者在一年内可以支付的金额设定了上限。例如,年收入在156万日元至370万日元之间的70岁或以上患者,在支付上限下,每年支付的药物费用不超过144,000日元。该药物治疗那些患有早期阿尔茨海默氏症和轻度认知障碍的人。该机构表示,据估计,日本每年有多达32,000名患者可以使用该药物,相当于986亿日元的市场。
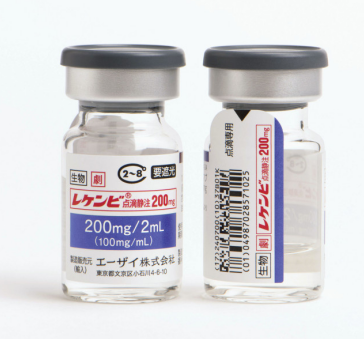
阿尔茨海默氏症药物lecanemab。(照片提供:卫材株式会社)
药物的剂量基于患者的体重。每年298万日元的费用是以体重50公斤的患者计算的。值得注意的是在美国使用lecanemab的每位患者每年的价格为26,500美元。
卫材表示,临床试验表明,与安慰剂相比,该药能抑制记忆力丧失和判断能力受损等症状的进展,减少27%。然而,一些服用该药的患者出现了脑肿胀和出血等副作用。
Lecanemab的全球获批情况
Lecanemab(仑卡奈单抗,商品名:乐意保/Leqembi)是日本卫材药业(Eisai)和美国渤健公司(Biogen)联合开发的靶向β-淀粉样蛋白(amyloidβ-protein,Aβ)的用于治疗早期阿尔茨海默病的新药,该药物适用于患有轻度认知障碍或轻度痴呆的成年阿尔茨海默病患者。这是近20年首个获FDA完全批准的阿尔兹海默病药物,被视为治疗开发的重大突破。
- 2023年1月,美国食品和药物管理局(FDA)给予lecanemab加速批准许可。
- 2023年7月,FDA完全批准了Lecanemab上市。
- 2023年9月,日本药品和医疗器械管理局(PMDA)批准了仑卡奈单抗上市。
- 2023年10月,Leqembi正式通过海南省药品监督管理局审核,落地海南博鳌乐城国际医疗旅游先行区(以下简称“海南乐城”),商品名为“乐意保”,定价3328.2元/瓶。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论