
每年国谈关门时间已经常态化固定至6月30日,所以很多企业为了拿到申报入场券,加班加点,各种资源一起上阵。毕竟,政策越来越卷,晚了一年环境可能已经巨变,参照药集采或者降价,一夜之间千金变平民。
今年上半年一共38个创新药获批上市,赶上当年的国谈,卡在关门前的是信达生物的1类创新药玛仕度肽注射液(商品名:信尔美)6月27日获批上市,用于在控制饮食和增加体力活动基础上对成人患者的长期体重控制,初始体重指数(BMI)为:BMI≥28 kg/m2(肥胖);或BMI≥24 kg/m2(超重),并伴有至少一种体重相关的合并症(例如高血糖、高血压、血脂异常、脂肪肝、阻塞性睡眠呼吸暂停综合征等)。(相关扩展阅读:减重20.1%!信达生物「玛仕度肽」III期临床达到主要终点,多重代谢获益显著)
截止到11月7日,下半年已经有25个创新药获批上市,将于2026年一起决战NRDL竞赛。
7月2日,长春金赛药业的生物药注射用伏欣奇拜单抗(商品名:金蓓欣)获批上市,适用于对非甾体类抗炎药和/或秋水仙碱禁忌、不耐受或缺乏疗效的,以及不适合反复使用类固醇激素的成人痛风性关节炎急性发作。
同日,江苏先声的注射用苏维西塔单抗(商品名:恩泽舒)上市,苏维西塔单抗联合紫杉醇、多柔比星脂质体或拓扑替康用于铂耐药后接受过不超过1种系统治疗的成人复发性卵巢癌、输卵管癌或原发性腹膜癌的治疗。
贝达药业的1类创新药酒石酸泰瑞西利胶囊上市(商品名:康美纳),联合氟维司群,适用于既往接受内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性成年乳腺癌患者。
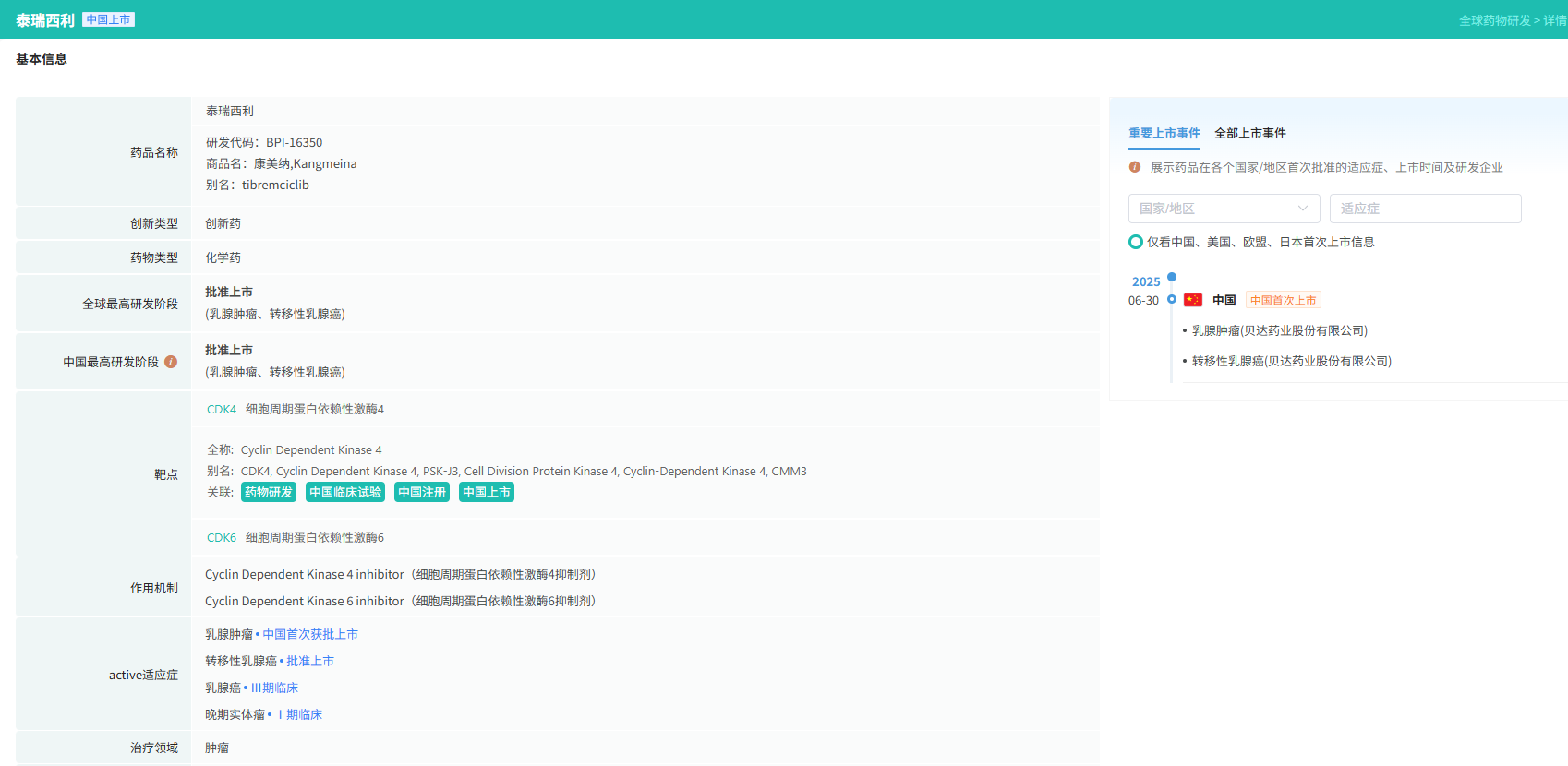
截图来源:摩熵医药数据库-全球药物研发数据库
通过优先审评审批程序附条件批准广州必贝特医药的1类创新药注射用盐酸伊吡诺司他(商品名:贝特琳),单药适用于既往接受过至少两线系统性治疗的复发或难治性弥漫性大B细胞淋巴瘤成人患者。
7月11日,苏州旺山旺水生物医药的1类创新药盐酸司美那非片(商品名:昂伟达),用于治疗勃起功能障碍。
通过优先审评审批程序附条件批准苏州亚盛药业的1类创新药利沙托克拉片上市(商品名:利生妥),用于既往经过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者。
7月18日,南京征祥医药的1类创新药玛硒洛沙韦片(商品名:济可舒)获批上市,用于既往健康的成人单纯性甲型和乙型流感患者的治疗,不包括存在流感相关并发症高风险的患者。
通过优先审评审批程序批准武汉禾元生物申报的重组人白蛋白注射液(水稻)(商品名:奥福民)上市,适用于肝硬化低白蛋白血症(≤30g/L)的治疗。
7月25日,扬子江的1类创新药盐酸妥诺达非片(商品名:泰妥妥)上市,该药适用于治疗勃起功能障碍。
7月30日,上海恒润达生的雷尼基奥仑赛(商品名:恒凯莱)上市,用于治疗经过二线或以上系统性治疗后成人复发或难治性大B细胞淋巴瘤,包括弥漫性大B细胞淋巴瘤非特指型、滤泡性淋巴瘤转化的弥漫性大B细胞淋巴瘤、伴MYC和BCL2重排的高级别B细胞淋巴瘤、高级别B细胞淋巴瘤非特指型。
8月1日,康缘的中药1.1类创新药参蒲颗粒上市。处方源自临床经验方,具有益气活血,清利湿热,通络止痛功效,用于盆腔炎性疾病后遗症引起的慢性盆腔痛中医辨证属湿热瘀阻证。
8月22日,通过优先审评程序附条件批准Novartis Pharma Schweiz AG的1类创新药盐酸阿曲生坦片上市,适用于降低有疾病快速进展风险的原发性免疫球蛋白A肾病(IgA肾病)成人患者的蛋白尿。
轩竹生物科技的1类创新药地罗阿克片(商品名:轩菲宁)上市,该药品单药适用于未经过间变性淋巴瘤激酶(ALK)抑制剂治疗的ALK阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
Daiichi Sankyo Europe GmbH申报的注射用德达博妥单抗(商品名:达卓优)上市,适用于治疗既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的激素受体(HR)阳性、人类表皮生长因子受体2(HER2)阴性(IHC 0、IHC 1+或IHC 2+/ISH-)乳腺癌成人患者。
通过优先审评审批程序批准武汉生物制品研究所有限责任公司申报的口服六价重配轮状病毒减毒活疫苗(Vero细胞)(商品名:武生儿轮宝)上市,适用于预防轮状病毒血清型G1、G2、G3、G4、G8、G9引起的婴幼儿急性胃肠炎。
8月29日,通过优先审评审批程序附条件批准恒瑞的1类创新药泽美妥司他片(商品名:艾瑞璟)上市,该药品适用于既往接受过至少1线系统性治疗的复发或难治外周T细胞淋巴瘤成人患者。
通过优先审评审批程序附条件批准格林格申报的1类创新药宗艾替尼片(商品名:圣赫途),单药适用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
10月13日,通过优先审评审批程序批准赣州和美药业的1类创新药莫米司特片上市,该药适用于治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者。
10月17日,杭州中美华东的1类创新药瑞玛比嗪,注射用外源性荧光示踪剂,需与美德康公司的经皮肾小球滤过率测量设备(TGFR)配合使用,评估患者的肾小球滤过率(GFR)。
四川科伦博泰生物的注射用博度曲妥珠单抗(商品名:舒泰莱)上市,用于既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
10月28日,杭州中美华东的1类创新药马来酸美凡厄替尼片(商品名:迈瑞东)上市,适用于具有表皮生长因子受体(EGFR)外显子21(L858R)置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的一线治疗。
勃林格的1类创新药那米司特片(商品名:博优维)上市,适用于治疗特发性肺纤维化(IPF)成人患者。
10月30日,通过优先审评审批程序附条件批准乐普的注射用维贝柯妥塔单抗(商品名:美佑恒)上市,适用于治疗既往经至少二线系统化疗和PD-1/PD-L1抑制剂治疗失败的复发/转移性鼻咽癌的成人患者。
11月5日,浙江艾森的1类创新药奥格特韦钠胶囊上市,用于治疗轻中型新型冠状病毒感染(COVID-19)的成年患者。
11月7日,通过优先审评审批程序附条件批准重庆精准生物的普基奥仑赛(商品名:普利得凯)上市,用于治疗3至21岁CD19阳性的难治或复发(首次缓解12H后复发需经挽救化疗)的急性B淋巴细胞白血病患者。
预计到明年关门,至少40多个创新药纳入队伍中。创新药获批真的是到了收割期,同仁们,抓紧时间做功课哈。
参考来源:
[1] NMPA/CDE官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
2. 重磅!《优化创新药临床试验审评审批试点工作方案》正式发布
3. 值得收藏:审评制度改革以来,NMPA批准的自主创新药汇总
4. 第三款NMOSD创新药!罗氏IL-6R单抗Enspryng获美国FDA批准
5. 中秋佳节拒绝“甜蜜陷阱”,全球三款创新药物带来糖尿病治疗新希望
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论