

摘要
大多数药物,需要频繁给药的短效制剂,这可能会对患者依从性产生负面影响,并增加不一致使用相关的失效风险。相比之下,长效缓释制剂,可以实现数周、数月或数年的药物持续释放。我们讨论了已获美国食品和药物管理局,FDA批准的至少1个月缓释并长效药物控释制剂,重点是其制剂中使用的新材料。不同的缓释机制,包括基于溶解的、基于生物降解的(预成型和原位成型)、不可降解的植入式和基于水凝胶的制剂,并探究了长效药物递送制剂的临床应用,包括长效避孕药、延长性激素抑制、阿片类药物和酒精成瘾治疗以及眼部局部药物递送。最后,总结了63种FDA批准的长效药物产品释放机制、给药持续时间、药物形式、给药途径、适应症、制造商和非活性成分。最后,展望了长效给药制剂未来的挑战和机遇。
1.简介
从避孕激素和抗炎剂等小分子到肽和抗体等生物大分子,医学中使用了多种药物分子。这些药物分子通常被称为活性药物成分。活性药物成分被纳入特定的药物递送制剂(即剂型)中,其中包括药物进入身体的途径。制剂还必须考虑治疗靶点(即药物作用部位的细胞或组织),以及药物在体内的物理化学特性和活性。用于长期治疗的药物通常需要频繁给药(即每天一次或多次),这可能是患者的负担和有效治疗的障碍。此外,药物可能需要进入身体难以到达的部位,例如关节、子宫、眼后部或鼻窦。这使得长效局部治疗具有更重要的意义。
长效给药制剂可以在数天、数周、数月甚至数年的过程中单次给药后缓慢释放药物,并且可以保持稳定的药代动力学特征。通常,药物输送速率的设计与药物从体内代谢的速率密切相关,以在血液或组织中的目标治疗浓度下保持稳定状态。长效药物递送制剂粒径太大而无法注射甚至无法植入,载药量低。这种情况意味着,随着所需药物给药率的增加,药物输送的最长持续时间会减少。对于通过排泄或新陈代谢,更快地从体内清除的药物,药物给药率更高。由于剂型中的药物不稳定性或体内新陈代谢等因素,低药物生物利用度(用于衡量体内给药后进入全身血流的药物比例)也会增加所需的药物释放率在到达体循环之前(例如,在注射部位)。所需的总剂量可以估计为给药速率和给药持续时间的乘积。对于某些药物,例如口服抗生素,剂量太高,由于需要大剂量体积,长期肠外给药是不切实际的。长效释放最适合在体内具有长半衰期(如数小时或数天)的强效药物。
长效给药制剂可以克服许多阻碍药物治疗成功的障碍。当通过口服、经皮或肺部途径递送时,肽和蛋白质药物通常具有低或可变的生物利用度,需要注射这些生物大分子。除单克隆抗体外,大多数蛋白质和肽类药物在血液中的半衰期较短,因此需要频繁注射,通常每天或每周多次注射,使患者依从性差和舒适度差。长效给药制剂可以显着降低注射频率;例如,接受6个月Lupron Depot治疗的前列腺癌患者,一年仅需两次注射,而不是每年365次注射。长效药物递送可以维持体内药物水平稳定,保持最低治疗血浆浓度和安全阈值浓度的之间,来提高药物功效和安全性。
与精神疾病或药物滥用作斗争的人经常在药物依从性方面遇到困难,这可能会产生毁灭性的影响:例如,利培酮治疗精神分裂症或纳曲酮治疗酒精依赖。在资源匮乏的环境中,依从性差也是一个问题,获得医疗保健的机会可能有限:例如,在非洲许多地区,不坚持加强疫苗接种是新生儿死于疫苗可预防疾病(如破伤风)的主要原因。其他药物,例如HIV疗法,需要高给药频率(例如每天四次);有效的药物治疗经常受到(经常)漏服的阻碍。同样,坚持每日口服避孕药可能忘记,但是这可以通过长效释放制剂来解决。
对于必须到达身体特定区域(例如口腔、关节、眼睛或大脑)的药物来说,长效局部治疗尤为重要。例如,眼内植入物可用于治疗眼部炎症;关节内注射以缓解关节疼痛;用于缓慢释放避孕激素的宫内和阴道装置;心脏支架涂层,以防止再狭窄,用于治疗冠状动脉疾病。此外,局部给药可以减轻药物引起的全身副作用和增加作用部位的治疗效果。在这些地区可能需要连续数月至数年的药物治疗,重复给药通常是不切实际或不可能的。
2.长效给药制剂
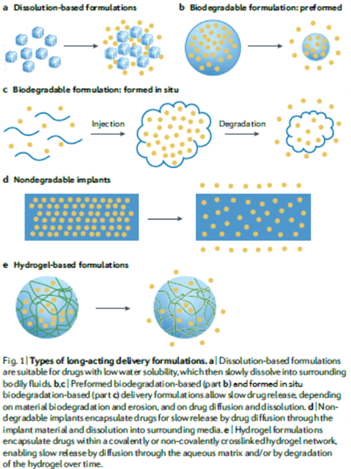
大多数长效给药制剂的设计基于溶解制剂、预制或原位可生物降解系统、不可降解植入物或水凝胶(图1,2)。水溶性低的药物可以加入到基于溶解的制剂中,该制剂在配制时不需要额外的赋形剂来控制药物释放。制剂在数周或数月内缓慢溶解,从而在作为药物悬浮液给药后释放药物。水溶性不够低的药物可以通过化学修饰形成不良在产生药物混悬液之前可溶解、可裂解的前药,或者它们可以与亲脂性抗衡离子结合以降低整体药物溶解度。药物可以被包埋(或微囊化)在可生物降解的聚合物中,因此药物释放受药物通过聚合物基质的扩散、聚合物基质的生物降解和侵蚀、聚合物溶胀和渗透诱导事件控制,或者在某些情况下,通过与聚合物基质的组分结合或聚合物链迁移以修复,先前打开的封闭孔。这种可生物降解的制剂可以预先形成,例如作为悬浮液注射的载药微粒,或通过注射后在体内硬化而原位形成。不可降解制剂通常是宏观尺寸的植入物,可以在使用后去除。植入物可以适应高载药量并促进药物释放机制,从而延长给药时间。这些制剂通常通过药物扩散通过聚合物基质来控制释放。最后,基于水凝胶的制剂是基于水的系统,它有利于药物稳定性和生物相容性。
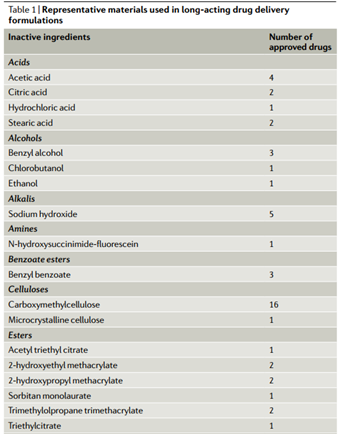
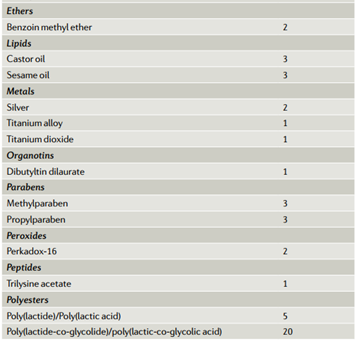
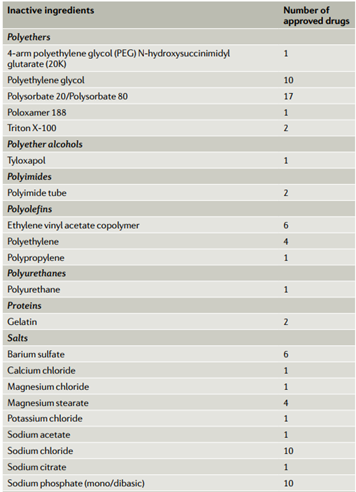
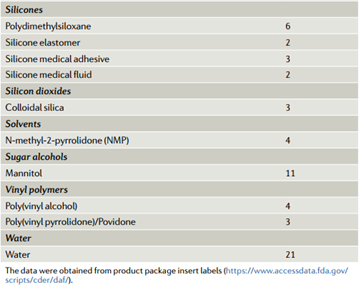
我们发现了60多种用于长效给药制剂的不同材料,最常见的是盐、聚醚、聚酯、水、纤维素、有机硅、聚烯烃、糖醇、酯和酸或碱(表1)。为了控制药物释放,生物可降解制剂通常使用丙交酯和乙交酯(PLG) 的聚酯共聚物,一些使用乳酸和乙醇酸共聚物(聚乳酸-乙醇酸共聚物(PLGA))或聚丙交酯的均聚物)或聚乳酸(PLA);不可生物降解的配方包含聚(乙烯-醋酸乙烯酯)(EVA)、有机硅、聚乙烯和其他聚合物。制剂中存在的其他赋形剂可以通过增加粘度和表面活性剂活性、缓冲pH值和控制渗透压来稳定悬浮液、提供机械强度、实现体内成像和控制其他特性。
2.1基于溶解的长效制剂
用于递送难溶性药物的基于溶解的药物递送制剂作为药物颗粒的悬浮液注射,该悬浮液精细分散在水性或油性载体中。药物粒径可能从纳米到数百微米不等;由于其较小的表面积与体积比,较大的颗粒通常释放药物更慢。注射的颗粒通常保留在给药位置,在那里它们可能被吞噬细胞内化。然后药物通过缓慢溶解释放,允许局部治疗作用或全身吸收。与通常具有较低载药量的赋形剂控制的长效制剂相比,药物混悬剂递送还允许施用高药物剂量。此外,药物的化学稳定性可以通过混悬剂提高,因为药物制剂在释放到体内之前一直保持固态。
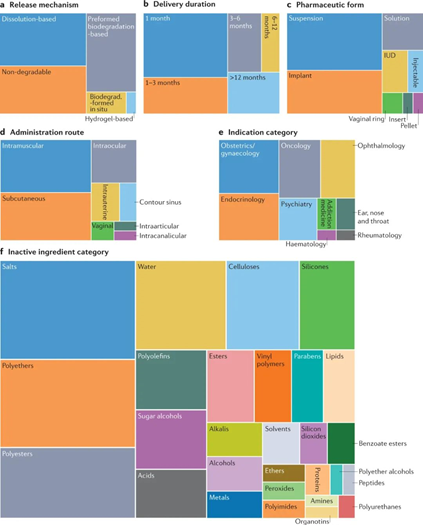
图2 FDA批准的长效给药产品的特点
基于溶解的长效混悬剂由润湿剂、反絮凝剂、粘度增强剂、缓冲液、渗透剂和液态载体组成。润湿剂使混悬粒子分散于液体介质中;反絮凝剂中和混悬粒子表面电荷,弱化范德华力以利于絮凝粒子再分散;粘度增加剂可以降低混悬粒子的沉降速率;缓冲液用于维持介质的pH值在7.0~8.4范围内;渗透剂使介质产生渗透压与生理环境保持等渗。
2.1.1基于溶解的长效制剂产品
目前FDA已经批准21种基于溶解的长效制剂,大部分产品是每月给药一次,部分2至3月给药一次,另有两个制剂为每6个月给药一次。这些基于溶解的长效制剂大部分为肌肉注射,部位为皮下注射或者眼内给药。
基于溶解的第一个药物递送系统是1953年由Endo Pharmaceuticals公司开发用于治疗性腺功能衰退的庚酸睾酮,1954,Par Pharmaceutical公司开发了戊酸雌二醇。1972年以后,基于溶解的长效药物递送制剂被广泛开发,大部分被用于治疗精神分裂症、内分泌、肿瘤、眼科疾病以及避孕。Mylan公司的氟奋乃静是基于溶解的长效制剂家族第一个用于治疗精神分裂症的药物,于1974年上市,给药频率为每月注射一次,之后才有六种同类药物上市,包括Janssen公司3个月注射一次的棕榈酸帕利哌酮。
三个月肌肉注射一次的醋酸甲羟孕酮冻干粉注射剂在临床和商业化上取得的巨大成功,促就了另外两款长效避孕药:Pfizer公司的醋酸甲羟孕酮和Upjohn公司的雌孕激素注射剂(Lunelle)。宫内铜释放设备被认为是活性成分为铜的基于溶解的长效递送装置,尽管FDA只批准一款产品(CooperSurgical公司的子宫环Paragard)上市,但之前使用过很多类似产品,并且在很多其他的国家或地区依然在使用。
2.2预制的可生物降解制剂
预制的可生物降解制剂是将药物包载于生物可降解材料中实现药物缓释的长效制剂。溶解性很高的活性药物很难开发成药物混悬液,加入能控制药物释放速率的赋形剂是实现药物长效递送主要方法。最常见是将药物包载于可生物降解聚合物基质中,聚合物基质能减缓药物释放速率,并在药物释放的过程中维持药物稳定。用于这类长效制剂的聚合物通常不溶于水,在水解或者酶促过程作用下能降解为水溶性并能从体内排出的无毒化合物。可生物降解预成型制剂通常以微粒或者毫米级直径的圆柱形植入物形式注射引入,在几个月的时间内随着聚合物缓慢降解而释放包载的活性药物。
常用于可生物降解预成型制剂的聚合物有PLG、PLGA、PLA 或聚丙交酯。结晶度高的聚合物很少用于这类制剂,因为结晶度高的聚合物溶解度和可变率较差,比非结晶材料的降解速率慢。而共聚物因可以通过改变单体单元实现对材料理化性质的控制,使其有更高的吸引力。除了合成聚合物,天然聚合物因来源广泛和生物相容性高,很早便用于药物开发,但因为天然聚合物材料的理化性质太过复杂,水溶性较差,分子量分布较宽,在使用上受到诸多限制。
其他可生物降解的聚合物,例如聚己内酯(PCL),降解速度甚至比聚(丙交酯)更慢。基于其高疏水性和快速水解性(与PLG和聚(丙交酯)的本体侵蚀相反),可以设计聚酐以通过表面侵蚀控制药物释放。聚(氰基丙烯酸烷基酯)、聚原酸酯、聚酰胺、聚酯酰胺、聚磷酸酯和PEG也可用于控释。使用可生物降解聚合物的优点是使用后不必去除递送剂型;然而,聚合物降解产物必须对封装的药物无毒且无损伤。值得注意的是,PLGs和PLGAs会迅速产生羧酸副产物,这些副产物会降低制剂和周围介质中的局部pH值,这会损坏酸敏感的封装药物,尤其是蛋白质。
除了合成聚合物之外,天然可降解聚合物也可用于制造基于生物降解的制剂,例如基于蛋白质的聚合物,胶原蛋白、白蛋白和明胶,以及多糖,例如琼脂糖、藻酸盐、角叉菜胶、透明质酸、葡聚糖,壳聚糖和环糊精。天然可降解材料长期以来一直用于医学,并且由于其丰富性和生物相容性而被广泛应用于药物。然而,天然可降解聚合物通常具有较宽的分子量分布。此外,如果没有额外的合成方法,它们的分子量分布无法调整,这会限制它们实现精确、受控的药物释放的能力。材料也会因批次而异,因此,合成聚合物更常用于制造长效药物递送制剂。
2.2.1预制的可生物降解制剂产品
目前,FDA已批准22种基于可生物降解材料开发的长效药物递送制剂,其中18种为预成型长效制剂,4种为在体内原位成型长效制剂。丙交酯乙交酯聚酯共聚物(PLG)、聚丙交酯、聚乳酸-羟基乙酸共聚物(PLGA)和聚乳酸(PLA)等是最常用的可生物降解预成型长效药物递送制剂的材料,作为关键辅料用于控制药物释放速率。这些产品中大部分是混悬注射剂,另有部分是植入剂,其中有一半是肌肉注入,其余的通过皮下或者其他部位局部给药。大部分产品的缓释时间为一个月,少数几个产品可实现长达6个月的缓释。
曲普瑞林微球是1986年在欧洲上市的首款长效药物递送制剂,之后又陆续上市了戈舍瑞林植入剂和亮丙瑞林微球。自此以后,可生物降解预成型制剂广泛应用于内分泌和肿瘤领域,各类产品稳步推出。
每月给药一次的纳曲酮微球为一种治疗阿片成瘾的可生物降解预成型制剂,它的出现为后续的丁丙诺啡植入剂和预充注射器给药的丁丙诺啡注射剂提出了新的药物递送机制。而地塞米松不仅有以可生物降解的PLG控制药物释放的玻璃体内植入剂,还有地塞米松眼内混悬液和地塞米松水凝胶缓释泪点塞。2019年,阿非糖苷皮下植入剂获FDA批准上市,成为全球首个用于红细胞生成性原卟啉症(EPP)患者提供系统性光保护作用以预防光毒性的药物。阿非糖苷皮下植入物中的药物不仅可以持续释放2个月,并且最快在2天内就开始释放药物,比其他植入剂释放药物的时间要短很多。
2.3原位形成的可生物降解制剂
与预先形成的制剂相比,原位形成的基于生物降解的制剂通常能够更容易地施用和更简单地制造。使用注射器将原位形成的制剂以液体形式注射,以在给药部位形成(半)固体贮库。所得的可生物降解基质在聚合物分子量下降和聚合物在体内最终侵蚀后,会在数周或数月内缓慢释放药物。与预制制剂相比,原位形成的制剂更容易制造,因为它们通常涉及液体溶液或悬浮液,无需形成(通常是干燥)颗粒或制造植入物。然而,原位制剂的缺点是有机溶剂与活性药物成分和聚合物赋形剂一起注射到体内;因此,需要考虑安全暴露限值,及其增加的毒性和副作用。此外,由于有机溶剂快速释放到组织中,注射会引起灼烧感。
可生物降解原位成型制剂常用的聚合物材料与预成型制剂类似,可以通过改造聚合物材料降低药物初始阶段的突释和实现所需的药物释放过程。提高聚合物的浓度和增加分子量可以提高聚合物溶液粘度,可以延长药物释放,但是粘度升高会增加注射的难度,甚至需要更粗的针头和注射器,造成强烈的疼痛降低顺应性。目前常用的方法是将原位成型制剂与黏性乳液或者低粘度油联合使用,改善依从性。
原位成型制剂的动力学与溶剂和聚合物特性有关,聚合物在水溶性高的有机溶剂中会快速沉淀,形成多孔基质的棒状药物储库;疏水性较强的有机溶剂则会减缓聚合物沉淀,最终形成孔径较少的球形药物储库。通过共溶剂调节药物储库形成的速率,可以避免药物在初始阶段发生突释。
2.3.1原位形成的可生物降解制剂产品
FDA已批准的22种可生物降解长效药物递送制剂中,只有4种为原位成型制剂。这些产品将PLG溶于N-甲基吡咯烷酮中,以溶液或混悬剂形式皮下注射给药形成储库,缓慢释放1月到6月。首款原位成型制剂是基于Atrigel药物递送系统的醋酸亮丙瑞林注射粉末/预填充注射器,于2002年获批上市,用于长效治疗前列腺癌。该产品由两支独立的预充式注射器组成,一支为活性成分即醋酸亮丙瑞林粉末,另一支为复溶用的 Atrigel 系统,两者充分混合后,在30 分钟内以液体形式皮下注射,固化后连续释放预定剂量的醋酸亮丙瑞林。
2.4不可降解植入物
与具有生物吸收优势的生物可降解递送制剂相比,不可降解植入物(每次给药一个或几个宏观装置)能够实现更长时期的受控药物释放,长达数年。然而,这些装置要么终生留在体内,要么需要在使用后通过小型外科手术移除。药物释放植入物可以通过注射或插入(例如,皮下、眼睛中)、手术放置(例如,动脉内)或其他程序(例如,子宫内或阴道放置)来施用。
相比于可注射的可生物降解制剂,植入剂既可以是简单的又可以很复杂的宏观装置,载药量更高,药物缓释时间更长。不可降解植入剂在设计上类似于可生物降解制剂,同样是将药物均匀分散于聚合物基质中,药物经扩散作用缓慢释放。这样的聚合物基质生产较为容易,但因为植入后有一定突释通常无法稳定地实现零级释放动力学。植入剂的表面通常会包裹一层聚合物膜外壳,用于减缓药物扩散和释放。聚合物膜厚度,植入剂表面积、药物溶解性、聚合物和水分配系数、药物在聚合物中的有效扩散率以及一些其他因素共同决定了药物的释放速率。
各种不可降解的生物相容性聚合物已用于制备植入剂,包括有机硅、聚乙烯醇(PVA)、乙烯-醋酸乙烯共聚物(EVA)和聚甲基丙烯酸甲酯(PMMA)。除不可降解的聚合物材料,金属材料也是植入剂的常用材料,例如钛、铜。最经典的设计是将药物装载于金属制备的棒状植入剂中,以带孔的盖子控制药物缓释。另有一种设计是以水溶性材料为渗透剂,中间用活塞隔开渗透剂和药物,植入后身体里的生理介质通过植入剂表面的渗透膜进入溶解水溶性材料,形成的渗透压推动活塞释放药物,药物的递送速率取决于渗透膜对生理介质的渗透性,稳定药物释放速率可以实现长达一年的药物缓释。
近几年开发了再填充植入剂,通常是在植入剂的表面有能够以针刺穿的隔膜,通过注射器对植入剂进行药物再填充。此外,还有通过无线控制机械泵调节药物释放速率的植入剂,可以实现精准按需给药。
2.4.1不可降解植入物的产品
目前FDA 已批准 19 种不可降解植入剂用于长效药物递送,其中11种为棒状植入剂,8种为宫内节育器(Intra-UterineDevice,IUD)、阴道环或支架。19种产品中,16种产品的递送效期不短于1年,一半产品的递送效期不短于3年,有1种产品的递送效期超过6年。这19种产品分别采用橡胶硅、聚乙烯类、乙烯-醋酸乙烯共聚物(EVA)和聚甲基丙烯酸甲酯(PMMA)控制药物释放速率,聚酰亚胺、金属钛、硫酸钡、银、硬脂酸镁、硅胶等也常作为不可降解植入剂的材料。
已批准的不可降解植入剂中,一半产品的给药方式是皮下注射、皮下腔注射或者玻璃体内注射,超过三分之一的产品是如节育器或阴道环这类女性生殖道植入剂。一半产品用于避孕,其余的适应症涉及眼科、肿瘤学、内分泌学、心脏病学和成瘾医学。
第一个不可降解的药物递送系统是1976年上市的一款释放黄体酮的节育器(Progestasert,Alza)。此后,不可降解皮下植入剂大量开发,其中基于聚二甲基硅氧烷(PDMS)制备两款左炔诺孕酮埋植剂,包括Wyeth-Ayerst公司的Norplant和Bayer公司的Jadelle。Chiron Vision公司基于EVA制备的更昔洛韦植入剂Vitrasert在眼科领域用于治疗巨细胞病毒视网膜。另有Bayer公司的三款释放黄体酮和左炔孕诺酮的宫内节育器Mirena、Skyla和Kyleena。阴道环有Merck公司的Nuvaring和Population Council公司的Annovera,同时释放雌激素和黄体酮。Alza在2000年上市了以渗透泵为动力的在1年内缓慢释放醋酸亮丙瑞林的的金属植入剂Viadur,用于治疗晚期前列腺癌。
2.5基于水凝胶的制剂
基于水凝胶的制剂包含在水溶液中形成交联网络的亲水性聚合物。水凝胶含有很大一部分水,可以输送亲水性小分子、大分子药物和细胞。基于水凝胶的制剂通常由可生物降解的聚合物制成,或者是从体内自然清除而不会降解的聚合物。与可生物降解的配方相比,水凝胶具有亲水性并具有出色的吸水能力。水凝胶递送制剂特别适用于不稳定的药物,例如蛋白质和肽,它们在暴露于有机溶剂、热、干燥和与它们掺入聚合物制剂相关的加工条件时容易变性。药物可以通过扩散、网络降解、溶胀、机械变形和/或聚合物-药物相互作用的变化(例如共价共轭、静电相互作用和疏水缔合)逐渐从水凝胶中释放出来。药物释放特性可以通过改变凝胶的化学成分或交联的程度和类型来调整。与由疏水性聚合物组成的制剂相比,水凝胶的亲水性和高含水量通常会导致相对快速的药物释放。这些亲水特性通常使将疏水药物包封在水凝胶中具有挑战性。
相比于可生物降解聚合物制剂和植入剂,可注射水凝胶制剂给药时创伤性很小,患者有更好的耐受性和更高的接受度。水凝胶既可以是预成型制剂,也可以是给药后在原位交联成型,还可以通过体内的温度、pH值、离子或者其他条件实现溶液-凝胶环境响应性相转变。凝胶在注射时可以是溶液、可流动凝胶或可压缩性微孔凝胶,给药后在给药部位形成或者恢复其交联网格结构,用于体内缓慢持续释放药物。
用于制备水凝胶的天然材料包括蛋白质(如纤维蛋白、胶原蛋白和明胶)、多肽和多糖(如壳聚糖、藻酸盐、透明质酸和葡聚糖),这些材料具有生物相容性、可生物降解性和来源广泛性。而合成的聚合物则具有明确的结构和可调节的功能性,尤其是PEG和PVA,因低毒性、吸水特性和较高的机械强度而广泛用于制备水凝胶。单体聚合物也用于水凝胶的制备,例如甲基丙烯酸羟乙酯、甲基丙烯酸羟丙酯、聚乙烯吡咯烷酮、异丙基丙烯酰胺、醋酸乙烯酯、丙烯酸、甲基丙烯酸等等。
水凝胶的网格结构可以通过聚合物自组装、与交联剂化学共价交联、以氢键或者静电作用物理非共价交联形成。药物的包载方法有很多种:在孵育过程中随着凝胶溶胀被动包载;在凝胶化前与凝胶前驱体溶液均匀混合包载;在凝胶形成过程中与聚合物化学共价连接包载。为获得长效水凝胶制剂,药物分子必须要先包载到聚合物的网格中,通过高密度交联来降低聚合物链之间的间距,这可以减缓药物从凝胶基质中的扩散速率。水凝胶制剂释放药物的机制主要依靠聚合物的降解和侵蚀作用,可以持续释放药物数周至数月。凝胶的初始粒径必须要足够小才能固定药物分子,在水解或酶的介导下,随着网格结构降解或者化学键断裂而逐渐增大。小于网格孔径的药物分子会因为药物的转运而快速释放,而大粒径的分子则滞留在凝胶中。
2.5.1基于水凝胶的制剂产品
迄今为止,只有一种使用基于水凝胶的长效递送制剂的产品 Dextenza获得了FDA的批准。该产品于2018年获得批准,由基于PEG的水凝胶制成,该水凝胶含有醋酸三赖氨酸和用于可视化的荧光素、缓冲盐和水。这种基于水凝胶的系统被植入管内(进入眼点)并释放地塞米松1个月,以治疗眼科手术后的眼部炎症和疼痛。仅一种基于水凝胶的产品已获批准这一事实表明,由于水凝胶制剂的高含水量和孔隙率,该技术用于实现长效给药具有一定的挑战。
3.局部长效给药制剂
上述FDA批准的长效药物制剂中,绝大部分的产品都是为全身给药而设计的,为最大限度地提高局部药物浓度和减少脱靶效应发生的几率,进一步提高产品疗效和安全性,约有30%的产品开发为局部给药长效制剂。在FDA批准的长效药物制剂中,47%的给药方式为眼内给药,其中一款为管内给药,26%的产品用于女性宫内避孕给药,其余的产品被用于轮廓窦或关节给药。这些产品的释放机制包括不可生物降解制剂(47%)、可生物降解预成型制剂(32%)、基于溶解的制剂(16%)和一款水凝胶制剂。
3.1生物吸收短于1月的制剂
根据临床需求,很多长效制剂的释药周期短于1个月。例如,米诺环素微球注射剂在三周内从PLG基质中缓慢释放米诺环素;原位成型的多西环素注射剂在一周内从聚乳酸中缓慢释放多西环素,这两种产品都是牙周袋局部给药用于治疗牙周炎。
其他生物吸收短于一个月的产品包括兰瑞肽注射液SomatulineLA(PLG微粒,两周制剂)、格拉司琼缓释注射剂Sustol(TEG-聚原酸酯半固体药丸、七天内制剂)、利培酮注射用粉末和溶剂RisperidoneConsta(PLG微球、两周制剂)、卡莫司汀植入膜剂Gliadel(聚酸酐薄膜,两到三周制剂)及其他。
3.2药物递送与药物作用时间
药物作用时间和药物从特定剂型中递送的持续时间是完全不同的。例如,短期药物递送可以因较长的药效学作用而实现持久的药理作用,提高给药剂量,在很长时间内将药物浓度维持在最低治疗水平以上。例如阿非糖苷皮下植入物(Scenesse,PLGA植入剂),会在几天内释放大量药物,但是药效可持续2个月。类似的,生物制剂抗血管内皮生长因子以高剂量注射到眼睛玻璃体内,注射后药物快速释放,用于治疗眼睛湿性年龄相关性黄斑变性,药物的清除率很低,可以在1到3个月内维持有效的药物浓度。
药物释放的周期通常要超过给药间隔,但是给药前期和后期很难将药物浓度维持在有效范围内,通常是以提高给药频次来解决这个问题,保持恒定的药物剂量。例如艾塞那肽微球Zaffaroni,给药频率为每周一次,但药物可以从PLG基质中持续释放70天,这种策略可以有效解决药物突释和降低毒副作用。类似的案例还有奥氮平注射用缓释悬浮液。
3.3长效药物医疗器械
医疗器械可以包载药物实现长效递送。在此类药物器械组合中,医疗器械是实现预期治疗效果的关键,包载的活性药物反而在其次。医疗器械的表面作为生理环境和植入装置的界面,对产品的体内融合度至关重要。但在医疗器械中易发生细菌感染,以生物膜的形式对抗治疗性的抗生素产生耐药性。
局部给药的最大优势是控制药物释放,例如Resolute Onyx支架用于治疗冠状动脉疾病,由高密度的铂铱核和外层钴铬层组成,还包括C9聚合物、C10聚合物和PVP,该不可降解的递送装置能实现对唑托莫司的持续缓释达一年。类似的药物洗脱装置也可采用可生物降解材料做成预成型制剂,例如聚乳酸和PLG。药物洗脱装置也适用于骨科、肺部、泌尿科和其他适应症,很多器械的释放周期不到一个月。医疗器械中的药物通常是包载在不可生物降解或可生物降解的聚合物基质中,药物通过扩散作用和聚合物侵蚀或降解实现缓慢释放。
3.4长效药物制剂的案例
FDA批准的第一个激素宫内节育器是Progestasert ,虽然已经停产,但它为后续批准的四款激素宫内节育器的设计提供了基础,分别是Mirena、Kyleena(Schering AG)、Liletta(Medicines360)和 Skyla(Bayer)。这些宫内节育器由一个T形聚乙烯框架和一个由聚二甲基硅氧烷(PDMS)制成的非生物可降解药物储层组成并包裹聚二甲基硅氧烷外壳,药物缓慢释放长达六年。
Depo-Provera(Upjohn)是一种长效避孕针剂,每3个月肌肉注射一次。该产品为药物混悬液,活性药物醋酸甲羟孕酮的颗粒悬浮在含有聚乙二醇、聚山梨酸酯、尼泊金甲酯、尼泊金丙酯和氯化钠的载体中。使用前轻轻摇晃产品,以确保药物颗粒均匀悬浮。注射后,醋酸甲羟孕酮颗粒在注射部位形成药物储库,醋酸甲羟孕酮的水溶性较差,在溶解作用下缓慢释放药物。
Norplant 是第一款避孕植入剂,于1990年获批上市,但因为疗效问题现已停产,并推出了改进后的新产品。该植入剂由6个柔性封闭包载左炔诺孕酮的胶囊组成,胶囊的材质是硅橡胶。皮下植入后,该植入剂能持续释放左炔诺孕酮至少5年。依托孕烯植入剂Nexplanon是美国目前唯一还在使用的避孕植入剂,以EVA为基质包载依托孕烯。该产品还含有用于放射成像的硫酸钡。Nexplanon置于皮肤下,可提供长达3年的持续避孕。这些避孕植入物是不可降解的,必须取出。
3.5长期抑制雄激素
激素依赖性前列腺癌和其他适应症可以通过长期使用LHRH激动剂(例如亮丙瑞林)来控制睾酮用于长期治疗。亮丙瑞林最早是皮下给药的速释制剂,然后由于其半衰期仅有3个小时,必须要在数年内每日给药。每日注射带来的不便促进了三款亮丙瑞林长效制剂的开发。
Lupron Depot是以PLG或聚乳酸为材料的预成型可生物降解微粒,肌肉注射后和缓释亮丙瑞林1、3、4或6个月。包载亮丙瑞林的干燥微粒储存在小瓶中或在预充好的双腔注射器中,水性稀释溶液中含CMC、甘露醇、吐温80和冰醋酸,分别用于增加粘度、等渗、乳化和调节酸碱度。
Eligard 是一种生物可降解原位成型制剂,醋酸亮丙瑞林可从聚合物基质中缓慢释放1到6个月。冻干的醋酸亮丙瑞林混悬在溶解PLG的甲基吡咯烷酮(NMP)溶液中,使用前将两支装产品混合,皮下给药。甲基吡咯烷酮缓慢扩散至水性生理环境中,使PLG沉淀形成大量固体,包载的亮丙瑞林用于缓慢释放。
Viadur是一款不可降解的植入剂,因生产成本昂贵已不再销售。该产品是4mm×45mm的钛合金药物储层,里面装载由DMSO溶解的醋酸亮丙瑞林,需要小型外科手术将其皮下植入。Viadur使用渗透泵机制,在一年内稳定地释放醋酸亮丙瑞林。渗透泵由氯化钠、CMC、PVA、硬脂酸镁和水组成,组织间液缓慢地通过聚氨酯膜渗入,渗透泵吸收水分后经活塞缓慢扩散药物。
3.6阿片药物和酒精成瘾
全球约有20亿人患有酒精使用障碍,1600万人患有阿片类药物使用障碍。两者都是慢性疾病,经常反复发作。阿片成瘾可以用阿片受体激动剂治疗,如美沙酮和丁丙诺啡;或可使用阿片受体拮抗剂,如纳曲酮治疗。这些药物通常需要每天使用,存在因差异化使用而引起的治疗失败的风险。长效药物可以有效改善患者依从性,同时减轻患者和医生的治疗负担。目前有三款长效缓释产品用于这类慢性疾病的治疗。
Probuphine 是FDA批准的一种长效丁丙诺啡产品,用于阿片类药物依赖的维持治疗,但已在美国停产。该产品是一款皮下植入剂,由不可降解的EVA基质组成,可在6个月内持续提供低剂量的丁丙诺啡。该植入剂由4根可弯曲的圆柱形杆组成,需要专业人员进行植入。
Sublocade是一款丁丙诺啡缓释制剂,用于治疗中至重度阿片类药物使用障碍。该产品是一款可生物降解的原位成型制剂,由溶解于甲基吡咯烷酮PLG和丁丙诺啡组成,每月注射一次。注射后形成固体凝胶药物储库,随着PLG聚合物缓慢降解而释放丁丙诺啡。
Vivitrol是FDA批准的酒精中毒和阿片类药物成瘾的长期治疗药物,为可生物降解预成型纳曲酮微粒制剂,每月肌肉注射一次。纳曲酮微粒由PLGA组成,水性混悬液包含CMC、聚山梨醇酯20和氯化钠。注射后,在聚合物降解和侵蚀的过程中,纳曲酮通过扩散作用和内部渗透压的作用下缓慢施杨药物。
3.7眼科局部递送
一些眼部疾病可以通过长效药物递送技术进行治疗,这些技术使药物能够局部递送到眼部。而以葡萄膜炎、湿性年龄相关性黄斑变性和黄斑水肿为例的视网膜疾病只能全身用药或局部玻璃体腔注射,不能通过局部滴眼液治疗。目前已有不可生物降解的医疗器械和可生物降解的制剂被批准用于玻璃体内注射。例如,Triesence是一种药物颗粒悬浮液,可以用曲安奈德治疗眼部炎症2至3个月。
不可吸收的产品也获得了FDA的批准,例如,Vitrasert是一种更昔洛韦6月长效制剂,用于治疗获得性免疫缺陷综合征(AIDS)相关巨细胞病毒视网膜炎,于1996年获批上市,由小丸(药物和硬脂酸镁)和控释膜(PVA和EVA)组成。类似的缓释药物储库设计也被应用于Reatisert和Iluvien,两者都为醋酸氟氢松制剂,前者为治疗葡萄膜炎的缓释30个月长效制剂,后者为治疗糖尿病性黄斑水肿的3年制剂。Iluvien是直径为0.37mm、长度为3.5mm的圆柱形植入剂,可以使用25号针头进行给药。药物包载于PVA基质中,再封装于不可生物吸收的聚酰亚胺管中,其中一端以PVA膜封闭,控制药物释放速率。类似的产品还有Yutiq,获FDA批准用于治疗慢性非传染性葡萄膜炎。
可吸收植入剂也被开发用于眼部疾病。例如Ozurdex是一款缓释6个月的PLG基质圆柱形地塞米松植入剂,用于治疗葡萄膜炎和糖尿病黄斑水肿。Durysta是一款缓释4个月的聚乳酸、PLG和PEG 3350的固体聚合物基质双马前列素植入剂,约为1mm,用于治疗青光眼药物。Dextenza为地塞米松缓释泪点塞,用于治疗术后眼部疼痛。
4.结论与展望
随着人们对长效药物递送制剂价值和需求的认识不断加深,以及关键性材料和药物递送系统的进步,自1953年上市的Delatestryl和Delestrogen两款长效制剂以来,大量的长效药物制剂在临床实践中稳步增长。在FDA批准的63款长效制剂中,大部分依然在临床中使用,仅有21% 已停产。
4.1长效药物制剂的递送机制
在长效药物制剂的递送机制方面,几乎所有的产品都属于基于不可降解、可生物降解预成型和基于溶解的释放机制。仅有6% 的产品是基于可生物降解原位成型释放机制,而水凝胶的药物释放仅有一款。约有39%的长效产品实现1个月的药物释放,其他分别有1到3个月长效(23%),3到6个月长效(14%)、6到12个月长效(7%)和1年以上长效(17%)。
4.2长效药物制剂的剂型
在长效药物制剂的剂型方面,混悬剂以40%比例位居第一,以可生物降解、预成型和基于溶解的制剂为主;植入剂以30%的比例位列第二,以可生物降解、不可生物降解和预成型制剂为主,植入剂最短缓释3个月,最长可达到6年。而在给药途径方面,肌肉注射、皮下注射和眼内给药是最常见的给药方式,占比分别为35%、32%和14%。
4.3长效药物制剂的适应症
在长效药物制剂的适应症方面,所有的产品中约有24%用于产科和妇科治疗,21%用于内分泌科治疗,18%用于肿瘤学治疗,15%用于眼科治疗,8%用于精神科治疗,4%用于瘾医学治疗,余下的部分用于耳鼻喉科、血液学和风湿病学治疗。长效药物制剂研发企业方面,有28家企业开发了1款长效制剂,14家企业开发了2款长效制剂,分别仅有1家公司开发了3款长效制剂(IntersectENT)和4款长效制剂(Bayer)。
4.4长效药物制剂的非活性辅料
在长效药物制剂的非活性辅料方面,最常用的辅料是盐(15%),多用于调节缓冲液的酸碱度和渗透压,改善产品稳定性或降低给药时的疼痛感;其次常用的是聚醚类辅料(13%),尤其是非离子型表面活性剂吐温80和聚乙二醇(PEG),用于改善疏水性粒子或者微球在水溶液中的分散度;第三常用的是聚酯类辅料(11%),例如PLG、PLGA、PLA等,作为可生物降解的聚合物基质用于控制药物释放;第四常用的辅料是水(9%),用于产品的混悬、增溶、复溶和注射;第五常用的辅料是纤维素(7%),尤其是羧甲基纤维素(CMC),用于增加产品粘度,提供粒子负电位改善混悬粒子的稳定性。其他的辅料还包括硅酮(5%)、聚烯烃(5%)、糖醇(5%)、酯类(4%)、金属(2%)、对羟基苯甲酯(3%)、酸(4%)、碱(2%)、聚乙烯类聚合物(3%)、二氧化硅(1%)和有机溶剂(1%)。
4.5展望
自1953年推出第一个长效给药制剂以来,控释给药在医疗实践中稳步增长。至少有63种长效药物产品已获得FDA批准,并能在1个月至6年甚至更长的时间内长期控释药物。这些递送制剂是定制的,使用各种控释机制、药物形式、给药途径和递送持续时间,专为特定适应症和患者群体而设计。超过60种不同的材料被用作长效给药制剂中的非活性成分。
综合市场信息可知,长效药物递送产品继续在患者护理中发挥重要作用,并且更多的产品正在开发中。这些制剂的技术挑战仍然是确定的剂量大小和释放持续的时间,其与药物效力和注射量有关。另一个挑战是蛋白质和其他生物制剂在微胶囊化和缓释过程中的物化稳定性管理。长效注射剂会继续增长,对全身给药和局部给药(例如眼部和关节给药)的关注度高,以及最近对支持免疫疗法的生物制剂和药物给药制剂的关注。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论