

随着PD-1抑制剂斯鲁利单抗于今年3月22日获得国家药监局批准上市,复宏汉霖(股票代码:2696.HK)正式启动向创新型生物制药公司的转型。在理清了斯鲁利单抗与美国FDA的监管路径后,复宏汉霖正在寻找合作伙伴,协同将中国制造的PD-1抑制剂推向美国市场,同时消除对公司主要生物仿制药特许经营权的担忧。同时,复宏汉霖和合作者Accord Healthcare计划在今年年底前向美国FDA提交复宏汉霖的罗氏赫赛汀生物类似药。
斯鲁利单抗批文信息
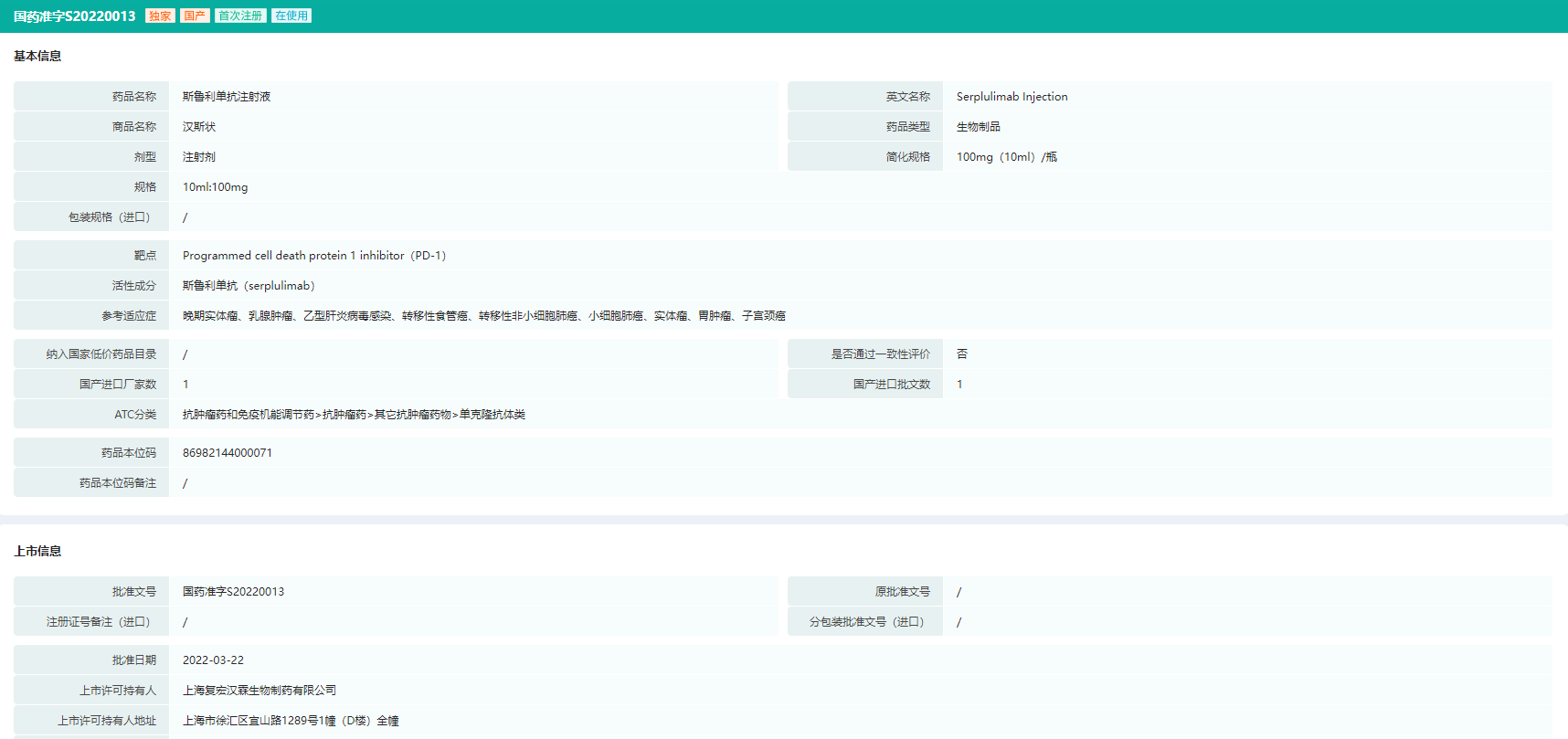
截图来源:药融云中国药品批文数据库
据药融云查询,斯鲁利单抗(汉斯状®)是中国批准的第13个PD-1 / L1抑制剂,是复宏汉霖首个创新型单抗H药,用于治疗微卫星高度不稳定(MSI-H)实体瘤,其鳞状非小细胞肺癌(sqNSCLC)、广泛期小细胞肺癌(ES-SCLC)和食管鳞状细胞癌(ESCC)适应症的上市注册申请也在审评中。
斯鲁利单抗适应症研发现状
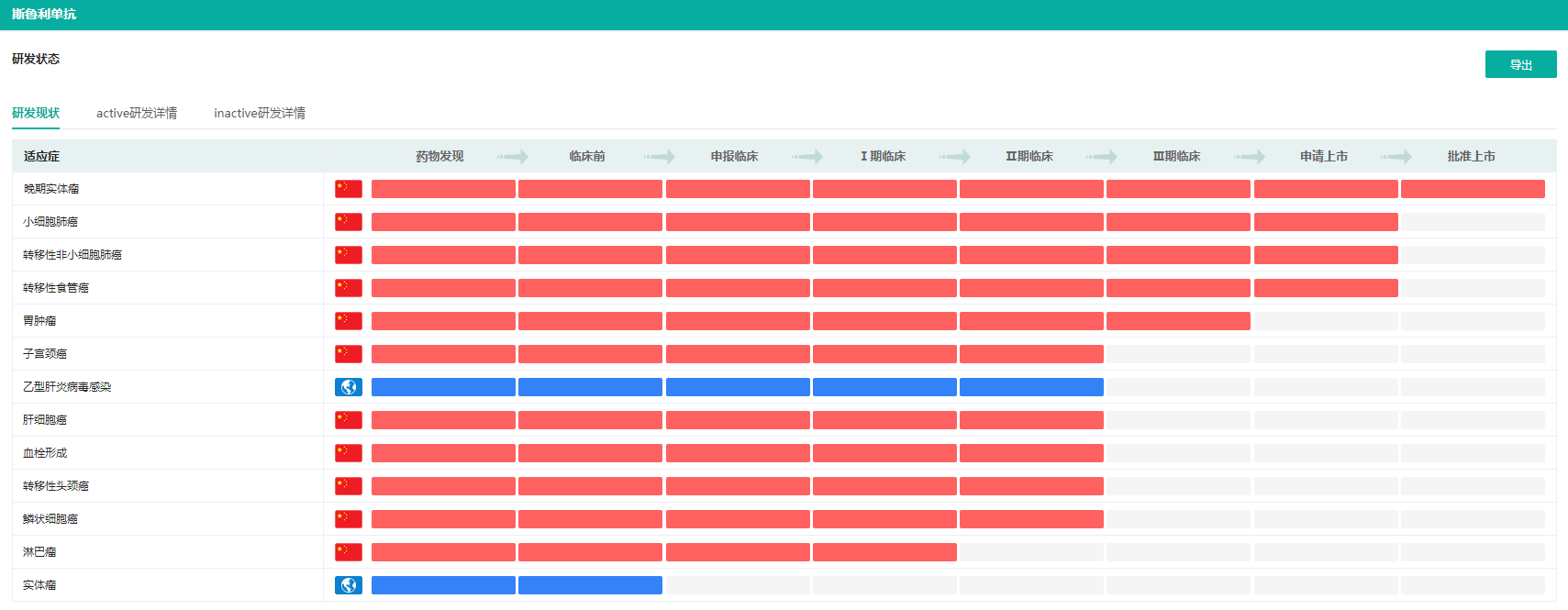
截图来源:药融云全球药物研发数据库
复宏汉霖董事长张文杰表示:“公司的目标是明年以整体市场份额进入中国五大PD-1 / L1抑制剂。”
在很大程度上,这一雄心壮志取决于新适应症的好消息:H药已于中国、土耳其、波兰、格鲁吉亚等国家和地区累计入组超3100人,其中2项国际多中心临床试验入组高加索人种的比例超过30%,是拥有国际临床数据较多的抗PD-1单抗之一。H药联合化疗一线治疗sqNSCLC,ES-SCLC和ESCC的NDA已获得NMPA受理,H药有望成为全球首个一线治疗SCLC的抗PD-1单抗。此外,斯鲁利单抗入选《2022 CSCO小细胞肺癌诊疗指南》作为ES-SCLC治疗推荐,其治疗小细胞肺癌(SCLC)也已获得美国FDA孤儿药资格认定。百时美施贵宝(BMS)因此前2次确认试验失败,在2020年底决定撤回OPDIVO ® (nivolumab,又称O药)在先前治疗的SCLC中的加速批准。默克公司于2021年3月效仿,在一线试用失败后撤回了Keytruda的三线SCLC使用。
斯鲁利单抗特殊审批
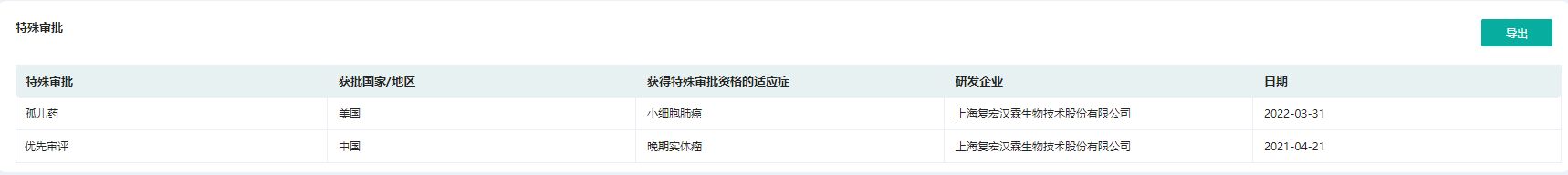
截图来源:药融云全球药物研发数据库
目前市场主要有2种PD-L1抑制剂。2019年经美国FDA批准,罗氏的Tecentriq联合化疗药物治疗ES-SCLC。IMpower133试验结果显示,在化疗中加入Tecentriq可降低30%死亡风险,患者存活率中位数为12.3个月,而对照组为10.3个月。阿斯利康于2020年进入该赛道,与单独化疗相比,其Imfinzi-chemo鸡尾疗法可将死亡风险降低27%。在CASPIAN试验中,Imfinzi联合化疗的患者中位寿命为13个月,而化疗组为10.3个月。
目前来看,复宏汉霖斯鲁利单抗似乎拥有最好的数据,在3期ASTRUM-005试验中,斯鲁利单抗联合化疗在新诊断的ES-SCLC患者中比单独化疗组降低了37%,患者的中位寿命分别为15.4个月和10.9个月。
研究人员在几个国家进行了这项试验,大约三分之一的患者是高加索人,但没有包括任何美国人群,这可能将会限制该药物在全球推进的开展。之前信达公司和礼来的PD-1竞争对手Tyvyt也因为类似原因没有得到支持。在与美国FDA交谈后,复宏汉霖现在了解到需要什么才能满足美国监管机构的要求。张文杰表示,将计划对美国大约200名患者进行一项桥接试验:包括黑人和西班牙裔代表将被分配到接受斯鲁利单抗或Tecentriq分组治疗。
张文杰补充道,美国FDA希望看到肿瘤反应率方面的“数字”差异,而不是总生存期或无进展生存率,因此这项研究应该很快。如果一切按计划进行,斯鲁利单抗可以在大约2年内获得美国的批准。目前,复宏汉霖正在美国和欧洲为其所有产品寻找营销合作伙伴,但该公司对斯鲁利单抗的商业化有更多的想法,“从长远来看,我们肯定考虑自己做全球营销”。
2022年上半年是复宏汉霖全面从Biotech向Biopharma进化的关键性的6个月,8月18日,复宏汉霖公布了2022年度中期业绩,实现营业收入约人民币12.894亿元,较去年同期增长约103.5%,主要来自多款产品陆续商业化带来的销售收入及授权许可收入等。在全速推进产品商业化布局的同时,复宏汉霖持续加码创新研发,2022年上半年公司研发开支约人民币8.274亿元。
据药融云数据库显示,复宏汉霖目前共有5款创新药产品上市,除斯鲁利单抗外,还有4款生物类似药,分别是曲妥珠单抗类似药、阿达木单抗类似药、利妥昔单抗类似药以及贝伐珠单抗类似药。其中,据药融云统计,利妥昔单抗的商业化效果最好,2021年在我国院内的销售额达到了近12亿人民币。(搜索"药融云小程序"进行相关更多数据查询)
复宏汉霖已上市创新药产品
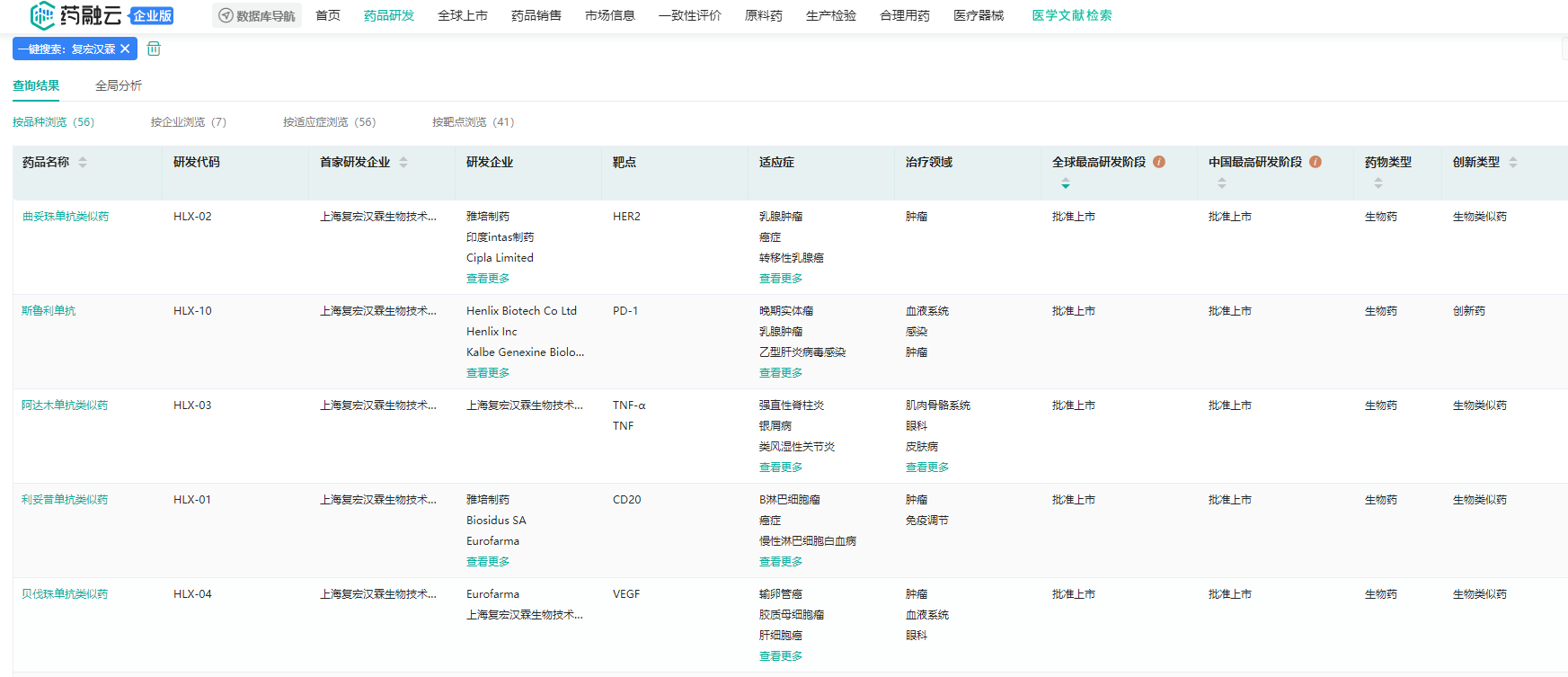
截图来源:药融云全球药物研发数据库
信息参考:
[1] https://www.fiercepharma.com/
[2] 药融云数据库https://www.pharnexcloud.com/?zmt-mhwz
想要解锁更多药企创新药信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、销售情况与市场前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论