
古生物学家斯蒂芬.杰伊.古尔德曾写道:“这是微生物的时代,过去如此,现在如此,将来还是如此……”
细菌是地球上最原始的生命形式之一,如果将地球过去38亿年的生命史压缩成24小时,那么我们的类人祖先将在午夜前最后两分钟内出现,而我们灵长类智人则在午夜前最后几秒登上历史舞台。与人类相比,细菌可以说是古老而坚韧的原住民。
作为20世纪人类最伟大的医学成就,抗生素的发现和使用挽救了数以亿计的患者,人们也曾认为抗生素可以一劳永逸地解决细菌感染,但是在迄今的70年间,由于抗菌药物在医疗及养殖领域的大量使用,甚至滥用,导致细菌耐药性的不断发展。
一项历时近20年的研究显示,在四环素、磺酰胺、青霉素和喹诺酮中观察到的细菌耐药率最高,并且在某些地区,这些化合物几乎已经完全失去了治疗感染的功效。与此同时,一些细菌正由单一耐药性发展为多重耐药性(MDR),构成严重公共卫生威胁。对于人类来说,一种“看不见”的敌人正在悄然出现——“超级细菌”。
多重耐药革兰氏阴性菌
世界卫生组织在2020年的一份报告中指出,虽然人们越来越意识到抗生素耐药性的直接威胁,但在全球范围内我们仍未能开发出迫切需要的抗菌疗法。也就是说,在人类与细菌的“军备竞赛”中,我们似乎已经落后。发表在The Lancet Global Health的一项研究表明,细菌性肺炎和血流感染是5岁以下儿童死亡的主要原因,约30%的败血症新生儿死于对多种一线抗生素耐药的细菌感染。
2017年,世界卫生组织发布了一份列有12种“超级细菌”的抗生素耐药“重点病原体”清单,并根据对新型抗生素的迫切需求程度将这些细菌分为三个类别:第一类为极高迫切度,耐碳青霉烯鲍曼不动杆菌、耐碳青霉烯铜绿假单胞菌、耐碳青霉烯肠杆菌位列其中;第二类为高迫切度,包含耐万古霉素屎肠球菌、黄色葡萄球菌、耐克拉霉素幽门螺杆菌等;第三类为中等迫切度,含青霉素不敏感肺炎链球菌、耐氨苄青霉素流感嗜血杆菌、耐氟喹诺酮志贺氏菌。
值得注意的是,在这份“超级细菌”清单中,第一类极高迫切度的耐药菌均为革兰氏阴性菌。因为虽然革兰氏阳性菌的细胞壁比革兰氏阴性菌厚,但革兰氏阴性菌有多层结构,并且脂多糖是革兰氏阴性菌所特有。复杂的结构意味着这类细菌的耐药机制也更加复杂,也导致了研发多重耐药革兰阴性菌抗菌药具有极高的技术壁垒。
据统计,2020年美国多重耐药革兰氏阴性菌抗菌药市场规模达到20.0亿美元(131亿元人民币),预计在2030年将增长至39.7亿美元(256亿元人民币);在国内,多重耐药革兰氏阴性菌感染的抗菌药市场保持稳定增长,从2016年的140亿元增至2020年的189亿元,预计2030年将达到422亿元。

然而,目前已上市治疗多重耐药革兰氏阴性菌感染的抗菌药物具有多方面的局限性。如新药开发进展缓慢,现有药物选择有限,大部分可用新药针对特定菌种的活性依然欠佳;目前已上市治疗多重耐药革兰氏阴性菌感染的抗菌药物均具有一定的毒副作用;新药的引入削弱了旧药的疗效,革兰氏阴性菌对目前药物的耐药性仍待进一步研究。随着全球范围内病原菌对现有药物的耐药性日益严峻,长期停滞不前的抗菌药物研发市场迎来了多款新型抗菌药物,为全球患者带来希望,然而中国本土创新的治疗多重耐药革兰氏阴性菌的抗菌药仍是空白。
多黏菌素
多黏菌素(Polymyxins)可以说是“大自然的馈赠”,是一种由多黏类芽孢杆菌产生的多肽类抗菌药物,多黏类芽孢杆菌在自然界分布广泛,也是土壤与植物微生态的优势种群之一。虽然多黏类芽孢杆菌本身属于革兰氏阳性菌,但其产生的多黏菌素却是革兰氏阴性菌的强大“克星”,能够与细胞壁脂多糖、脂蛋白的磷酸基结合,使细胞膜通透性增加,从而杀死细菌。

在自然界中,多黏菌素包含A、B、C、D和E五种亚型,但由于A、C、D亚型的毒性较大,目前上市产品主要为多黏菌素B和多黏菌素E。

▲多黏菌素的结构
图源:Synthesis of Best-Seller Drugs, 2016
早在20世纪50年代,多黏菌素就已上市,是临床上治疗革兰氏阴性菌感染的经典药物,特别是耐碳青霉烯类肠杆菌的唯一有效抗生素,已经成为治疗对其他抗生素有耐药性的感染的最后一线药物。不过,由于上市时间较早,多粘菌素没有经过完整的现代药物开发流程的验证,具有较严重的肾毒性,因此从上个世纪70年代开始逐渐停用,并被β-内酰胺类抗生素等安全性更高的抗菌药物所取代。
然而,近入21世纪后,曾在临床遭淘汰的多黏菌素又“重获新生”。随着耐碳青霉烯的细菌感染在全球范围内广泛出现,鲍曼不动杆菌、铜绿假单胞菌、肠杆菌等细菌的耐药形势日益严峻,而对抗这类细菌可选择的药物有限,临床上重新开始将多黏菌素加入联合疗法以对抗这些多重耐药性革兰氏阴性菌。据药融云数据库(www.pharnexcloud.com/?zmt-mhwz)不完全统计,多黏菌素(Polymyxin)类药物的全国医院销售数据逐年攀升,2021年达到了约19.14亿元,同比增长61.49%,而2022年仅上半年就达到了12.54亿元的销售额。
多黏菌素(Polymyxin)类药物院内销售情况

截图来源:药融云全国医院销售数据库
虽然临床上对多黏菌素类药物的需求逐渐增加,但是这类药物的肾毒性等问题依然存在。一项纳入48项研究共6199例患者的荟萃分析(Polymyxin-induced nephrotoxicity and its predictors: a systematic review and meta-analysis of studies conducted using RIFLE criteria of acute kidney injury;Pharmacological Research,01/2021)显示,多黏菌素引起的肾毒性合并发生率为45%;多黏菌素E引起的肾毒性合并发生率约为48%,而多黏菌素B为38%。为了解决传统多黏菌素类药物存在的缺陷,新一代多黏菌素类药物的开发逐渐提上日程。
MRX-8:多黏菌素类新型抗菌药
MRX-8是一款多黏菌素类新型抗菌药物,由专注于感染性疾病新药研发的科创板“超级抗生素”第一股——上海盟科药业股份有限公司(下称“盟科药业”)开发,用于治疗多重耐药革兰氏阴性菌感染。
临床前研究结果显示,MRX-8对临床分离得到的革兰氏阴性菌包括大肠杆菌、肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌、产酸克雷伯菌、柠檬酸杆菌、产气肠杆菌、阴沟肠杆菌等均表现出良好的抗菌活性。

▲MRX-8与现有药物对部分美国临床分离得到的革兰阴性菌的抗菌活性对比(注:MIC数值越低则抗菌活性越高)
而且由于MRX-8与现有的碳青霉烯类抗菌产品作用机制不同,不存在交叉耐药,因此MRX-8对目前临床最严重的碳青霉烯耐药的革兰氏阴性菌仍然有效,包括耐碳青霉烯鲍曼不动杆菌、耐碳青霉烯铜绿假单胞菌、耐碳青霉烯肺炎克雷伯菌、耐碳青霉烯肠杆菌等。

▲MRX-8对部分碳青霉烯(美罗培南)耐药阴性菌的活性情况(注:MIC数值越低则抗菌活性越高;MIC大于4mg/L代表对美罗培南耐药)
传统的多黏菌素类抗菌药物存在较强的肾毒性问题,限制其临床应用,MRX-8的开发正是克服了这类安全性问题。公司在早期化合物设计阶段,就引入了创新的“软药”设计思路,同步进行结构—活性关系与结构—毒性关系研究,最终得到了兼具有效性和安全性的MRX-8分子。体外HK-2试验肾毒性分析显示,MRX-8对肾细胞的半数抑制浓度大于200M,无显著毒性。在动物毒理研究中,相同剂量的多黏菌素B可导致肾毒性相关生物标记物的显著升高,而MRX-8未观察到此现象,即相比现有多黏菌素类药物,MRX-8的肾毒性显著降低。

▲MRX-8和多黏菌素B对人肾细胞的毒性对比
同时,MRX-8对肺部感染具有比传统多黏菌素类药物更好的疗效。在免疫低下小鼠铜绿假单胞菌肺炎模型实验中,与多黏菌素B相比,在给药剂量相当的情况下,MRX-8使铜绿假单胞菌菌落数降至多黏菌素B治疗组的1%,疗效显著提高。

此外,传统的多黏菌素类药物均为发酵生产,为生产、有效性、安全性带来了不确定性。MRX-8采用合成的方法进行原料药的生产,过程更加可控,显著提高了产品纯度,保证产品质量的一致性,更符合现代新药开发的要求。
药融云数据库显示,MRX-8正在中国和美国开展I期临床试验。

截图来源:药融云全球药物研发数据库
2022年10月24日,盟科药业披露MRX-8的美国临床I期试验结果,研究结果显示MRX-8在预计的临床治疗剂量下,对于美国健康受试者具有可接受的安全性和符合预期的药代动力学特性。在本次美国I期临床试验中,在预计临床治疗剂量1mg/kg、一天两次给药后,试验获得了MRX-8在人体内的药物暴露量数据,并根据上述研究预计该暴露量可有望对大肠杆菌、绿脓杆菌和鲍曼不动杆菌等引起的感染达到理想的疗效。同时,在探索性的高剂量给药情况下,试验也积累了肾损伤的发生数据。
接下来,盟科药业将会继续推进MRX-8的研发进度,推动中国I临床试验的顺利开展。公司将在完成中国I期临床试验后,结合前述美国I期临床试验结果,决定后续的临床开发策略。作为一家面向全球的抗感染药物领军公司,盟科药业力争早日将产品推进上市,为患者带来新的治疗选择。
此次进展也意味着,盟科药业的抗感染药物管线实现了从革兰氏阳性菌到革兰氏阴性菌的全面覆盖。MRX-8一旦开发成功,将改变多重耐药革兰氏阴性菌难以治疗的现状,甚至成为全球市场的稀缺型产品,从而进一步打造盟科药业在抗感染领域的全球竞争力。
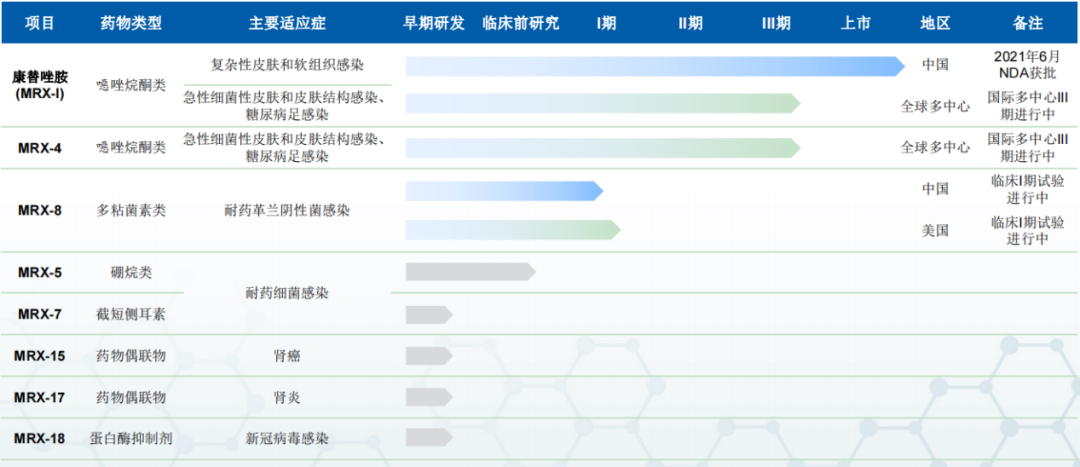
▲盟科药业pipeline
(信息或非最新,以官方发布为准)
盟科药业扎根“超级抗生素”稀缺赛道
在国内甚至全球范围内,少有企业在抗生素领域进行深度的布局,盟科药业可谓是科创板创新药公司的一股“清流”。
WHO的一份报告指出,由于药物开发过程中的经济挑战和固有的科学挑战,以及抗生素产品开发的高壁垒,限制了一些主要投资机构和许多大型制药公司对这一领域的兴趣,全球范围内抗生素开发工作主要由中小型企业开展,而这些企业往往难以筹得资金以将产品成功推到商业化阶段。在国内甚至少有企业能够看懂超级抗生素赛道的长期价值,大部分公司在高风险、长周期面前不敢下注。因此在应对“超级细菌”的“超级抗生素”的强烈市场需求下,盟科药业的稀缺性得以显现。
自成立之初,盟科药业便聚焦于全球日益严重的细菌耐药性问题,扎根“超级抗生素”稀缺赛道,秉承着“以良药求良效”的理念,目标为临床最常见和最严重的耐药菌感染提供更有效和更安全的治疗选择。除了前文提及的多黏菌素类新型抗菌药物MRX-8以外,盟科药业已有一款自主研发产品获批上市,多款创新产品处于在研阶段。
盟科药业核心产品康替唑胺是首个在中国上市的国产原研下一代噁唑烷酮类抗菌新药,可用于治疗多重耐药性革兰氏阳性菌引起的感染。盟科药业拥有自主知识产权,专利保护期可延至2033年。药融云数据库显示,该药于2021年6月通过国家药品监督管理局优先审评审批程序批准上市,获批仅半年便于2021年12月通过国家医保谈判纳入2021年国家医保目录(乙类),可谓迅速。目前该药已获批复杂性皮肤和软组织感染适应症,且正在拓展适应症治疗糖尿病足感染等。另据盟科药业披露,康替唑胺已于2022年3月启动全球多中心III期临床试验。商业化方面,2021年下半年,康替唑胺实现了766万元的销售额,而2022年前三季度累计实现营业收入约3438万元至3538万元,是去年同期的6.26至6.44倍,商业化前景可期。

截图来源:药融云全球药物研发数据库
MRX-4是基于康替唑胺结构独特设计和开发的水溶性前药,具有新的分子结构,可在体内转化为康替唑胺以发挥疗效,且相比康替唑胺拥有更长的专利保护期。MRX-4具有与康替唑胺相同的抗菌谱和药理性质,将作为已知或疑似多重耐药性革兰氏阳性菌感染的新用药选择。同时,该药被开发为口服和静脉注射两种剂型,为不同临床应用场景提供不同用药选择。在临床开发方面,MRX-4采用了国际化的临床试验策略,目前正在开展治疗急性细菌性皮肤和皮肤结构感染、糖尿病足感染的全球多中心III期临床试验,未来计划于美国、欧盟及中国等全球主要地区申报上市。商业化方面,由于MRX-4与康替唑胺在适应症和临床科室方面的一致性,MRX-4上市后可以通过康替唑胺的商业化团队和销售渠道进行市场推广,取得良好的协同效应。
除上述3款已进入临床阶段或商业化阶段的核心产品外,盟科药业还有多项处于临床前阶段的抗耐药菌新药,肾癌及肾炎药物以及抗新冠药物管线。
- 在耐药细菌感染领域,盟科药业有2款处于早期开发阶段的候选药物:硼烷类化合物MRX-5为新作用机制药物,目前尚无同类药物获批上市,具有firstinclass的潜力;截短侧耳素类抗生素MRX-7为基于一款已上市新药进行了改构,通过改善通透性及代谢稳定性,在保持或增强药效的同时,提高生物利用度,从而减少口服剂量、提高安全性。
- 在肾脏领域,盟科药业利用新的多肽药物偶联技术,自主设计并开发了肾脏靶向新药MRX-15和MRX-17,分别针对肾癌和肾炎。
- 针对新冠病毒,盟科药业选择冠状病毒特有的3CL蛋白酶作为靶点,开发口服小分子抑制剂MRX-18,目前该项目处于先导化合物优化阶段。
结 语
自2007年成立以来,盟科药业已在超级抗生素领域深耕了15年,首款自主研发的1类新药康替唑胺获批上市,打破了国内高端抗生素领域的外来垄断格局,而MRX-8的开发有望填补中国本土创新治疗多重耐药革兰氏阴性菌的抗菌药的空白,甚至成为全球稀缺型产品。期待盟科药业的创新“果实”能够顺利实现商业化落地,也希望有更多机构与企业能够关注到这一领域紧迫的需求,帮助人类在与细菌的“军备竞赛”中锻造更有力的武器。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据库,vip.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;
盟科药业公司公开披露(正文图片除标注外,均来自企业官方);
MissingMicrobes: How the Overuse of Antibiotics Is Fueling Our ModernPlagues;
Van BoeckelTP, Pires J, Silvester R, et al. Global trends in antimicrobialresistance in animals in low- and middle-income countries. Science.2019;365(6459):eaaw1944. doi:10.1126/science.aaw1944;
https://www.who.int/news/item/27-02-2017-who-publishes-list-of-bacteria-for-which-new-antibiotics-are-urgently-needed;
https://www.who.int/news/item/15-04-2021-global-shortage-of-innovative-antibiotics-fuels-emergence-and-spread-of-drug-resistance;
https://www.thelancet.com/journals/langlo/article/PIIS2214-109X(17)30362-5/fulltext;
https://doi.org/10.1016/j.phrs.2020.105328;
短期亏损难掩长期价值,盟科药业决战超级抗生素赛道,https://mp.weixin.qq.com/s/uFaGQItVk06JXiFErWhs0w;
为数不多,拥有获批上市1类新药的盟科医药;即将科创板上市,https://mp.weixin.qq.com/s/jlRQccLOt-y3UkjAKMpsMA;等等。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论