
据药融云数据库显示,盟科药业启动「康替唑胺片」和MRX-4治疗中度或重度糖尿病足感染的3期临床研究。不久前,2022年5月1日,盟科药业宣布其自主研发的抗耐药菌新药注射用MRX-4和康替唑胺片序贯用于治疗糖尿病足感染的全球三期临床试验,在洛杉矶的Harbor-UCLA 医学中心开始首例患者给药。

截图来源:药融云中国临床试验数据库
值得注意的是,近日证监会同意盟科药业科创板IPO,这意味着盟科药业很快将成为中国“超抗第一股”。将于7月27日开启申购,公司本次发行前总股本为5.25亿股,本次拟公开发行股票1.30亿股,占发行后总股本的比例为19.84%,其中网上发行2470.00万股,申购代码787373,申购价格为8.16元,单一账户申购上限为2.45万股,申购数量为500股的整数倍,顶格申购需持有沪市市值24.50万元。

康替唑胺片(优喜泰®)是由盟科药业自主研发,拥有国际知识产权的1类新药。于2021年6月1日,正式获得国家药品监督管理局(NMPA)的批准,用于治疗复杂性皮肤和软组织感染,成为首个在我国上市的国产噁唑烷酮类抗菌新药,打破了国内高端抗生素领域的外来垄断格局。
获批仅半年,盟科药业康替唑胺片即被纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2021年)》,是此次新版目录中唯一新增的具有新化学结构的抗耐药菌新药。与利奈唑胺属于最严格的“特殊使用级”不同,康替唑胺属于第二类的“限制使用级”,在临床使用上有更少的限制性。凭借差异化的市场定位和药物安全性的优势,康替唑胺有望迅速获得高端抗生素的市场份额。
康替唑胺片医保目录信息

截图来源:药融云医保目录数据库
据弗若斯特沙利文数据显示,噁唑烷酮类药物在中国治疗多重耐药革兰阳性菌感染的抗菌药市场中持续呈增长,预计将在2030年增长至60亿元。据盟科药业财报,2021年下半年,康替唑胺实现了766万元的销售额,而在今年1-3月其销售收入已增加至1068.7万元,仅今年一个季度其销量就已超过2021年全年的水平,商业化前景可观。
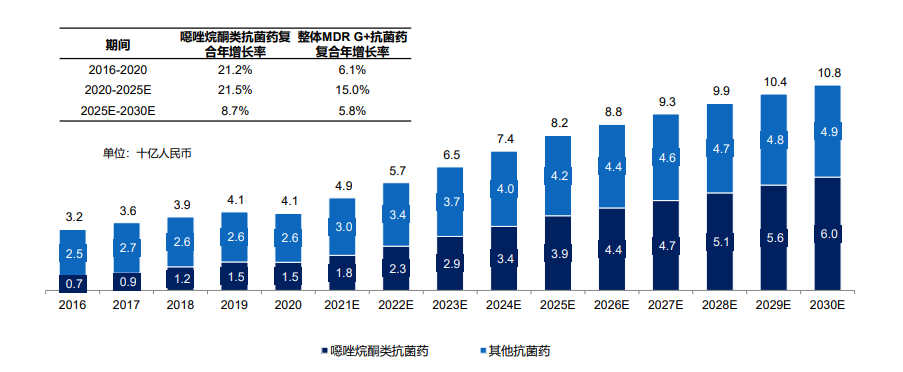
图片来源:盟科药业招股书
在美国,康替唑胺(Contezolid)也获得了美国食品药品监督管理局(FDA)授予的合格感染类疾病产品(QIDP)认证,可享受快速通道(Fast Track)资格和额外的上市后市场专有权保护。2022年5月1日,盟科药业宣布MRX-4和康替唑胺片序贯用于治疗糖尿病足感染的全球三期临床试验,在洛杉矶的Harbor-UCLA 医学中心开始首例患者给药,这是注射用MRX-4上市申请的注册临床试验,也将作为康替唑胺片进一步扩展适应症的研究,是康替唑胺首个国际多中心临床试验。
据悉,目前盟科药业商业化产品及临床阶段药物共3款,其中康替唑胺已于中国进入商业化阶段,同时已完成美国II期临床试验;MRX-4已完成美国II期临床试验和中国I期临床试验,并已启动MRX-4序贯康替唑胺的全球多中心III期临床试验;MRX-8正进行美国I期临床试验。
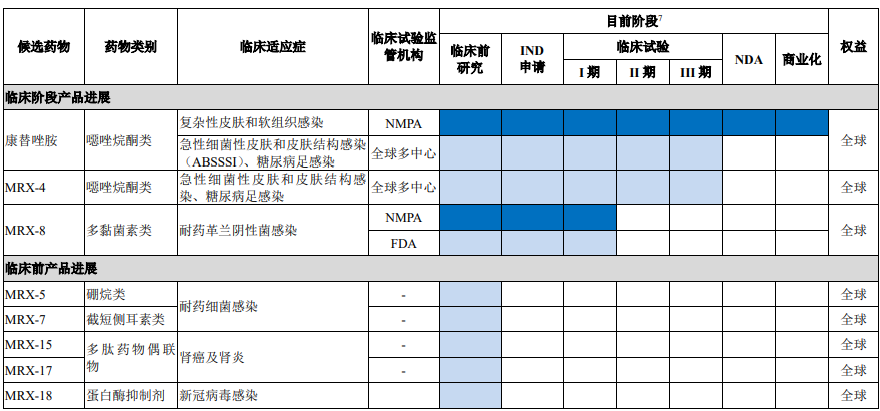
截图来源:盟科药业招股书
其中MRX-4为康替唑胺的“升级版”。是由于盟科药业在进行康替唑胺的开发中,发现康替唑胺的水溶性较低,对需要大剂量服用的抗菌药而言,开发注射用制剂存在较大的挑战。因此在康替唑胺的结构中引入可降解的磷酸基团,以提高药物分子的水溶性,并改善药代动力学性质,进行反复的分子设计与优化验证,而最终得到的达到预期设计目的的候选药物。
除了超级抗生素之外,盟科药业也在积极开发其他品种,比如运用抗生素技术开发两款肾病药物,MRX-15(肾炎)、MRX-17(肾癌),未来会申请IND,切入到其他领域。同时公司利用化学改构能力上的优势,开发当下热门的ADC药物、小分子新冠药MRX-18等热门领域产品管线,主要临床前在研项目和拟达到的目标如下表。
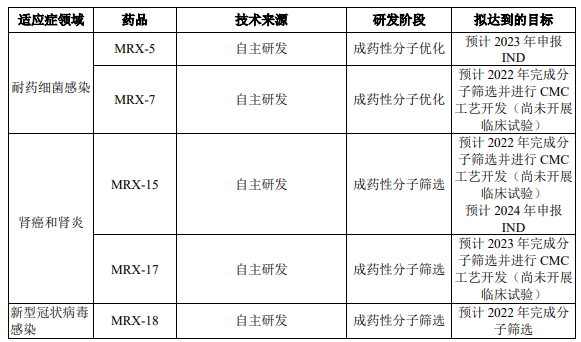
截图来源:盟科药业招股书
参考来源:
[1] 盟科药业官网
[2] 盟科药业官方披露
[3] 药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论