
君赛生物向港交所递交招股书,拟登陆港股生物科技板块。其凭借全球首款“免清淋、免IL-2注射”的TIL疗法GC101等构建竞争优势,GC101预计2026年提交上市申请。公司另一重点产品GC203也已进入后续开发阶段。
日前,聚焦实体瘤创新细胞疗法与创新药开发的上海君赛生物股份有限公司(下称“君赛生物”)正式向港交所递交招股书,拟依据港股18A章登陆生物科技板块。
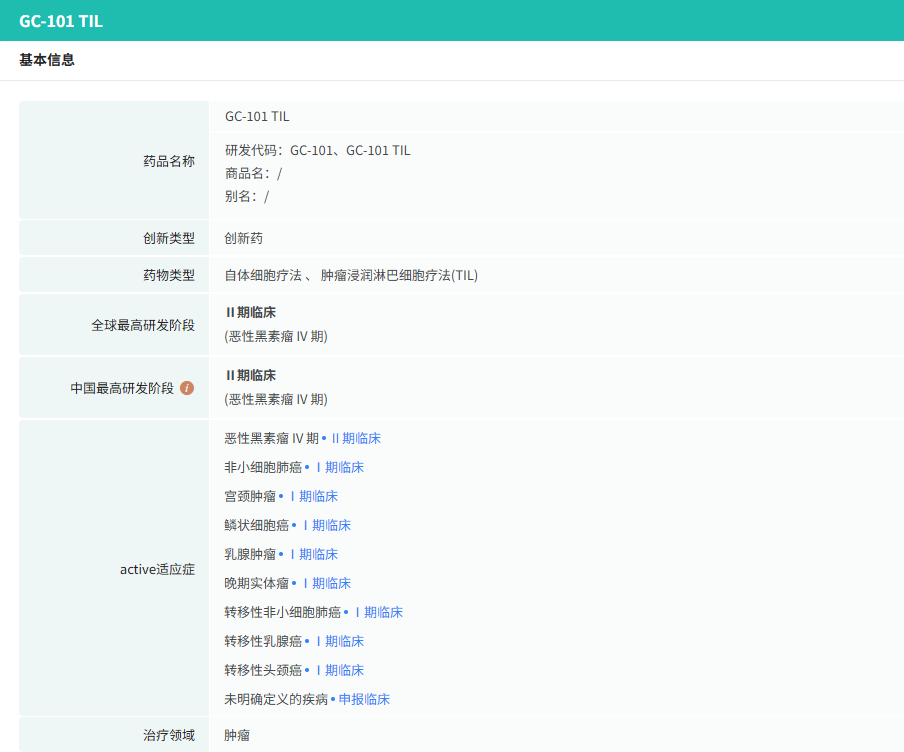
据弗若斯特·沙利文资料,这家成立六年的企业,凭借全球首款无需高强度清淋化疗、无需IL-2(白细胞介素-2,一种促进T细胞生长、分化及存活的细胞因子)给药的TIL(肿瘤浸润淋巴细胞)疗法 GC101,以及全球首款非病毒载体基因修饰TIL细胞新药 GC203,在实体瘤治疗领域构建起差异化竞争优势。
最新临床数据显示,GC101 针对标准治疗失败的转移性晚期非小细胞肺癌患者客观缓解率(ORR)达41.7%,针对晚期黑色素瘤患者客观缓解率为30%,有望成为中国首个获批上市的TIL疗法。
截图来源:摩熵医药数据库-全球药物研发数据库
乘着港股生物科技板块回暖、首版商业健康保险创新药品目录落地的行业东风,君赛生物此次IPO(首次公开募股)募资能否支撑其度过临床冲刺与商业化筹备的关键期,应对全球十余款同类在研产品的竞争,成为市场关注的核心。
聚焦癌症免化疗疗法,有望将“370万元治疗费用”平民化?
TIL疗法是目前实体瘤治疗领域的热门方向,所用细胞主要来源于切除的肿瘤组织。该疗法通过收集自体TIL细胞,在体外激活并大量扩增,经淋巴细胞清除处理后回输至患者体内。激活后的TIL细胞可识别肿瘤特异性抗原并破坏肿瘤细胞。
但传统TIL疗法有个大问题,治疗前需要给患者做高强度清淋化疗,还得注射大剂量IL-2,这两种操作不仅会让患者出现严重副作用,整个过程还存在治疗相关死亡、严重感染、心肺功能损伤等风险,这些因素以及高昂的价格极大限制了临床应用。
从目前数据来看,君赛生物的 GC101 对多种难治性晚期实体瘤都有效果。针对标准治疗失败的10例转移性晚期黑色素瘤患者(中位前序治疗线数为3.5,100%经PD-1抗体治疗失败)客观缓解率为30%,中位无进展生存期为5.5个月。
针对标准治疗失败的12例转移性晚期非小细胞肺癌患者(中位前序治疗线数为3),中位随访13.0个月时, GC101 展示出41.7%的客观缓解率,中位缓解持续时间未达到;12个月总生存率为66.7%,中位生存期尚未达到。
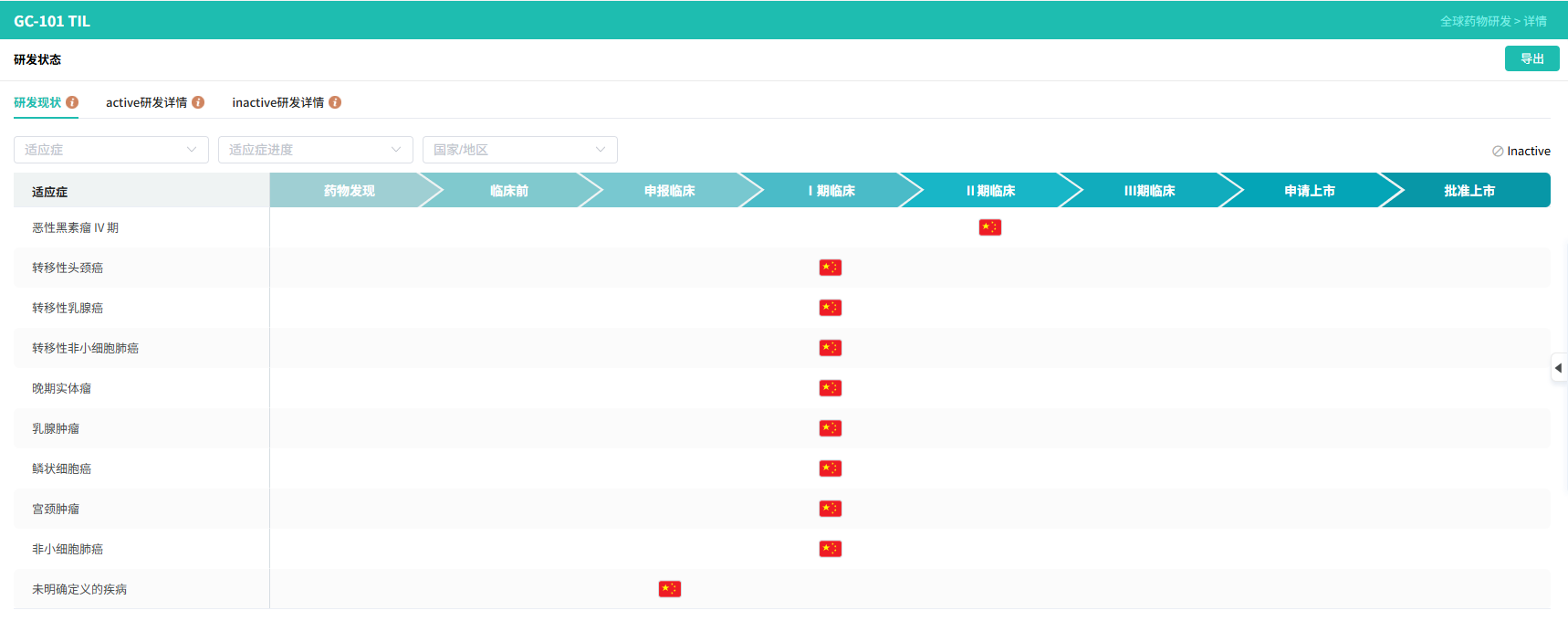
目前,GC101 用于治疗黑色素瘤的临床试验正在开展关键II期临床试验,预计将于2026年提交生物制品许可申请(BLA);GC101用于治疗非小细胞肺癌的临床管线目前处于Ib期临床。除此之外,其在宫颈癌、胆管癌、结直肠癌、乳腺癌、头颈部鳞状细胞癌、肉瘤、胆囊癌等恶性肿瘤中均显示出巨大潜力。
查数据,找摩熵!图源摩熵医药数据库
按照计划,GC101预计2026年提交上市申请,若成功获批,将成为国内首个上市的TIL疗法,且治疗成本预计仅为进口产品的几分之一。除了 GC101,君赛生物还有一款重点产品 GC203,是全球首款非病毒载体基因修饰TIL新药。这款产品在 GC101 基础上做了优化,能让回输的免疫细胞在体内更活跃、存活更久。
目前,GC203 在卵巢癌患者中已显示出潜力,在IIT(研究者发起的临床试验)中,GC203治疗高度经治的卵巢癌患者,客观缓解率为33.3%,完全缓解率达11.1%,一年整体生存率达68.8%。目前,该产品已获得临床研究批准,进入后续开发阶段。
从行业前景来看,全球TIL疗法市场增长迅速,预计到2035年规模将达45亿美元。中国市场虽起步晚,但增速更快,2030年至2035年复合年增长率预计达40%,超过同期全球市场的增长速度。君赛生物的产品布局,正踩中这一增长风口。
研发投入持续增长,十余款同类疗法同台竞技
2023年公司研发开支5762万元,2024年增至9099万元,2025年上半年已达5280万元,核心产品相关研发成本占比为46%。随着GC101等产品进入关键临床阶段,临床试验规模扩大、生产工艺优化等将进一步推高研发支出。
事实上,君赛生物已完成C轮融资,投资方包括凯泰资本、复容投资等资深机构。全球范围内,已有十余款同类TIL疗法处于在研阶段,美国IOVANCE公司作为行业领军者,其产品 Amtagvi 已获批黑色素瘤适应证,国内方面,华赛伯曼等企业的TIL疗法也在快速推进。君赛生物需在临床进度、疗效数据、成本控制等方面持续构建优势,才能在竞争中脱颖而出。
值得一提的是,行业政策正释放积极信号。中国监管机构推出的突破性治疗药物程序、附条件批准程序等,加速了创新细胞疗法的审批进程。2025年12月,首版商业健康保险创新药品目录纳入5款国产CAR-T疗法,为同类创新细胞疗法的支付体系建设提供了参考,这有望缓解TIL疗法未来商业化的支付压力,提升产品可及性。
参考来源:
[1] 企业官网/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论