
药物研究其中一个非常重要的考察因素是安全。

Allogene Therapeutics公司虽然在去年年底经历了因“染色体异常”导致的临床研究搁置,但后续经过一系列的努力和对问题的解决,Allogene近日宣布,在研的现货型CAR-T疗法——ALLO-501A的潜在关键性2期临床试验ALPHA2开启,该试验用于复发/难治性(r / r)大B细胞淋巴瘤(LBCL)患者。据药融云数据库显示,ALLO-501A为CD19靶向药物,目前在美国和法国开展临床试验,其中在美国进展稍快,针对B淋巴细胞瘤的试验已推进到临床2期。
药物基本信息(部分)
截图来源:药融云全球药物研发数据库
Allogene在披露2期开始的声明中表示,该协议“得到了1期试验的临床和转化数据的支持,表明当与包括优化剂量的’抗CD52单克隆抗体’ALLO-647的淋巴细胞增溶方案一起使用时,单剂量的ALLO-501A可以实现深度反应。”其中ALLO-647为Allogene公司即将展开的另一项EXPAND试验,检视其在研药物ALLO-647搭配标准淋巴去除方案(氟达拉滨/环磷酰胺)改善同种异体CAR-T疗法的效果。若试验结果积极,该公司将与美国FDA讨论递送ALLO-501A与ALLO-647的上市申请。
r/r LBCL的单臂2期ALPHA2试验将使用单剂量的ALLO-501A,含1.2亿个CAR-T细胞,其预期的淋巴细胞补充方案(FCA90)由氟达拉滨(30mg / m2/天x 3天)和环磷酰胺(300 mg/m2/天x 3天)加 ALLO-647(90 mg)。ALPHA2试验将招募大约100名接受过至少2种先前治疗线且先前未接受过抗CD19治疗的患者,主要终点是对客观反应率(ORR)的统计。
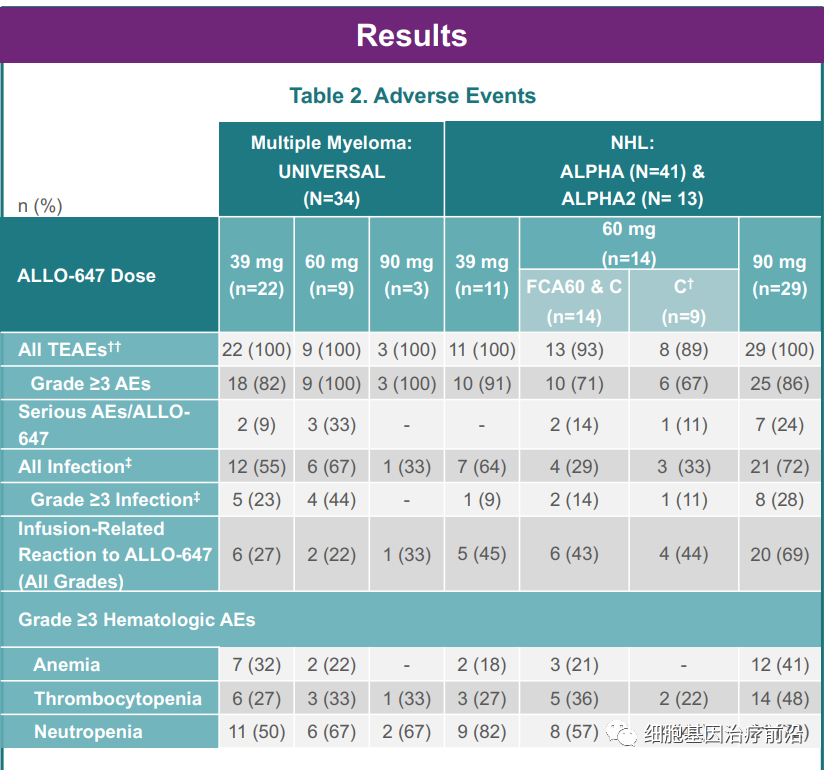
2期试验的参与者将接受90mg的ALLO-647。在该剂量下,86%的参与者在早期的非霍奇金淋巴瘤(NHL)试验中具有3级或更严重的治疗突发不良事件,60mg剂量的受试者发生率为71%。可见,较高的剂量与病毒感染细菌的高发生率有关。
同时,EXPAND试验是ALLO-647的一项单独的潜在注册试验,目标是潜在地实现AlloCAR T候选产品(包括ALLO-501A)的扩增、持久性和改善临床结果。该随机扩展试验预计将招募约70名 r/r LBCL 患者,旨在证明ALLO-647的安全性及其对淋巴细胞耗竭方案整体有效性的贡献。患者将被随机分配接受与ALPHA2试验相同的单次1.2亿细胞剂量的ALLO-501A,并单独使用氟达拉滨和环磷酰胺淋巴细胞去除方案(对照组,不含ALLO-501A)或与ALPHA2试验相同的淋巴细胞补充方案(试验组)。
因为研究将较高的ALLO-647暴露,与更深、更长的淋巴细胞消退和更高的IL-15水平联系起来,Allogene选择了90mg剂量。
今年6月,美国FDA授予了该现货型CAR-T疗法再生医学高级疗法(RMAT)指定为 r/r LBCL。这一称号支持了对现成的CAR-T疗法产品的需求,“可以更快、更可靠、更大规模地交付,”Allogene研发执行副总裁兼首席营销官Rafael Amado博士当时表示。
ALLO-501A特殊审评
截图来源:药融云全球药物研发数据库
信息参考:
[1] https://allogene.com/
[2] 药融云数据库
想要解锁更多药企创新药研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、药物研发信息、申报审批情况、临床试验信息、最新进展、市场规模与前景等,以及帮助企业抉择可否投入研发时提供数据参考!注册立享15天免费试用!

<END>


































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论