
1.Resmetirom研发历程
2005年,罗氏的研发人员在研究糖尿病或肥胖疾病的治疗药物过程中发现了有降低肝内脂肪潜力的Resmetirom【1】,同年7月罗氏就这一发现在美国申请了临时专利,并于2006年7月提出正式申请。但罗氏似乎对Resmetirom一类药物的研发兴趣不大,2008年12月便将其全球范围内的研发及商业化权益转让给了VIA Pharmaceuticals Inc【2】,2011年9月Madrigal Pharmaceuticals Inc购买并承接了VIA Pharmaceuticals Inc的所有资产,至此,Resmetirom的权益归Madrigal Pharmaceuticals Inc所有【3】。
获得权益后,Madrigal Pharmaceuticals Inc便紧锣密鼓地开始了Resmetirom治疗非酒精性脂肪性肝炎(NASH)的I期临床研究,2016年10月顺利进入II期临床,2019年3月进入III期临床【3】,经历数年III期临床试验研究,2023年6月Madrigal Pharmaceuticals Inc向FDA提出了新药申请,最终Resmetirom凭借出色的临床积极结果于2024年3月14日获FDA加速批准上市。Resmetirom从发现到上市历经18年的漫长岁月,从默默无闻到脱颖而出,背后离不开Madrigal Pharmaceuticals Inc公司在NASH治疗领域的专注和坚持。Resmetirom的获批是NASH治疗领域的里程碑事件,填补了此前NASH治疗领域的市场空白。(相关阅读:【深度】NASH百亿美元蓝海市场即将爆发,谁将成为下一个掘金者?)
Resmetirom研发历程

2.Madrigal Pharmaceuticals Inc简介
Madrigal Pharmaceuticals Inc是一家致力于开发心血管代谢疾病和NASH治疗领域小分子药物的公司【4】,其前身为VIA Pharmaceuticals Inc。VIA Pharmaceuticals Inc成立于2004年9月,是一家专注于开发针心血管疾病治疗药物的生物技术公司【2】。2011年9月VIA Pharmaceuticals Inc将资产全部出售给了Madrigal Pharmaceuticals Inc【3】。
2016年7月,Madrigal Pharmaceuticals Inc完成了对Synta Pharmaceuticals的并购,以推进NASH新药研发【3】。
3.Resmetirom原研专利全球布局分析
01化合物专利
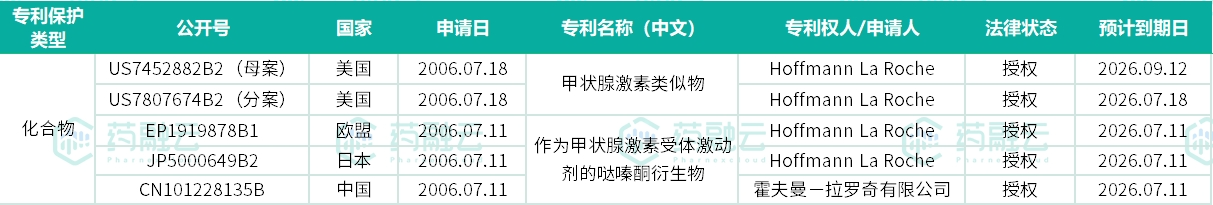
罗氏集团发现Resmetirom化合物后,2005年7月在美国申请了临时专利(US70121505P),基于临时专利,2006年7月11日提出正式专利申请(国际公开号:WO2007009913A1),化合物专利全球布局的国家/地区包括美国、加拿大、欧盟、俄罗斯、中国、日本、韩国、新西兰、澳大利亚、阿根廷、墨西哥、厄尔多瓜和巴西。
目前Resmetirom化合物专利权仍归罗氏所有,在美国申请日为2006年7月18日,由于在美国获得了56天的专利期延长,预估其在美国到期日为2026年9月12日,其他国家/地区到期日仍为2026年7月11日。
Resmetirom合物专利全球国家/地区布局
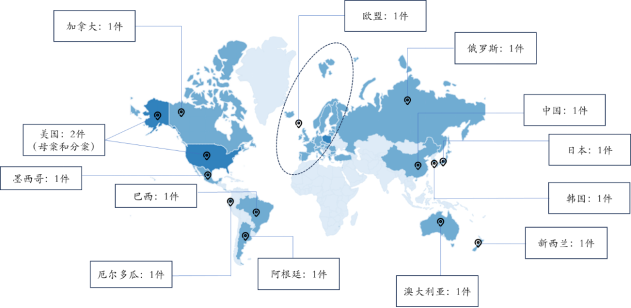
图片来源:https://www.lens.org/;整理自药融咨询
Resmetirom化合物专利主流国家/地区详情
02晶型专利
Resmetirom的化合物专利将于2026年7月过期,Madrigal Pharmaceuticals已布局申请了2项晶型专利以延长药品专利保护期:
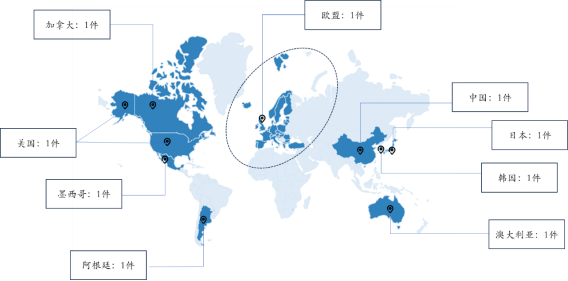
(1)“合成甲状腺激素类似物及其多形体的方法”(国际公开号:WO2014043706A1;WO2014043706A8),保护I型晶型,专利申请日为2013年9月17日,目前在美国、欧盟、日本和中国均已获得授权,布局的国家/地区包括美国、加拿大、欧盟、俄罗斯、中国、日本、韩国、新西兰、澳大利亚、印度、阿根廷和墨西哥。
Resmetirom晶型(1)专利全球国家/地区布局

图片来源:https://www.lens.org/;整理自药融咨询
(2)“2-(3,5-二氯-4-((5-异丙基-6-氧代-1,6-二氢哒嗪-3-基)氧基)苯基)-3,5-二氧代-2,3,4,5-四氢-1,2,4-三嗪-6-腈的固体形式”(国际公开号:WO2020010068A1),保护游离态晶型、共晶、多种盐晶型,该项晶型专利还在申请中,暂未获得授权,目前布局的国家/地区包括欧盟、美国、加拿大、阿根廷、墨西哥、中国、日本、韩国和澳大利亚。
Resmetirom晶型(2)专利全球国家/地区布局
图片来源:https://www.lens.org/;整理自药融咨询
Resmetirom晶型专利主流国家/地区详情
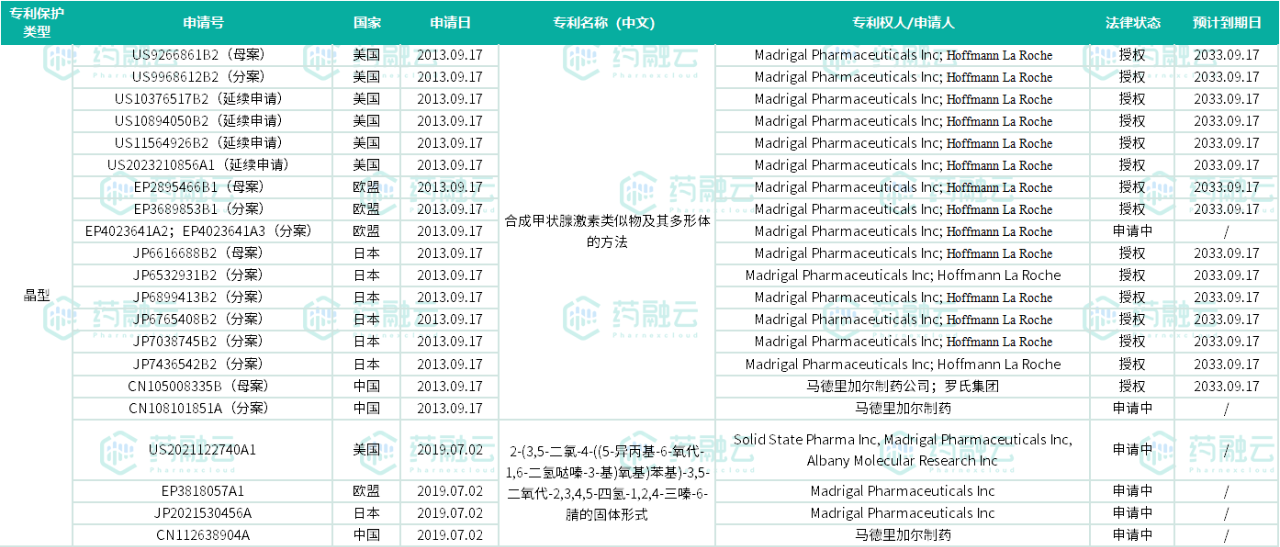
信息来源:EPO官网、药融云专利检索数据库;整理自药融咨询
03用途专利
原研公司申请了3项关于Resmetirom的用途专利:
(1)“用于治疗肝紊乱或血脂紊乱的瑞舒伐他汀和Resmetirom的治疗组合”(国际公开号:WO2022165227A1):要求保护的是瑞舒伐他汀和Resmetirom组合治疗NASH或脂肪肝和高脂血症或高胆固醇血症的新用途,申请日为2022年1月28日,目前专利还在申请中,暂未获得授权,专利申请布局的国家/地区包括加拿大、欧盟、中国、日本、韩国和澳大利亚。
Resmetirom用途专利(1)全球国家/地区布局
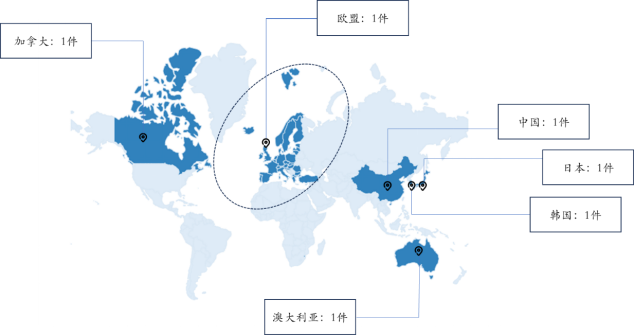
图片来源:https://www.lens.org/;整理自药融咨询
(2)“用于减少肝脏体积的Resmetirom”(国际公开号:WO2023049491A1):要求保护的是Resmetirom改善NASH患者疾病进展过程中出现的肝脏体积增大症状的用途,申请日为2022年9月27日,专利还在申请中,目前同族专利申请国家只有阿根廷。
Resmetirom用途专利(2)全球国家/地区布局
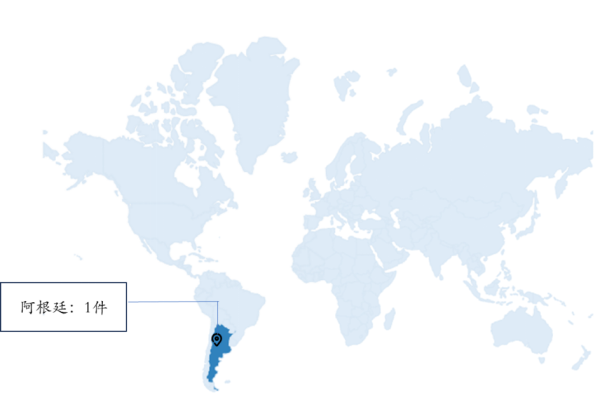
图片来源:https://www.lens.org/;整理自药融咨询
(3)“用THR-BETA兴奋剂治疗肝脏疾病或脂质疾病的方法”(国际专利号:WO2018075650A1):要求保护的是Resmetirom治疗NASH和高脂血症或高胆固醇血症的用途,申请日为2017年10月18日,专利申请布局的国家/地区包括美国、加拿大、欧盟、墨西哥、日本和澳大利亚,其中美国和欧盟的申请已获授权,日本的申请还在审理中,在中国曾提交过申请(公开号:CN110167557A),但因逾期未答复审查意见通知书已被视为撤回。
Resmetirom用途专利(3)全球国家/地区布局
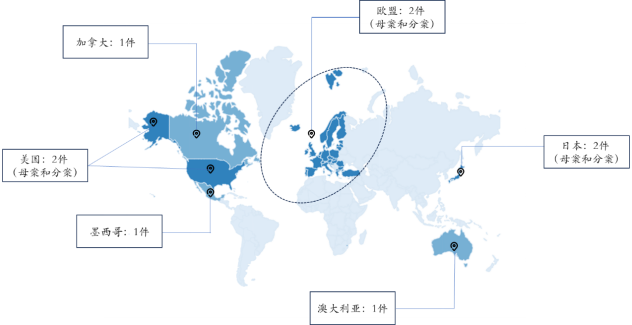
图片来源:https://www.lens.org/;整理自药融咨询
Resmetirom用途专利主流国家/地区详情

信息来源:EPO官网、药融云专利检索数据库;整理自药融咨询
04制备方法专利
原研公司还申请了1项Resmetirom的化合物制备专利(国际公开号:WO2022087141A1),该专利申请日为2021年10月20日,在美国、欧盟、日本和中国都已提交申请,且均还在审理中。
Resmetirom制备方法专利主流国家/地区详情

信息来源:EPO官网、药融云专利检索数据库;整理自药融咨询
结语
Resmetirom化合物专利将于2026年7月11日过期,但原研公司已经着手在全球主要国家/地区布局其晶型专利和用途专利,构建药品专利保护网络。
晶型专利方面,I型晶型专利在全球主流国家/地区已获授权,预计2033年9月17日到期;其他游离态晶型、共晶、多种盐晶型专利还在申请中。
用途专利方面,瑞舒伐他汀和Resmetirom组合治疗NASH或脂肪肝和高脂血症或高胆固醇血症还在申请中;Resmetirom改善NASH患者疾病进展过程中出现的肝脏体积增大症状的用途专利还在申请中;Resmetirom治疗NASH和高脂血症或高胆固醇血症的用途专利在美国和欧盟已授权,日本还在申请中,中国的专利申请已被视为撤回,可持续关注。
参考资料:
[1]https://www.linkedin.com/posts/tao-cong_resmetirom-rezdiffra-nash-activity-7175292072369770496-3I66
[2]药融云bcpmdata:药融云医药交易&投融资数据库 (bcpmdata.com)
[3]Madrigal Pharmaceuticals Inc年度报告
[4]Madrigal Pharmaceuticals Inc官网:https://ir.madrigalpharma.com/news-releases/news-release-details/madrigal-pharmaceuticals-completes-merger-synta-create-leading
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论