
6月10日,晖致医药的瑞维那新吸入溶液正式获批,成为国内首个每日一次雾化吸入的长效抗胆碱药(LAMA)。
距离获批仅10天,已有3家仿制企业迅速完成申报并获受理。
四川普锐特6月19日首家,广州大光与齐鲁制药紧随其后,于6月20日同天获受理,三家均为4类仿制。

仿制药企业入局的速度越来越快。
尤其今年以来,仿制药“等原研一落地,立刻快节奏群起而攻之”的打法,已经频繁上演。
佩玛贝特片,原研获批仅15天,第五家仿制便已申报上市。第五家申请上市,原研获批仅15天!
乙酰半胱氨酸注射液更疯狂,原研上市短短1个月,36家申报,已然卷到极限。20天19家!乙酰半胱氨酸彻底失控!
前脚原研刚上市,后脚仿制药就排队进场。
仿制药的进场速度被不断刷新,频率已经超过了一天一家。
如今,瑞维那新成为最新一例“被集火”的品种。
瑞维那新由Theravance Biopharma研发,2018年11月获FDA批准。2019年晖致医药获得其在大中华区的独家商业化权益,并于2023年完成国内III期临床申报。此次以5.1类路径获批,为国内首张上市批件。
作为一款新型长效LAMA产品,瑞维那新可每日一次雾化吸入,主要用于缓解慢性阻塞性肺病(COPD)患者的呼吸道痉挛。肺部定向性强、维持时间长、全身副作用较少。
更早在2023年10月,瑞维那新已被纳入药政司公示的第三批鼓励仿制药建议目录,属于政策“明确鼓励仿制”的品种之一。

背后,是一个不容忽视的庞大市场。
《柳叶刀》刊发的《中国成人肺部健康研究》显示,我国慢阻肺患者总人数已接近1亿,40岁以上人群的患病率达到13.7%。由于COPD不可逆,治疗方案的核心诉求在于减缓急性加重,提升生活质量。长期依赖吸入治疗,是这一人群的用药常态。
据摩熵数据库统计,2023年我国阻塞性气道疾病吸入剂在全国医院销售总额已突破800亿元。
高患者基数、慢病依赖性、市场确定性,使得此类产品在仿制路径清晰、无专利限制的背景下,天然成为国产企业眼中的“可攻之地”。
除已申报上市的3家外,原研上市前还有武汉人福利康、云南龙海、长风药业、江苏正大清江4家企业申请临床,并获临床默示许可。但并未开展临床。

若继续推进,一个月内形成10家申报的规模,并非难事。
论国产仿制药的进口替代,吸入制剂市场可谓极具代表性。
长期以来,吸入制剂被视为“药械协同、壁垒高筑”的典型代表,由阿斯利康、勃林格殷格翰、GSK等外资巨头主导市场,凭借设备绑定与推广优势,在医院端几乎垄断。
2019年是拐点。当年,健康元拿下国内首个吸入制剂仿制批文。2020年,CDE出台《经口吸入制剂仿制药药学与人体生物等效性研究指导原则》,为国内企业提供标准化路径。
加上专利到期的窗口同步开启,技术盲区转化为产业风口。
至今已有19个吸入品种完成仿制过评,其中6个已纳入集采。

进入2025年,国产吸入制剂更全面提速。短短两个月,喜讯连连。
4月9日,济民可信集团自主研发的吸入用丙酸倍氯米松混悬液获批,打破原研凯西制药十余年的独家垄断。
4月22日,远大医药的丙酸氟替卡松鼻喷雾剂获批,终结GSK在华25年的独占地位。
5月21日,河北创建药业成为该品种的第二家过评企业,距首仿上市仅1个月。
过去高度封闭、审批周期冗长的品类,正在被国产仿制药企业集体拆解,申报节奏从年压缩至月,直至以日为单位。
截至目前,除晖致合作引入外,国内已有近150家药企拥有吸入制剂在用批文,另有逾百家处于临床阶段。
仿制药正全面进入提速状态,原研未热,仿制先至。

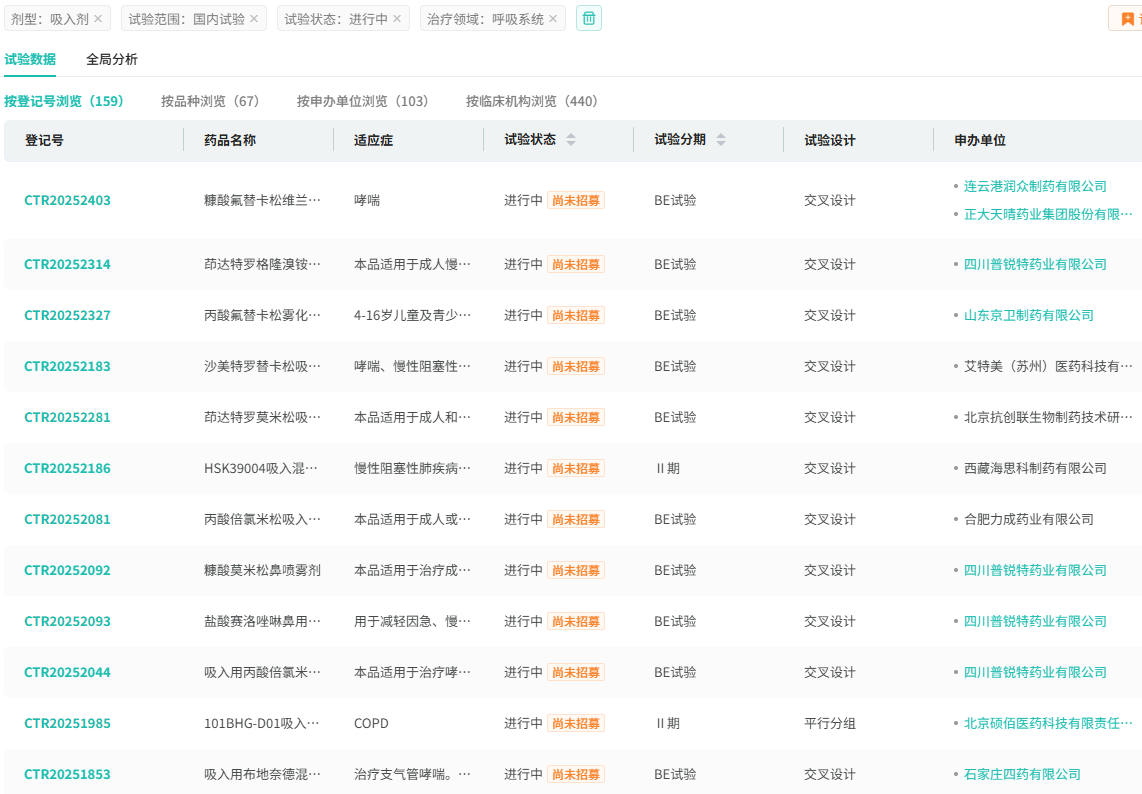
图源:摩熵医药数据库
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论