1.3.1 本周国内医药大健康行业政策法规速览
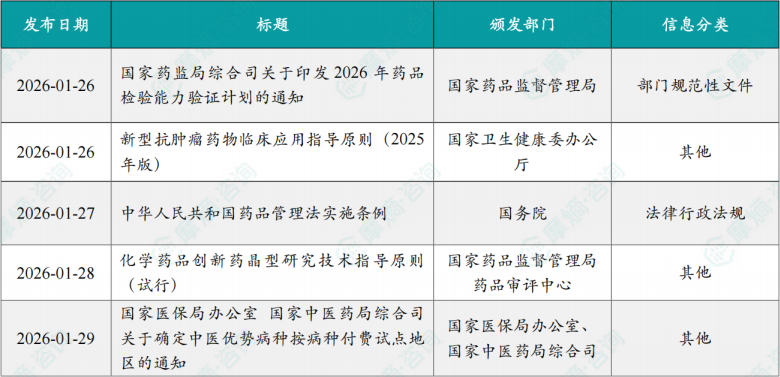
1.3.2 本周重点行业政策详细说明
·《中华人民共和国药品管理法实施条例》发布
1月27日,国务院总理李强日前签署国务院令,公布修订后的《中华人民共和国药品管理法实施条例》,自2026年5月15日起施行。《条例》共9章89条,修订后的主要内容如下:
一是完善药品研制和注册制度。支持以临床价值为导向的药品研制和创新,鼓励研究和创制新药,支持新药临床推广和使用。明确药物非临床安全性评价研究机构资格认定程序,细化药物临床试验管理要求。设立药品上市注册加快程序,明确药品再注册程序,规定处方药、非处方药转换机制。对符合条件的儿童用药品、罕见病治疗用药品给予市场独占期,对含有新型化学成份的药品等进行数据保护。细化药品上市许可持有人的责任。
二是加强药品生产管理。严格药品委托生产管理,压实委托生产时药品上市许可持有人的责任,明确可以委托分段生产药品的情形。明确中药饮片、中药配方颗粒生产、销售的管理要求。
三是规范药品经营和使用。完善药品网络销售管理制度,压实药品网络交易第三方平台提供者责任。加强医疗机构药事管理,保障使用环节药品质量。明确医疗机构配制制剂审批流程,规定医疗机构制剂调剂使用条件和程序,支持配制儿童用医疗机构制剂,满足儿童患者用药需求。
四是严格药品安全监管。明确药品安全监督检查措施。细化药品质量抽查检验流程,规定当事人对检验结果有异议的,可以申请复验。针对违法行为设定了严格的法律责任。
同期事件:
1. 2026年第5周01.26-02.01国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第5周01.26-02.01国内仿制药/生物类似物申报/审批数据分析
3. 2026年第5周01.26-02.01全球创新药研发概览
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.01.26-2026.02.01) },如需查看或下载完整版报告,可点击!
扩展阅读:
1. 2024年第34周08.19-08.25国内医药大健康行业政策法规汇总
2. 2024年第25周06.17-06.23国内医药大健康行业政策法规汇总
3. 2024年第22周05.27-06.02国内医药大健康行业政策法规汇总
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论