对于医药投资者、医药股民来说,重磅新药的获批临床、上市申请、批准生产等信息,都会给股价带来很大的提振作用。
那么这些新药的一手信息是如何知晓的呢?如全球最新上市新药、最新突破性疗法、新药研发最新进度等消息该如何查询?
一、官方权威渠道:监管机构的公开信息平台
①中国CDE(药品审评中心)——国内新药信息的"第一现场"
国家药品监督管理局药品审评中心(CDE)官网是查询国内新药审评审批信息的权威来源。可获取以下关键信息:
受理品种信息:查询2000年1月1日至今CDE承办的所有受理号、药品品种及企业信息,第一时间发现哪些企业的IND(临床试验申请)或NDA(新药上市申请)已被受理
突破性治疗公示:查看被纳入突破性治疗药物程序的品种,这类药物通常具有重大临床价值,获批概率高,对股价催化作用明显
优先审评公示:纳入优先审评的品种审评时限缩短至130个工作日,信息公布后往往成为市场热点
临床试验默示许可:自2018年起,我国对新药临床试验实施默示许可制度,CDE官网会公示相关许可信息
上市药品信息:新药获批上市后6个月内,CDE会公开技术审评报告,大家可查看药品的质量、安全性、有效性等关键审评细节。
查询技巧:进入CDE官网首页→点击"信息公开"→选择对应栏目。对于具体品种,输入受理号、药品名称或企业名称即可追踪审评进度。
②美国FDA——全球创新药市场的"风向标"
FDA是全球最重要的药品监管机构,其审批动态直接影响跨国药企及国内出海企业的估值。大家可重点关注:
Drugs@FDA数据库:涵盖所有经FDA批准上市或曾经上市的药品,可查询审批注册信息、专利数据、市场保护期等。
加速批准(Accelerated Approval)通道:2024年FDA通过该通道批准了多款重磅药物,如首款MASH药物Resmetirom、首款TIL疗法Lifileucel等,这类信息往往提前反映在临床数据发布阶段。
突破性疗法认定(Breakthrough Therapy):获得该认定的药物可享受快速通道待遇,FDA官网会实时更新认定名单。
③欧盟EMA与日本PMDA
对于布局海外市场的药企,EMA的集中审批程序(CP)和PMDA的先行审评制度同样值得关注,可通过其官网查询在审品种及审批结论。
二、第三方专业数据库:高效整合与深度分析
官方渠道信息权威但分散,专业医药数据库则通过渠道整合、可视化分析,大幅提升信息获取效率。
①摩熵医药(原药融云)——全球新药研发管线监测平台
摩熵医药的全球药物研发数据库覆盖已上市及处于各研发阶段的开发及发现药物,创新类型全面包含创新药、改良型新药、改良型生物制品、改良型疫苗、生物类似药,解决新药管线纵深要点:
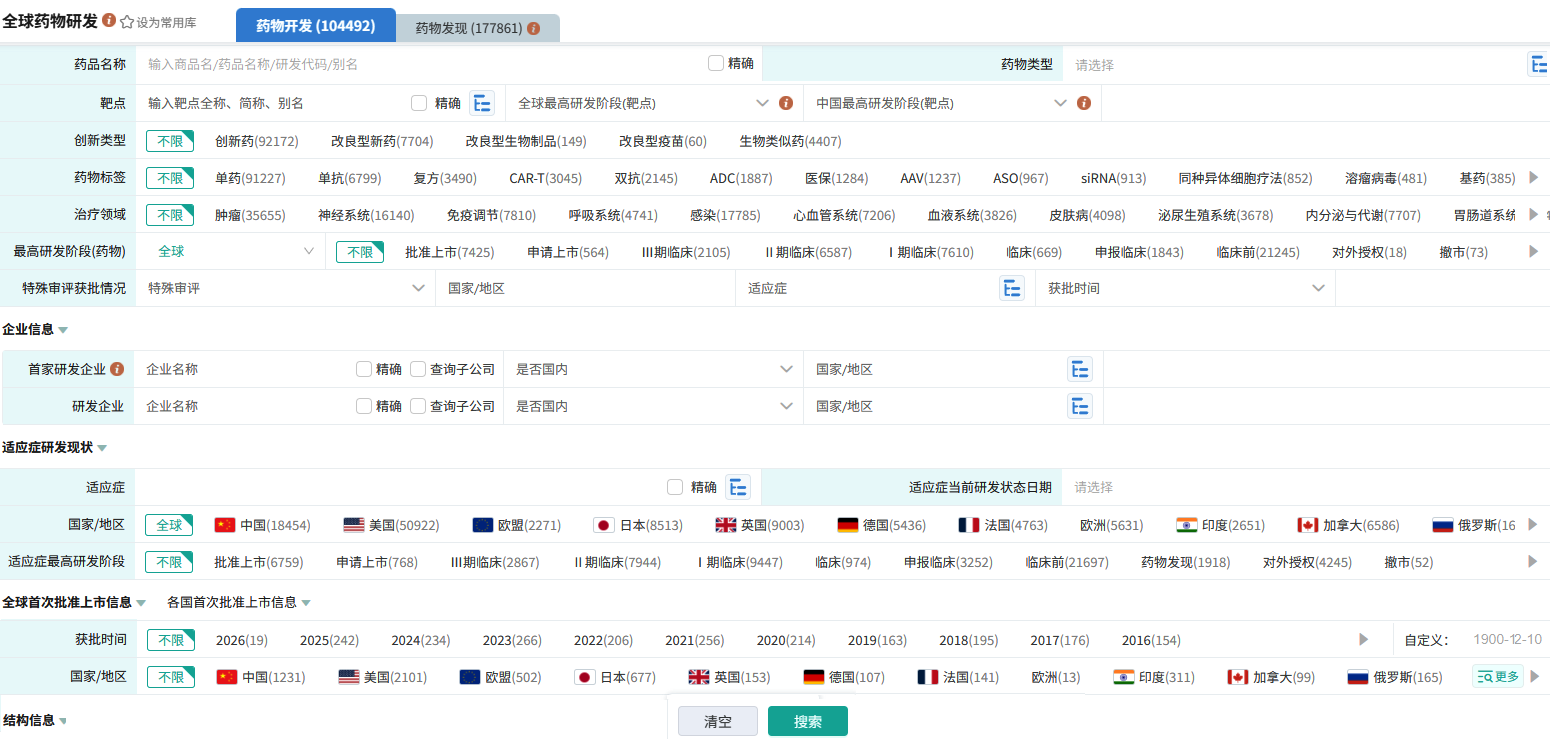
图源:摩熵医药-全球药物研发数据库
企业研发管线全景扫描:输入企业名称(可勾选查询子公司),一键获取其在研品种数量、适应症布局、靶点分布、研发阶段分布
历年全球新药上市统计:支持按适应症、获批时间、国家地区、特殊审批情况(如附条件批准、孤儿药认定)筛选,2023年全球获批上市新药237个,可通过可视化分析把握行业趋势
靶点赛道热度监控:选择特定靶点(如HER2、Claudin 18.2、KRAS等),查看全球及中国范围内各研发阶段的药物数量,评估竞争格局。
AI审评时间预测:基于历史样本数据,对新药、进口药、仿制药的审评完成时间进行预测,帮助判断催化剂兑现时点
药品审评时光轴:直观展示从CDE承办、技术审评到发件的各节点时长,识别审评延误风险,也支持按受理号、药品名称、活性成分、企业名称订阅,状态变化时通过站内信、邮件、微信推送提醒。
三、上市公司公告与研报会议:验证与前瞻
①定期报告与临时公告
根据监管要求,药企需在年报、半年报中披露主要研发项目基本情况,包括临床阶段、核心适应症、后续里程碑。临时公告则用于披露IND获批、临床试验完成、NDA受理、获批上市等关键节点。
②券商研报与行业会议
券商研报:关注医药首席分析师的"管线深度报告",通常包含DCF估值模型,量化特定品种的峰值销售预测。
学术会议:ASCO(美国临床肿瘤学会)、ESMO(欧洲肿瘤内科学会)、ASH(美国血液学会)等会议是重磅临床数据首发阵地,企业会提前发布摘要标题,会议期间公布详细数据。
四、信息获取的实战策略
①建立"监控清单"机制
对重点持仓或关注标的,建立包含以下要素的监控表:
核心品种受理号(用于CDE官网查询)
临床登记号(用于ClinicalTrials.gov或中国药物临床试验登记与信息公示平台查询)
预期里程碑时点(基于管理指引或AI预测)
②区分信息层级
一级信息:CDE/FDA官网的受理、审批公示,具有最高权威性
二级信息:数据库整合的进度分析、时间预测,用于提高效率
三级信息:券商研报、自媒体解读,需交叉验证
③警惕时间差风险
第三方数据库订阅功能获取信息快于市场,但需注意:CDE官网公示存在T+1或更长的滞后,重大进展企业有义务通过公告披露。建议以官方渠道为最终确认依据,避免基于非公开信息交易。
④关注特殊审评通道
突破性治疗药物程序:CDE自2020年实施,截至2024年已纳入数百个品种,审评资源倾斜明显。
附条件批准:用于治疗严重危及生命且尚无有效治疗手段的疾病的药品,基于早期临床数据提前批准,但需继续完成确证性研究
优先审评审批:针对临床急需药品、防治重大传染病和罕见病等疾病的创新药改良型新药
新药信息通过CDE/FDA官网+专业数据库+公司公告的三维信息体系,足以支撑大多数投资决策。关键在于建立系统化的监控机制,在信息发布的第一时刻做出反应,同时深入理解审评规则,判断里程碑事件对估值的真实影响。记住,在医药赛道,信息获取能力也是医药行业的核心竞争力。
注:本文提及的CDE审评报告公开政策自2021年6月1日起实施,新药应在获批上市后6个月内完成技术审评报告公开。投资者可通过CDE官网"信息公开-上市药品信息"栏目,双击品种栏下载完整审评报告。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论