
对于新药开发,制剂人想着如何在临床期间完成持续的样品供应,满足临床试验用药的需求;一旦药品上市,就要想着如何建立稳健工艺的持续生产,满足市场用药需求。制剂人一直在服务,想着我们制备的制剂产品,安全,有效,稳定,具有良好的顺应性且可持续生产。其实,在新药开发过程中,制剂人更关切的内容可以总结为:生物利用度,稳定性和可生产性,此三种要素共同驱动着新药的发现与开发,共同托举着一个新药的诞生,共同造就一个新药的商业化。
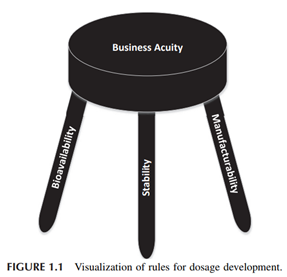
(来源于参考文献1)
药物无法单独进行给药,需要一定药物载体递送药物,发挥此种作用的物质可以称之为辅料。新药中固体制剂开发尤其鼎盛,如速释片剂与胶囊。固体制剂中离不开在处方中处于大多数的填充剂/稀释剂,又因处方中药物(1)剂量太低(2)和/或可压性较差,(3)和/或过润滑的出现或制剂需要崩解性能,往往填充剂-乳糖作为最佳选择而横空出世。
长期以来,辅料被视为惰性填充剂。现在正在发生一种转变,辅料越来越多地被视为功能性成分,其用途远远超出了其作为单纯的填充剂的存在。辅料为制剂提供了加工功能并将药物输送到需要的地方。批次间辅料的差异以及了解这种差异对辅料行为的影响对于应用开发至关重要。今天,我们不妨花点时间谈谈乳糖可能对于药物生物利用度,稳定性以及可生产性带来的影响。如果说药物的药物生物利用度,稳定性以及可生产性是驱动我们新药制剂开发的三驾马车,如何找到马车中驼驾的乳糖“背后隐藏的秘密”,以防被默默无闻的“傻白甜”被刺而导致药物研发破产,将是我们今后在药物开发中需要格外重视的事情。
三驾马车之一之生物利用度
辅料具有广泛特性,对最终药物产品很重要。欧洲和美国关于速释制剂生物豁免的监管指南要求深入了解辅料的生物药剂学影响,以便仅根据溶出度测试确定两种递送相同API的不同产品之间的生物等效性。图2总结了可能受辅料影响的生物药剂学过程。指导文件提到了一些关键的辅料,如甜味剂或表面活性剂。然而,许多辅料没有被提及,潜在相互作用的新机制仍在被发现。
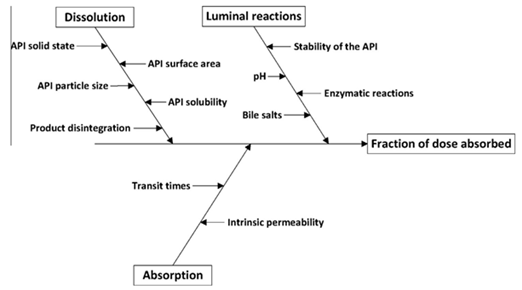
图2.可能受辅料调节的生物药剂学过程。(来源于参考文献2)
因为辅料在固体药物剂型中占有很大比例,占制剂总质量的99%(感觉文献中有点夸大),所以它们对质量属性的影响具有统计学意义。在体外和/或体内,辅料对药物溶解度、溶出及渗透性的影响,可能会影响口服的生物利用度和生物等效性。
乳糖是一种从牛奶中得到的二糖,由D-半乳糖和D-葡萄糖通过β(1-4)-糖苷键连接而成。乳糖主要用作处方的可溶性稀释剂。在37℃水中观察几种不同结晶形式的乳糖粉末,β-乳糖具有较高的初始溶解度和溶出速率,溶解度和溶出速率依次减小,顺序为β-乳糖(0.5g/ml)>α-乳糖无水形式(0.27g/ml)>α-乳糖一水合物(0.13g/ml)。α-乳糖一水合物和β-乳糖的崩解速度比无水乳糖快,压力的增加导致崩解时间增加。快速的崩解性归因于乳糖的多孔性,允许水分快速渗透。
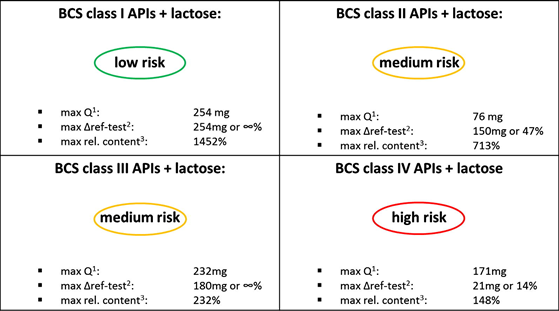
图3 BCS分类与乳糖用量差异造成BE不等效的概率(来源于参考文献2)
一般认为乳糖是默默无闻的“傻白甜”,根本不会把它与药物生物利用度不等效联系起来。很遗憾,有研究表明,乳糖可以通过多种机制对API的溶出造成影响,例如促进制剂的崩解、固体分散体的形成和颗粒的解聚,进而干扰药物的生物药剂学性质,对药物在体内的生物利用度和治疗效果产生影响。通过统计学分析,比较仿制药与创新药中乳糖用量的变化与BE不等效的关系,研究表明,BCS I类API的低概率和BCS II和III类API的中概率,而乳糖和BCS IV类API的组合被归类为高概率。
小结:乳糖似乎扮演者溶出调节剂的角色,影响着药物的生物利用度。
三驾马车之一之稳定性
一般而言,重要的标准是辅料在制备药物产品的整个保质期内保持惰性。然而,根据活性药物和辅料化学结构中的功能,它们可能会发生相互作用。乳糖是一种还原糖,因此可能与含有伯胺,仲胺基团的化合物发生美拉德反应。美拉德反应的反应性可能因浓度和其他条件而异。许多产品已成功地用乳糖配制而成,并且已被证明是稳定的。例如,群多普利是一种仲胺,与多种辅料(包括乳糖)具有热稳定性。与乳糖一起成功配制的产品的另一个例子是普瑞巴林,一种伯胺,硬明胶胶囊制剂,其中乳糖一水合物作为非活性成分。
在商业上,有些产品的活性药物成分是伯胺,并且含有低于75%的乳糖和非活性辅料。该产品在环境条件下约2年的保质期内不会出现美拉德反应。然而,当同一类型的产品含有超过95%的乳糖作为辅料时,尽管在最初一年不可见,但仍有可能发生相互作用。
下表是两个不同制造商提交的相同药品的比较。在这两种产品中,API都是含伯胺的化合物。此处,活性药物成分(API)相同,但产品I中有四种辅料,产品II中只有一种辅料与产品I相似但浓度不同。提供了在室温和加速条件下6个月的稳定性研究数据。产品1没有杂质趋势,所有数据都在范围内,因为乳糖浓度较低。然而,产品II在室温下呈上升趋势,结果几乎接近加速条件下的最高限值。在处方前研究中,公司没有观察到任何杂质增加的趋势,但在18个月的室温下,产品II有上升趋势,并且在24个月内肯定会超出限度。

表1 同一API不同处方组成(来源于参考文献3)
小结:如果你的产品具有伯胺或者仲胺,如果可以选择,尽可能避开还原糖,或许也是一种不错的选择。不害怕它出现(稳定性问题),就害怕它晚出现。
三驾马车之一之可生产性
众所周知,在速释口服固体制剂中,与胶囊相比,片剂更胜一筹,获得制剂人的青睐。若想窥探片剂开发中乳糖所发挥的作用,首先需要了解片剂的制备过程。一般来说,这包括两部分:(1)粉末从储存容器(有或没有机械搅拌和运输)、料斗流入压片模具;(2)粉末在压片机内的压实模具,在两个冲头之间成片。乳糖的流动使处方能够以均匀的形式快速进入片剂模具,从而实现恒定的体积/质量。对于压片处方,模具填充密度应高于0.5g/mL以确保良好的加工。由于乳糖有许多等级,新药制剂开发员需因“工艺”施之“不同级别之乳糖”,以保持中间体颗粒具有高堆积密度和良好的流动性(使片剂重量恒定)。

(来源于参考文献4)
DC是生产口服片剂的最简单方法,通常用于中高剂量制剂。根据生产分类系统(MCS),需要API自身具有良好的粉体学性质,同时也需要选择合适辅料。DC乳糖等级通常是喷雾干燥的(喷雾干燥的乳糖)、粒状的(制粒乳糖)或滚筒干燥的(无水乳糖)。喷雾干燥乳糖的无定形部分非常适合制造一定强度片剂,因为它具有延展性和良好的流动性。喷雾干燥的乳糖具有非常适合中低剂量配方的形态,因为其不仅结合了出色的流动性和可压实性,而且具有非常好的混合性能,同时还可以实现出色的含量均匀度。这是由产品的形态引起的,它是一种多孔聚集体,可以将制剂的其他成分(如API)保持在孔中。然而,由于喷雾干燥乳糖的表面积很大,它可能容易过度润滑。通过流化床制粒或高剪切制粒的制粒乳糖在压实和崩解性能方面表现出非常不同的方式。由于其腔体的储存能力,这两种颗粒状产品都适用于中高剂量制剂。制粒乳糖在润滑步骤中几乎没有负面的相互作用。无水乳糖,由于其非常小的β-乳糖微晶,具有出色的压实性能,可以制造出Ts最高的片剂。
DC工艺具有经济优势,而乳糖的安全性良好和成本还可以,似乎冥冥之中,乳糖挺适合于DC。那么后面的故事就是乳糖如何与DC“撒糖”。DC需要API与辅料能够更好的融合在一起,具有良好的流动性,可压性以及混合均匀性,且能在持续生产中保持稳定。这些中间体所呈现功能如何与乳糖和API的性质,如粒度及粒度分布,颗粒形态,颗粒间静电,颗粒表面粗糙程度等,建立一定的联系,通过控制乳糖和API的关键物料性质(CMAs)从而达到制剂产品(CQAs)。
总结:固体制剂开发之于新药开发,就如乳糖之于固体制剂一样的重要。那么,乳糖的性质,特别是关键物料性质,对于开发出合格的新药制剂产品,那是相当重要了。一直以来,乳糖所呈现的形象,可能仅仅是被选作为一种理所当然的口服固体制剂中的填充剂,有的时候乳糖在处方中的用量,乳糖的型号,似乎很自然的的在笔尖挥洒,不“加“思索。从本文来看,乳糖似乎又肩负着不一样的使命,控制着或者说影响着驱动新药制剂开发的三驾马车。乳糖似乎不再是坐在车上的“傻白甜”,更像是英勇地驾驶着马车的冲锋战士。
相关阅读:
《乳糖与微晶,固体制剂中的“金童玉女”?》
《制剂开发过程中关于亚稳态药物转晶的研究思路》
参考文献:
1. How to Develop Robust Solid Oral Dosage Forms from Conception to Post-Approval
2.Novel insights into excipient effects on the biopharmaceutics of APIs from different BCS classes: Lactose in solid oral dosage forms
3. Regulatory Notes on Impact of Excipients on Drug Products and the Maillard Reaction
4. Application of lactose in the pharmaceutical industry
5. Biopharmaceutical aspects and implications of excipient variability in drug product performance
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论