
2022年完结在即,据药融云数据库,截至2022年12月27日,今年已经有50多款新药在中国获批,其中包括16款1类新药。获批上市的1类新药中有4个进口新药和12个国产新药。
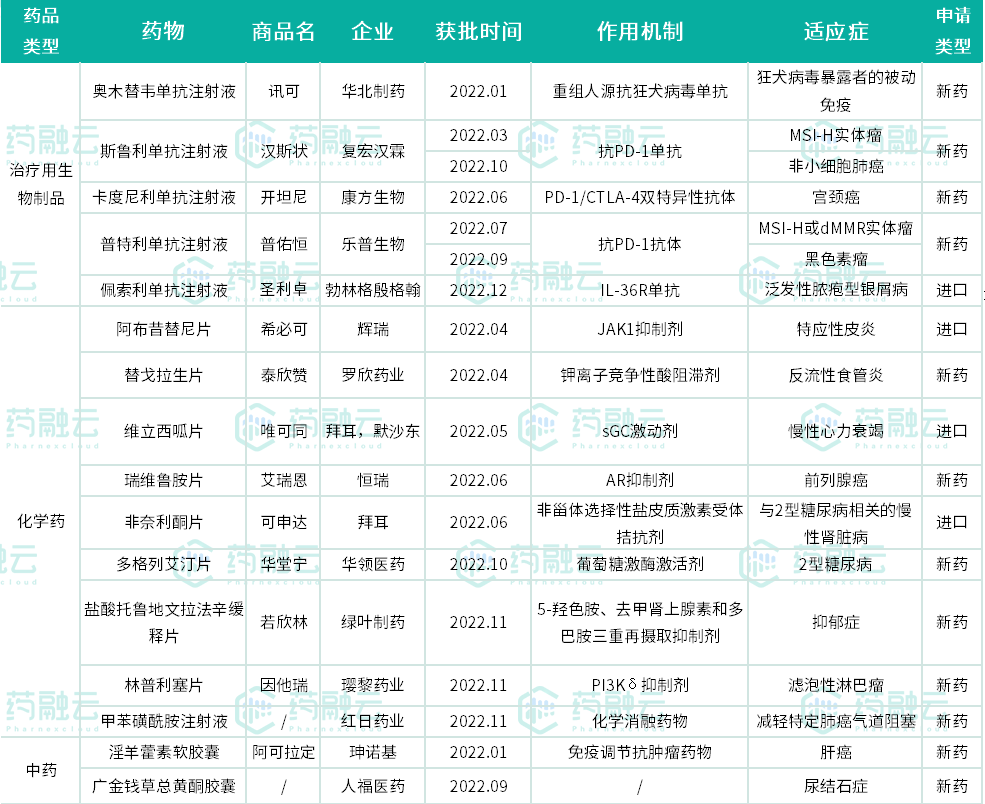
经过整理分析,可以发现,2022年获批上市的1类新药有以下几个特点。
一、小分子药物优势仍在
2022年获批上市的1类新药中,除开中药,治疗用生物制品有5个,小分子化学药则足有9个,占比约三分之二。这样的情形似乎昨日重现:在2021年获批上市的1类新药中,小分子化学药也几乎占据了三分之二。
可见,尽管近几年来各大公司的主要盈利产品中小分子药物比例越来越低,大分子药物的研发也如火如荼,但小分子药物依然是创新药品中的主流。
其中原因或与适应症有关。今年获批的5款生物制品,均为注射液剂型,主要集中在抗肿瘤和免疫调节领域。而化药新药除了甲苯磺酰胺为注射液外,其余均为片剂,适应症则相对广泛。除瑞维鲁胺片适用于前列腺癌、林普利塞片适用于滤泡性淋巴瘤外,其余7款新药均为非抗癌药物,适应症涉及消化系统、呼吸系统、心血管系统、神经系统等。
二、多个“首款”新药重磅来袭
新《药品注册管理办法》增加了4个药品注册快速通道,分别为突破性治疗药物、附条件批准、优先审评审批、特别审批。从2022年获批上市的1类新药来看,16款中有11款都是通过优先审评获得加速批准。
同时,今年有多款产品属于“首款”新药,具有一定临床意义:
华北制药的奥木替韦单抗是国内获批上市的首个用于成人狂犬病毒暴露者的被动免疫的单抗药物;
康方生物的卡度尼利单抗是全球首款获批的PD-1/CTLA-4双抗,同时也是我国首款获批的本土双特异性抗体;
恒瑞医药的瑞维鲁胺是我国获批的首个国产新型雄激素受体(AR)抑制剂;
璎黎药业的林普利塞片是我国首个高选择性PI3Kδ抑制剂;
绿叶制药的盐酸托鲁地文拉法辛缓释片是我国首个自主研发并拥有自主知识产权用于治疗抑郁症的化药1类创新药,是目前全球唯一一个从药物作用机制到临床效果均被证实的多重再摄取抑制剂(SNDRIs);
华领医药的多格列艾汀片是全球首个获批的葡萄糖激酶激活剂(GKA)类药物;
人福医药的广金钱草总黄酮胶囊是全球首创的防治尿结石症中药新药。
此外,卡度尼利单抗、普特利单抗、林普利塞、瑞维鲁胺和淫羊藿素软胶囊等均为附条件批准。附条件批准是指用于严重危及生命且尚无有效治疗手段的疾病、公共卫生方面急需的药品,现有临床研究资料尚未满足常规上市注册的全部要求,但已有临床试验数据显示疗效并能预测其临床价值,在规定申请人必须履行特定条件的情况下基于替代终点、中间临床终点或早期临床试验数据而批准上市。未来这几款附条件批准药物能否获得完全批准还取决于后续的临床试验数据。
三、8款1类新药或将首次国谈
此前国家医保局印发的2022年国家医保目录调整工作方案中明确2017年1月1日至2022年6月30日期间,经国家药监部门批准的新通用名药品可以申报参加。
若能顺利通过谈判纳入医保目录,将有望通过医保加速进院速度,从而实现产品的加速放量。经梳理,2022年获批上市的1类新药中有8款或可参与,分别是珅诺基的淫羊藿素软胶囊、华北制药的奥木替韦单抗、复宏汉霖的斯鲁利单抗、辉瑞的阿布昔替尼、罗欣药业的替戈拉生片、康方生物的卡度尼利单抗、拜耳的维立西呱片和非奈利酮片、恒瑞医药的瑞维鲁胺。
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论