
11月24日,CDE官网显示,泽璟制药1类新药 ZG006 的一项申请拟纳入突破性治疗,拟定适应症为 ZG006 单药治疗 DLL3 阳性的晚期神经内分泌癌患者。

截图来源:CDE官网
ZG006 是泽璟制药开发的一种靶向两个不同DLL3表位以及CD3的三特异性 T 细胞衔接器。该药的抗DLL3端可以与肿瘤细胞表面不同DLL3表位相结合,抗CD3端可以结合T细胞,进而利用T细胞特异性杀伤肿瘤细胞。
2025年7月,CDE已授予 ZG006 突破性治疗,用于单药治疗复发或进展的晚期小细胞肺癌患者。
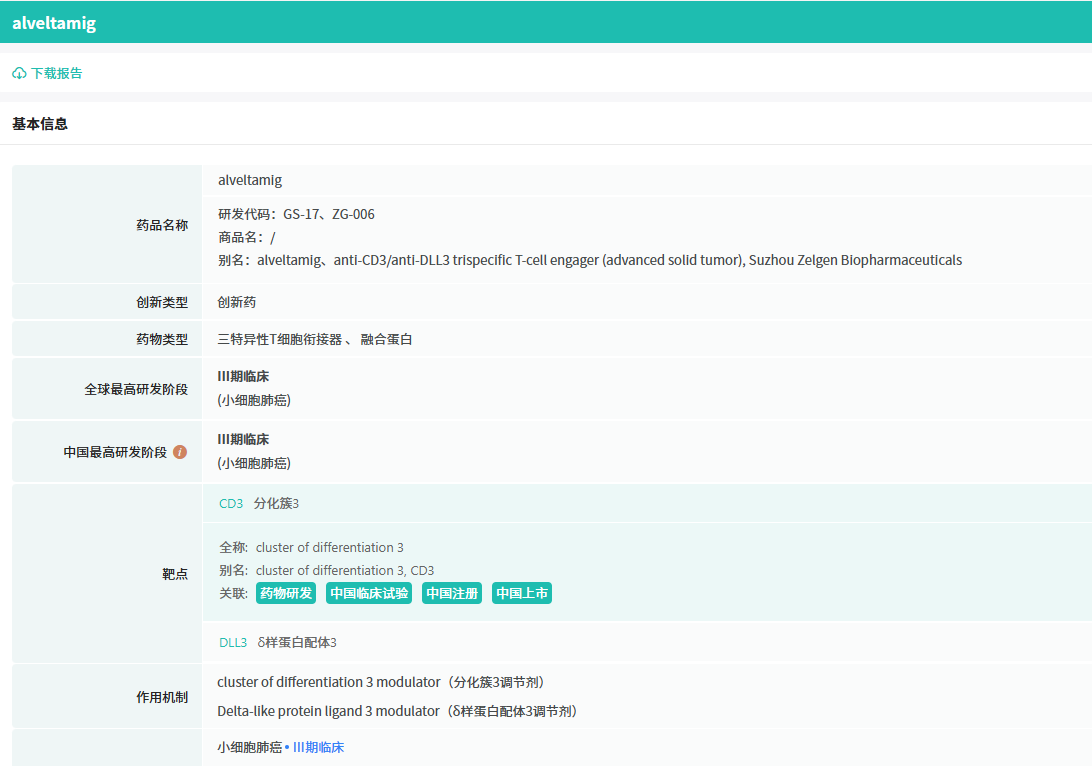
截图来源:摩熵医药数据库-全球药物研发数据库
本次拟纳入突破性治疗的申请针对的是一项新适应症:ZG006 单药治疗既往至少经含铂方案治疗后复发或进展的DLL3阳性(≥50% 的肿瘤细胞 DLL3 任意强度染色)的晚期神经内分泌癌患者。今年11月,美国FDA已授予 ZG006 治疗神经内分泌癌的孤儿药资格。
近年来,DLL3已成为SCLC、神经内分泌癌治疗的潜力靶点。据摩熵医药数据库显示,截止目前,全球共有超 30 款活跃的DLL3管线处于临床研究及以上阶段,成分类别包括 ADC、双抗、三抗、CAR-T、核药等等。
研究进度来看,目前只有安进的 塔拉妥单抗( CD3×DLL3 双抗)在海外获批上市。在国内,塔拉妥单抗已申报上市,目前正在审评中。泽璟制药的 ZG006 正在开展针对小细胞肺癌的 Ⅲ 期,不仅是进度最快的国产DLL3管线,也是全球范围内进度最快的靶向DLL3 的三抗药物。
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论