
2025年11月12日,全球细胞疗法领导者传奇生物科技公司(NASDAQ:LEGN)公布了2025年第三季度未经审计的财务业绩及公司主要重点。
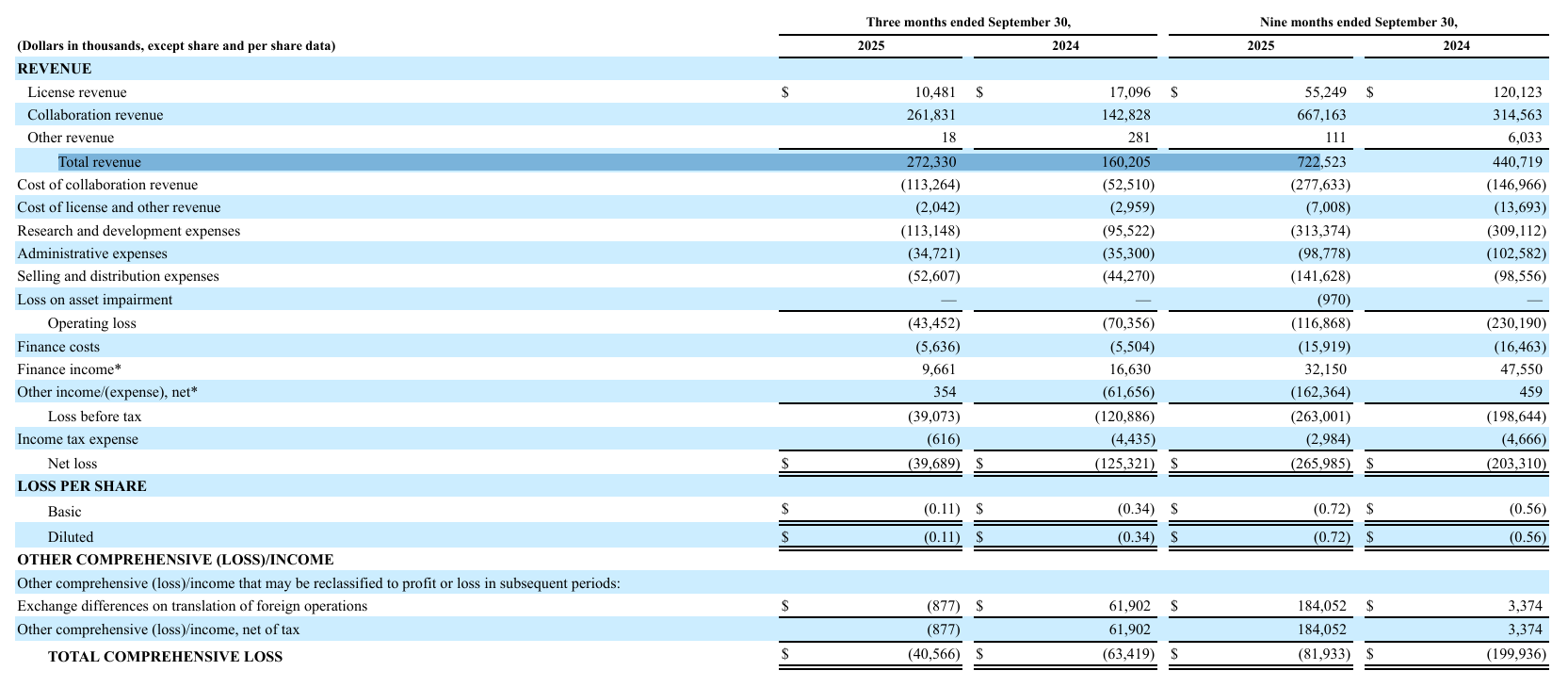
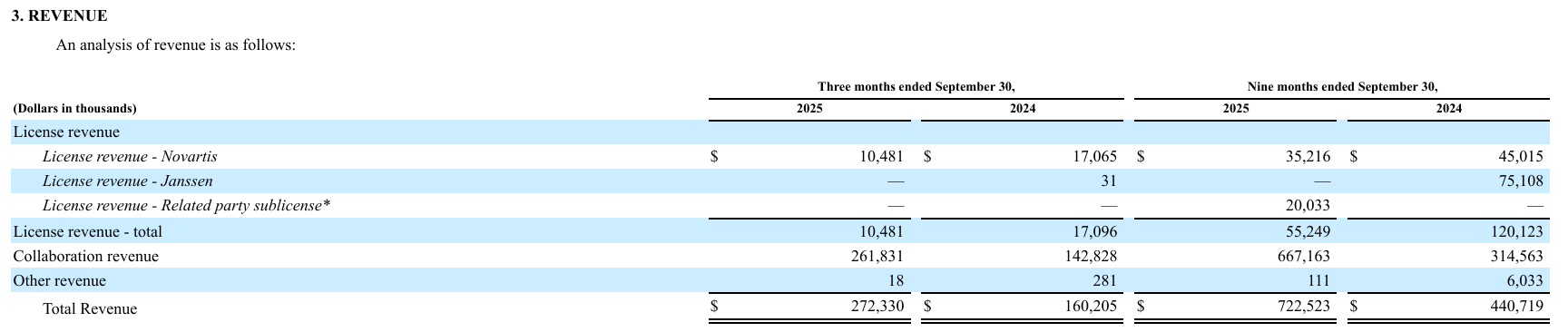
根据财报,截至2025年Q3,公司现金及现金等价物、定期存款总额约为10亿美元,Q3许可收入为1,050万美元,同比下降38.6%,下降的原因与相关临床试验活动的时间安排有关。该许可收入源自与诺华的许可协议,随着传奇生物开展 LB2102 I期临床试验,这一收入会随着时间的推移而得到确认。
Q3的合作收入为2.618亿美元,同比增加83.3%,增长的原因主要是由于与杨森合作与许可协议有关的 CARVYKTI® 销售产生的收入增加。Q3的研发费用为1.131亿美元,同比增加18.4%,主要是由于在研管线研发活动增加,以及BCMA靶点前线临床研究的投入。

值得注意的是,传奇生物与强生合作开发的BCMA CAR-T疗法 Carvykti 2025Q1-Q3销售额为13.32亿美元,同比增长112%,其中Q3销售额5.24亿美元!Q1和Q2分别为3.69亿美元和4.39亿美元,成功实现季度的持续增长,主要是因为1)在前线患者中渗透率提升,截至Q3美国市场需求中60%来自前线适应症;2)覆盖治疗中心增长,已覆盖美国治疗中心131个(包括38个社区医院),已覆盖全球治疗中心246个、今年以来非美治疗中心近乎翻倍。
Carvykti 适应症拓展:CARTITUDE-5和CARTITUDE-6 两项III期临床正在进行。2)突破产能瓶颈:公司预计至2025年底可支持年产能10,000例,其中比利时产能Techlane已于Q3投产,美国Raritan产能扩产有望H2就位。
Carvykti(通用名为西达基奥仑赛)是一款靶向B细胞成熟抗原的CAR - T疗法,用于既往接受过包括蛋白酶体抑制剂、免疫调节剂和抗CD38抗体的治疗方案,且在末次治疗期间或之后出现疾病进展的复发或难治性多发性骨髓瘤成年患者。
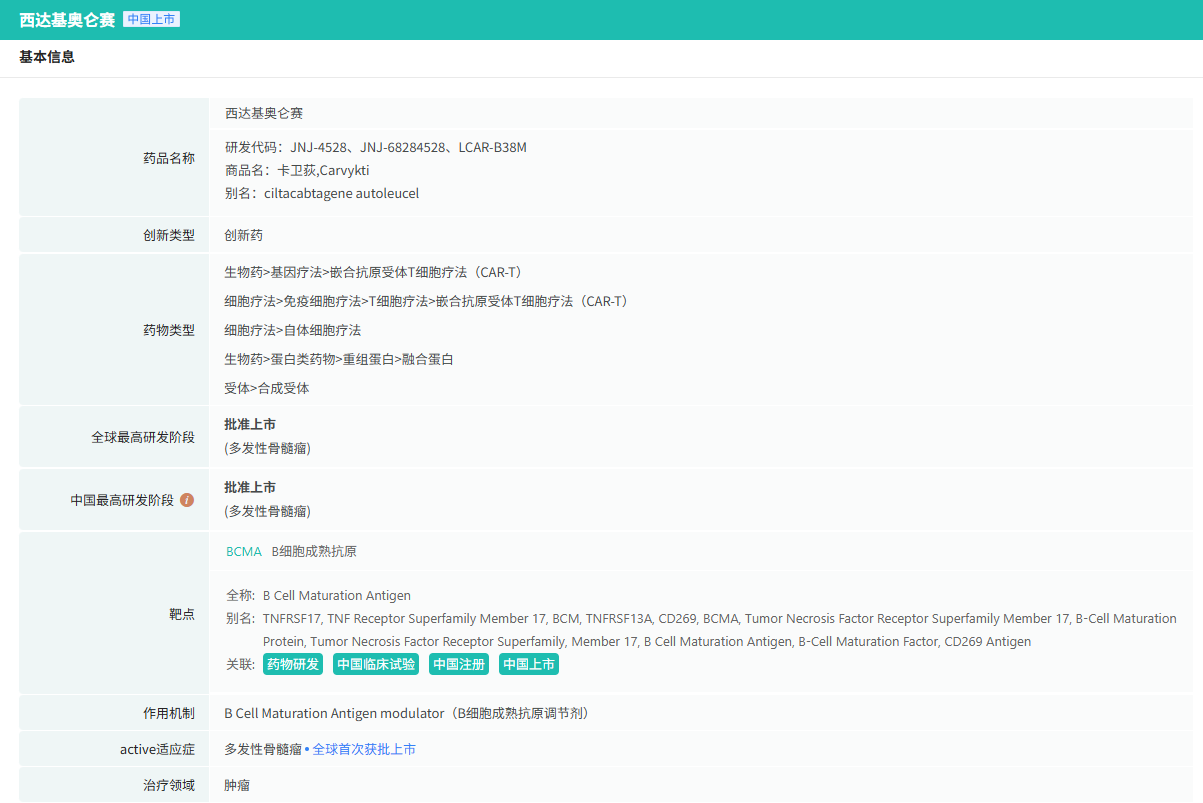
截图来源:摩熵医药数据库-全球药物研发数据库
Carvykti 2018年获中国国家药品监督管理局首个CAR - T临床试验申请批件,之后在全球多个国家和地区开展临床试验,并陆续获得多项认定和批准。2022年2月28日,美国上市申请获美国食品药品监督管理局批准;同年5月,欧盟委员会授予其附条件上市许可。
参考来源:
[1] 公司财报/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 传奇生物CAR-T疗法Carvykti营收大增388%
2. 传奇生物与强生豪掷1.5亿扩产,加速Carvykti剑指“重磅炸弹级”地位
3. 传奇生物:2025年CAR-T年产能将达10,000剂(附最新管线)
想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论