
当CAR-T在血液瘤领域大杀四方时,实体瘤的攻坚战谁来打?答案是TIL细胞疗法。2024年FDA首款产品获批,2026年中国本土研发井喷,君赛生物、华赛伯曼等企业频频刷新数据。本文将深度解读TIL细胞疗法最新进展,剖析TIL疗法是什么治疗方法,以及它如何成为癌症患者的新希望。
一、什么是TIL细胞疗法?有哪些优势与挑战?
在癌症治疗的浩瀚星空中,PD-1抑制剂是“解除封印的刹车”,CAR-T是“人工改造的导弹”,而TIL细胞疗法则是那支潜伏已久、最懂敌人的“天然特种兵”。
过去十年,免疫治疗彻底重塑了肿瘤治疗格局。但对于占癌症死亡人数绝大多数的实体瘤(如肺癌、肝癌、黑色素瘤),我们仍急需更强效、更持久的治疗手段。2026年的今天,随着上海君赛生物、华赛伯曼等中国企业的接连突破,TIL细胞疗法正从实验室的“贵族疗法”走向临床的“普惠方案”。
1. TIL疗法是什么治疗方法?
那么,TIL疗法究竟是什么?TIL细胞疗法(Tumor-Infiltrating Lymphocytes Therapy,肿瘤浸润淋巴细胞疗法)是一种利用患者自身免疫细胞来对抗癌症的创新方法。
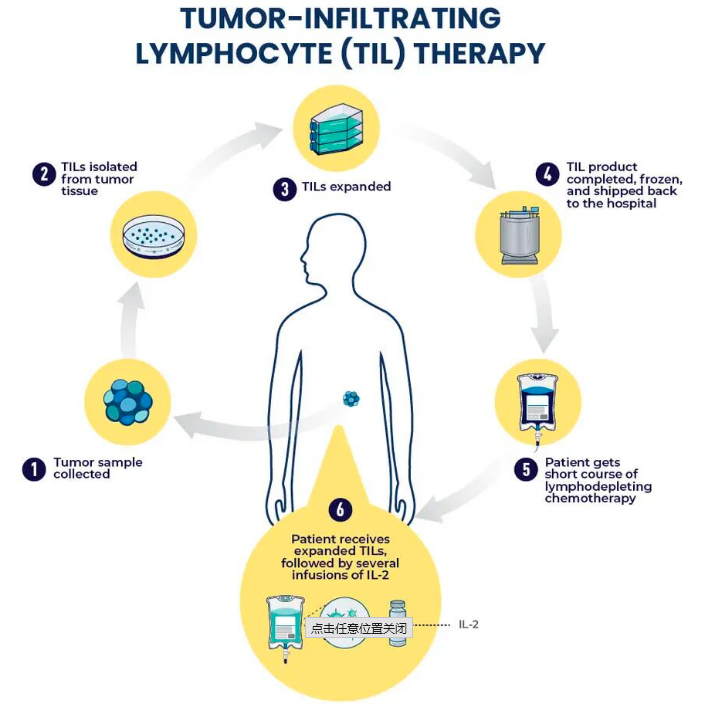
图片来源:NIH官网
治疗过程分为四个关键步骤:
(1)采集“抗癌尖兵”:通过手术或活检从患者肿瘤组织中提取浸润的淋巴细胞(TILs)。这些细胞天然具备识别患者自身肿瘤独特抗原的能力,是身体内最了解“敌人”的“特种部队”。
(2)体外“扩军备战”:在实验室中,利用先进的细胞培养技术,将数量有限的TILs扩增数百甚至上千倍,形成一支规模庞大的“免疫军团”。
(3)回输“强化部队”:将扩增后的TIL细胞回输到患者体内。传统方案需要配合高剂量IL-2(白细胞介素-2)支持细胞生存,但新一代疗法已实现“免清淋、免IL-2”的重大突破。
(4)精准“围剿作战”:回输的TILs凭借其天然的多靶点识别能力,精准定位并持续杀伤肿瘤细胞,实现对癌细胞的针对性清除。
2. TIL细胞疗法的优势
(1)天然识别能力:TIL细胞天然存在于肿瘤组织中,能够识别多种肿瘤抗原,无需像CAR-T那样进行基因改造。
(2)高效性:在高突变负荷的肿瘤(如黑色素瘤、肺癌)中,TIL疗法表现出较高的疗效。
(3)个体化治疗:由于使用的是患者自身的细胞,减少了排斥反应的风险。
3. TIL细胞疗法的挑战
(1)依赖肿瘤突变负荷:TIL疗法的效果很大程度上取决于肿瘤的突变负荷。在突变较少的肿瘤(如胰腺癌、卵巢癌)中,疗效有限。
(2)体外扩增导致的免疫疲惫:长时间的体外培养可能导致TIL细胞的功能下降和多样性降低。
(3)肿瘤微环境的抑制:肿瘤组织内的抑制性因素(如PD-L1、IDO、ARG1等)会限制TIL细胞的功能。
(4)回输后的持久性问题:传统TIL疗法依赖高剂量IL-2维持细胞生存,但高剂量IL-2会引起严重的副作用。
4. 技术升级:基因工程技术的应用
为了克服上述挑战,研究人员正在尝试通过基因工程技术对TIL细胞进行改造,以提高其疗效和持久性。
(1)去除“刹车”基因:通过基因编辑技术去除抑制T细胞反应的基因(如PD-1、CISH等),可以使TIL细胞维持更长久的活性。
(2)增加“追踪导航”能力:通过外源基因表达趋化受体(如CXCR2、CCR5),使TIL细胞能够更好地迁移到肿瘤部位。
(3)自带“能量补给”:通过导入特定细胞因子基因,使TIL细胞能够在肿瘤内局部分泌因子,提高其耐久性和安全性。
(4)装上“外挂武器”:将TIL细胞与人工识别系统(如CAR)结合,形成复合型TIL细胞,兼具CAR-T的精准性和TIL的浸润优势。
(5)保留“年轻态”:通过激活干性转录因子(如TCF-1、FOXO1)和富集记忆干性T细胞亚群,延长TIL细胞的寿命和记忆性。
二、TIL细胞疗法的发展历程
TIL细胞疗法并非一蹴而就的创新,其背后凝聚了科研人员数十年的探索与努力。早在20世纪80年代,美国国家癌症研究所(NCI)的Steven A. Rosenberg博士及其同事开创了这一领域的先河。
1980年代初:Rosenberg博士团队率先尝试从癌症患者血液中分离淋巴细胞,并发现IL-2是激活和长期培养T细胞的关键因子。1983年,重组IL-2的成功开发,使得大规模生产IL-2成为可能,为T细胞疗法的临床应用铺平了道路。
1985年:团队进行了首个涉及淋巴因子激活的杀伤细胞(LAK)的临床试验,验证了自体细胞回输的安全性和可行性。
1987-1988年:Rosenberg博士团队将目光转向了更精准的TILs。他们开展了首个利用自体TIL治疗转移性黑色素瘤的临床试验,并于1988年发表了初步结果。试验表明,在经过环磷酰胺清淋预处理的患者中,回输TIL并辅以IL-2治疗是安全可行的。
1994年:团队对86名接受TIL治疗的转移性黑色素瘤患者数据进行了总结。令人振奋的是,在那个靶向药和免疫检查点抑制剂尚未问世的年代,这项“原始”的细胞疗法取得了34%的客观缓解率(ORR)。
2000–2010年代:随后研究重点转向提高扩增效率、简化流程并拓展适应证:从传统需长期培养和筛选的“经典TIL”,发展到无需肿瘤反应性筛选的“Young TIL”,显著缩短制备周期并提高细胞活性,在黑色素瘤中观察到持久缓解。临床前和早期临床研究逐渐将TIL用于宫颈癌、肺癌等多种实体瘤,为后续产业化奠定基础。
2010–2020年代:2010年代后,企业化开发推动TIL疗法走向成熟:以Iovance为代表的公司对TIL制备进行标准化和规模化,开发出 lifileucel 等产品,并在黑色素瘤、宫颈癌等适应证中开展关键临床试验。
2024年2月,美国食品药品监督管理局(FDA)加速批准了Iovance公司研发的 Lifileucel(商品名Amtagvi)用于经治的不可切除或转移性黑色素瘤,成为全球首个获批的TIL疗法,也是首款获批用于实体瘤的T细胞疗法,标志着TIL疗法正式进入临床应用时代。
Lifileucel基本信息查询
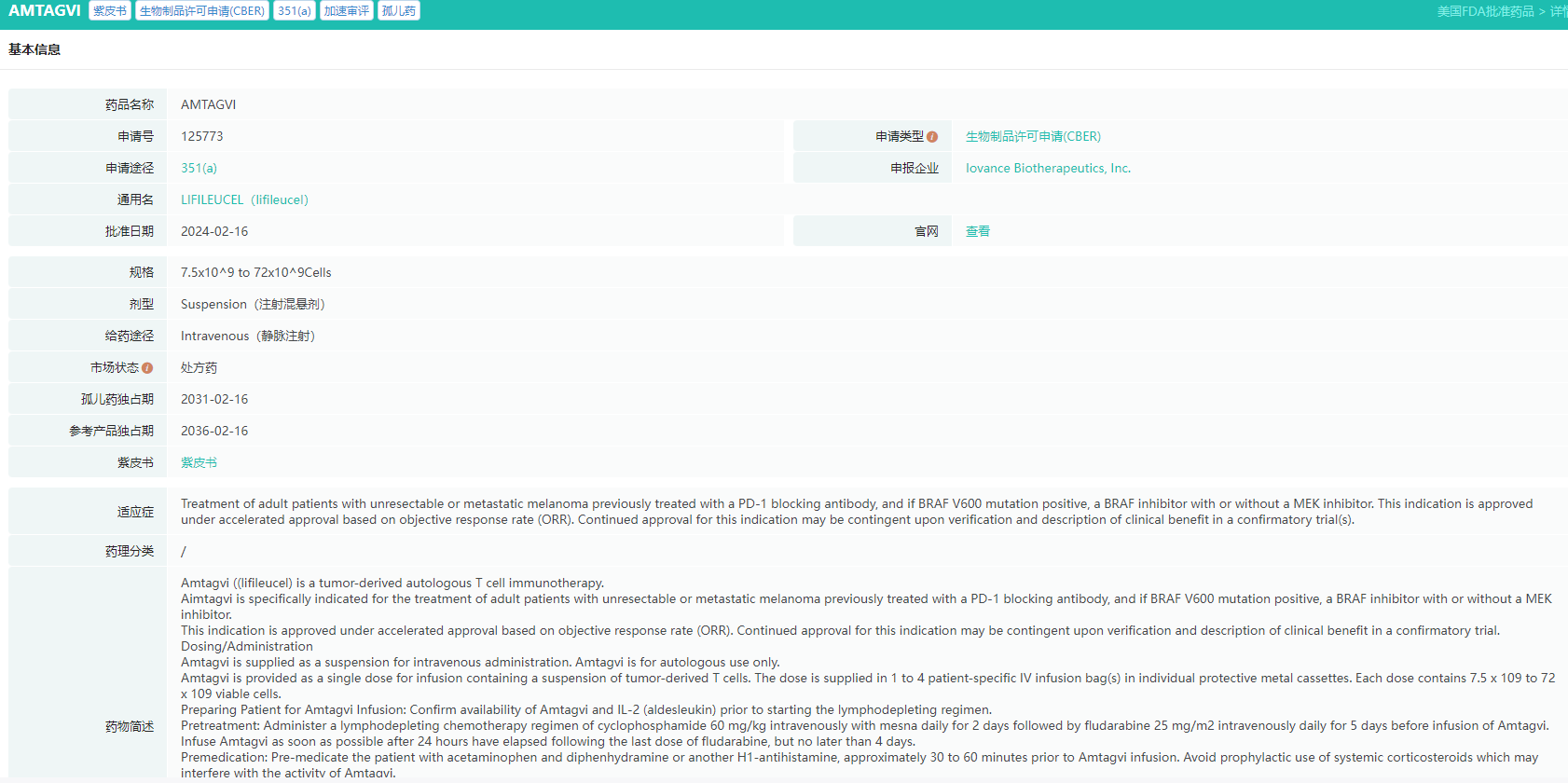
查数据,找摩熵!图源:摩熵医药-美国FDA批准药品数据库
三、TIL细胞疗法的竞争格局及最新进展
全球TIL疗法领域呈现出“一超多强、分化加剧”的局面。以Iovance为首的第一梯队已跨过商业化门槛,而以Obsidian、KSQ为代表的第二梯队正通过基因改造技术试图实现“弯道超车”。与此同时,中国企业凭借在工艺上的快速迭代和临床资源的优势,正在成为不可忽视的重要力量。
据摩熵医药数据库统计,截止目前全球已有超过120条TIL疗法管线,主要适应症涵盖黑色素瘤、非小细胞肺癌、宫颈癌、头颈部鳞状细胞癌以及卵巢癌等。在国内,已有近20家企业布局TIL疗法,其中4条管线处于临床Ⅱ期,6条处于临床Ⅰ期,预计未来有望迎来新的突破。
KSQ Therapeutics:KSQ-001EX(KSQ-001)是一种由CRISPR/Cas9基因编辑技术进行工程改造的新型TIL疗法,目前处于2期临床试验阶段。KSQ-001EX 由TIL(肿瘤浸润淋巴细胞)组成,通过CRISPR/Cas9基因编辑技术来抑制SOCS1。SOCS1(细胞因子信号转导抑制因子1)是T细胞内的一种“刹车”蛋白,敲除它相当于解除了T细胞的限制,使其对细胞因子更敏感,增殖能力更强,抗肿瘤活性更持久。
KSQ-001EX全球研发状态/进度查询
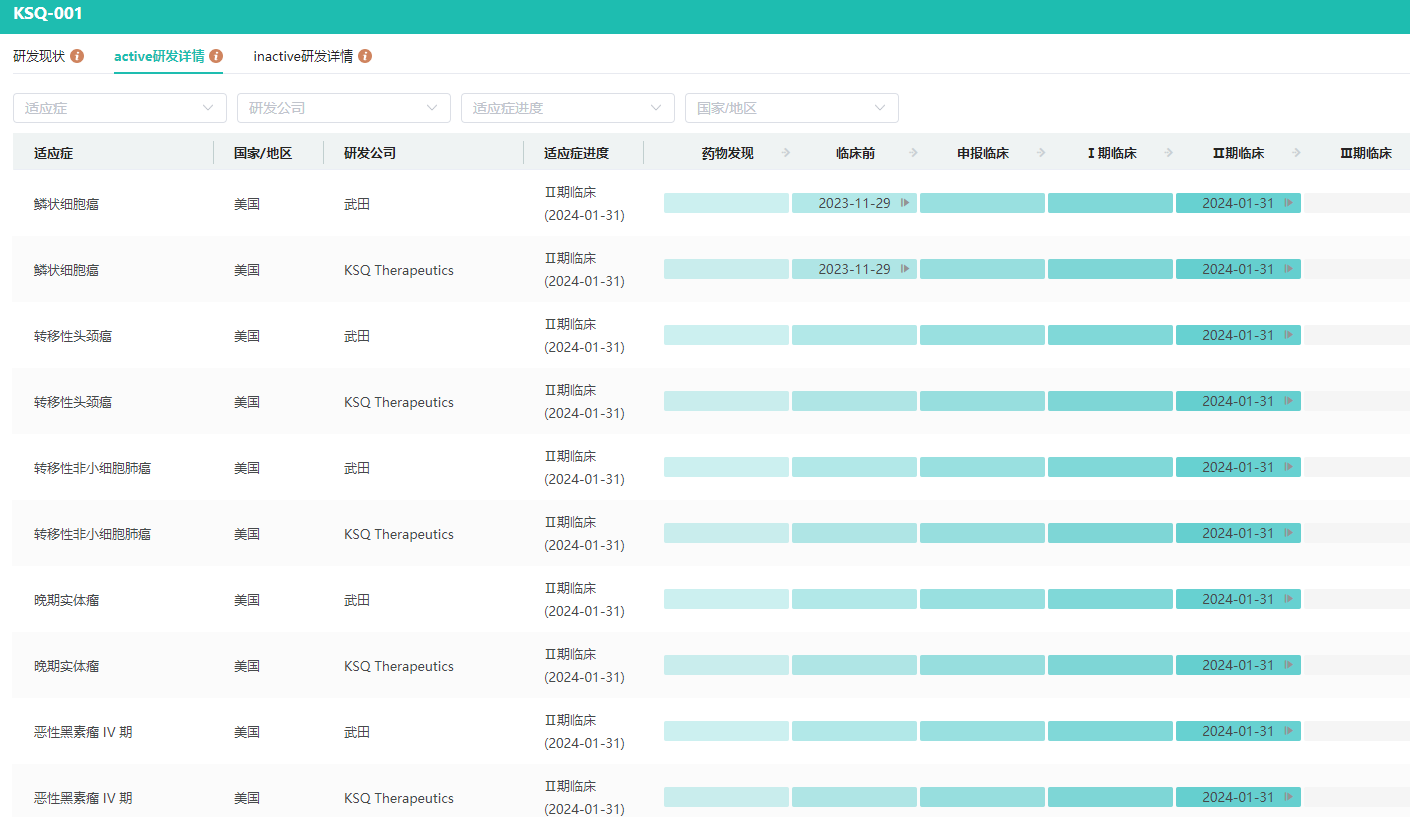
查数据,找摩熵!图源:摩熵医药全球药物研发数据库
Obsidian Therapeutics:OBX-115 是一款基于“cytoDRiVE”平台开发的基因工程化TIL,目前处于2期临床试验阶段。其核心在于转入了一个膜结合的白介素-15(mbIL-15)基因,且该基因的表达受一种小分子药物(乙酰唑胺)的调控。这种设计旨在利用IL-15替代高毒性的IL-2,实现T细胞的自我维持与增殖。
华赛伯曼:该公司自主研发的 FAST-TIL(HS-IT101,临床II期)在2025年欧洲肿瘤内科学会(ESMO)年会上首次公布了I期临床试验数据。FAST-TIL 针对传统TIL疗法的痛点进行了突破性创新,具有IL-2依赖程度更低、肿瘤组织需求量更少、生产时间更短等多项优势。
君赛生物:其研发的 GC-101 是全球首款无需清淋、无需IL-2注射的天然TIL疗法。目前针对多种晚期实体瘤处于临床2期研究阶段,有望成为中国首个获批上市的TIL疗法。其最新公布的临床数据显示,GC101 在标准治疗失败的晚期非小细胞肺癌患者中,客观缓解率达到41.7%,疾病控制率为66.7%。此外,君赛生物的另一款产品 GC-203(处于I期临床)是全球首创的非病毒载体基因修饰TIL疗法,在晚期卵巢癌患者中疾病控制率高达83.3%。
沙砾生物:该公司的 GT-101 是中国首个进入临床的TIL产品,用于治疗复发或转移性宫颈癌,目前处于2期临床阶段。I期临床试验结果显示,在11例宫颈癌患者中,客观缓解率为45.5%,疾病控制率高达90.9%。另一条管线 GT201,处于1期临床,属于第二代基因工程化TIL,表达膜结合IL-15。沙砾生物还开发了CRISPR双敲的TIL产品 GT-316,在多线治疗失败的妇科肿瘤患者中取得了超过32周的完全缓解。
蓝马医疗:其自主研发的TIL疗法 LM-103注射液 已进入关键性临床研究阶段,成为国内首个针对恶性黑色素瘤且无需联合PD-1等抗肿瘤药物就进入关键II期临床试验的TIL疗法。
LM-103注射液(CTR20254771)临床试验信息查询
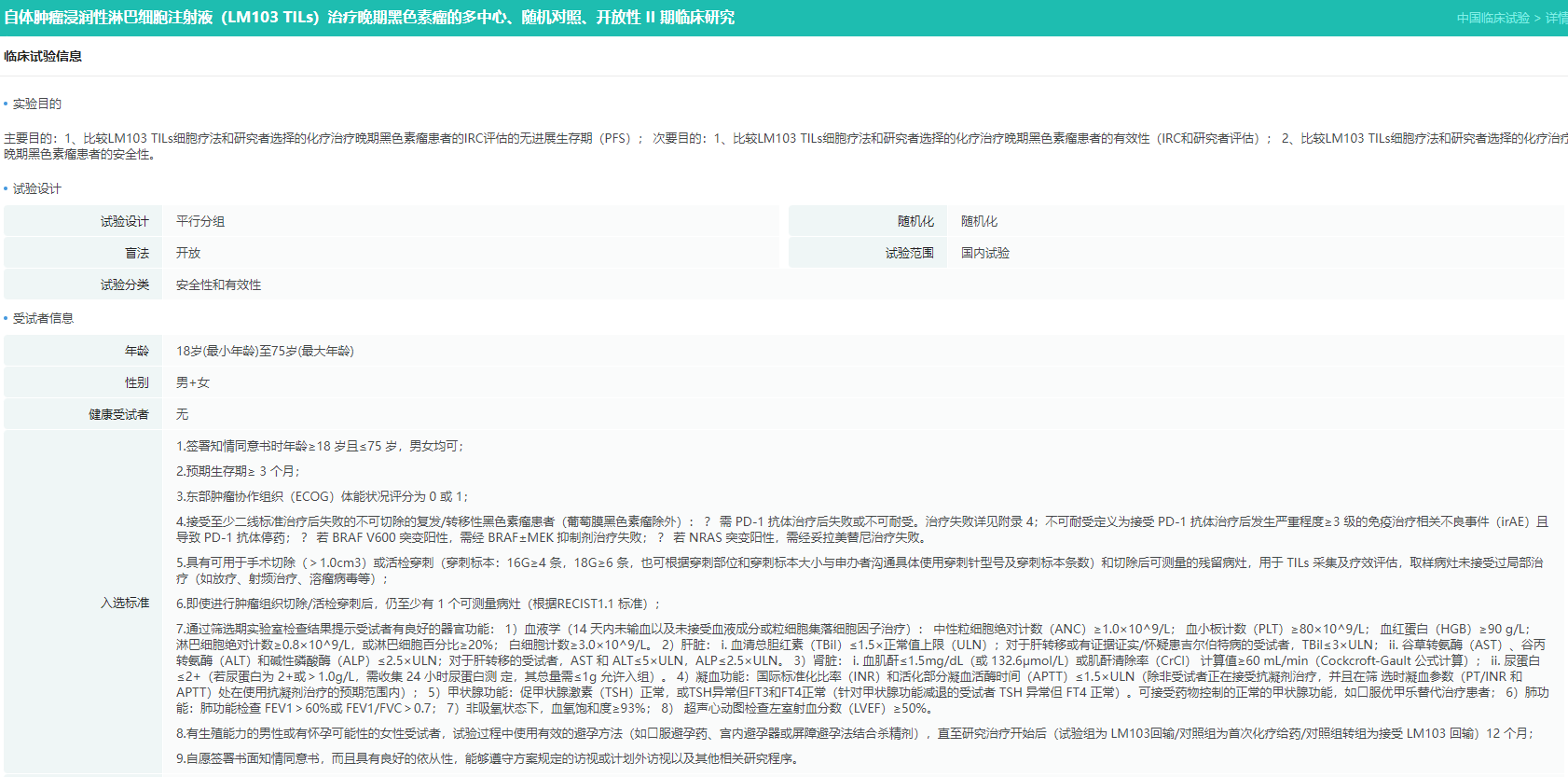
查数据,找摩熵!图源:摩熵医药中国临床试验数据库
百吉生物:研发的 BST-02 是全球首款针对肝癌的TIL疗法,目前处于I期临床阶段,具有可冻存、无需高剂量IL-2等优势。I期临床试验中,一名受试者在接受 BST02 回输18周后,靶病灶完全消退。
卡替医疗:创新性地从外周血中分离类TIL细胞进行基因修饰,用于治疗胆道肿瘤。一项发表在《Cell Reports Medicine》上的概念验证研究显示,这种ScTIL疗法在晚期胆道肿瘤患者中取得了显著的疗效,治疗组和对照组的疾病控制率分别为100%和0%,中位总生存期分别为18.3个月和3.2个月。
四、从“天价药”到“普惠药”:成本、可及性与未来商业模式
任何一项创新疗法,最终能否惠及广大患者,关键在于其可及性,而成本是决定可及性的核心因素。全球首款TIL疗法 Lifileucel 定价高达数十万美元,这无疑为许多患者设置了很高的门槛。如何将TIL疗法从“天价药”变为“普惠药”,是整个行业面临的重大课题。
中国企业在这一方面正展现出巨大的潜力与决心:
本土化研发与生产:通过自主研发和规模化生产,国内企业有望大幅降低TIL疗法的制造成本。君赛生物和华赛伯曼均公开表示,其生产成本远低于海外同类产品,例如,华赛伯曼的 FAST-TIL 成本据称仅为 Amtagvi 的十分之一、Search Result 君赛生物的生产成本也不及Iovance的10%。
技术创新驱动成本下降:
(1)自动化生产:引入自动化、封闭式的细胞制备系统和新型生物反应器,可以减少人力成本,提高生产效率和成功率,是降低成本的关键。有研究预测,自动化生产可使TIL制造成本降低30%,长期来看甚至有望降低三分之一。更有机构的目标是通过自动化将成本降低90%以上。
(2)简化治疗方案:如君赛生物的“免清淋、免IL-2”方案,不仅降低了药品本身的生产成本,更大幅削减了患者住院、ICU监护、以及处理严重不良反应等相关的巨额医疗费用,从整体上降低了治疗的总成本,让TIL疗法更易于在更广泛的医疗机构中推广。
(3)商业模式探索:未来,随着技术的成熟和成本的下降,TIL疗法的商业模式也可能更加灵活,例如探索按疗效付费、金融保险合作等模式,进一步提高患者的可及性。
可以预见,在技术创新和本土化生产的双重驱动下,中国将有望率先实现高性价比TIL疗法的普及,为中国乃至全球的实体瘤患者提供更可及的生命新希望。
结语:
TIL疗法作为第三类免疫治疗的核心手段,正逐步从实验室走向临床。随着基因工程技术的持续进步,TIL疗法有望实现更高的疗效、安全性与可及性。未来,该疗法或将具备感知肿瘤微环境、智能释放治疗因子、自动调节活性与持久性的能力,为更多癌症患者带来新的希望。我们有理由相信,TIL疗法将与手术、放疗、化疗、靶向治疗等传统手段协同应用,为人类攻克癌症这一顽疾贡献更大力量。
扩展阅读:
2. 全球首款TIL细胞疗法lifileucel欧盟申报上市!
3. 华赛伯曼:首款TIL细胞疗法获批临床,用于治疗晚期实体瘤
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论