药融圈获悉:2023年2月中旬,继“293XS细胞库”之后(宜明细胞“悬浮293XS细胞库”完成在美国FDA的DMF备案),宜明细胞自主驯化的另一细胞库“HEK293T细胞库”也完成了向美国FDA的DMF(Durg Master Files, 药品主文件)备案,并已收到确认函,备案号为DMF 29108(见图1)。
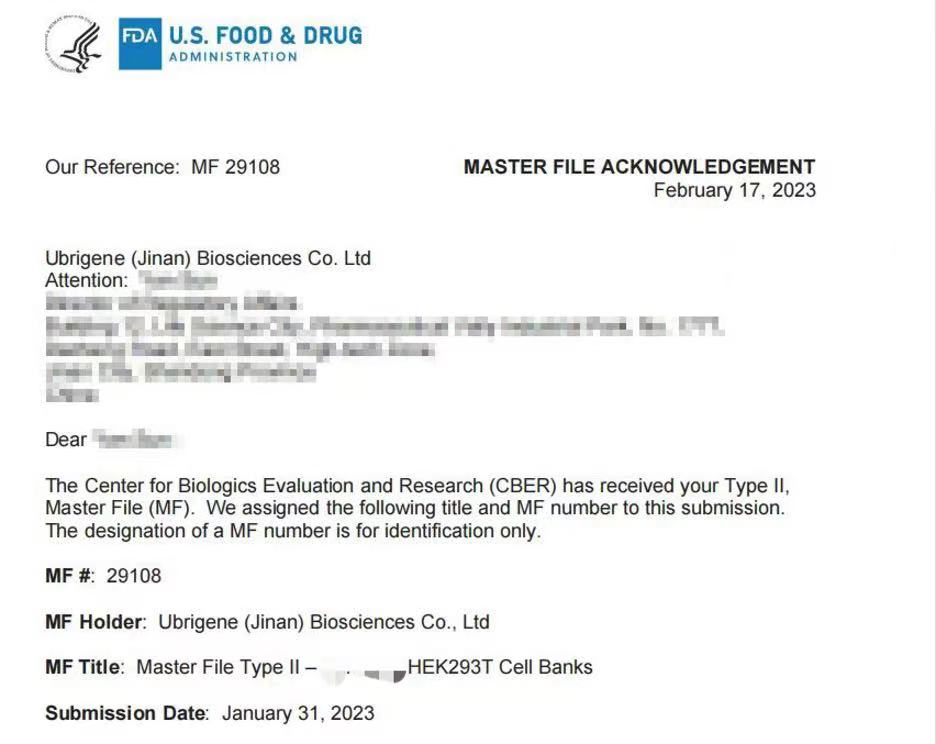
图1:宜明细胞用于慢病毒生产的293T细胞库完成在FDA的DMF备案
这一HEK293T细胞库用于慢病毒载体的大规模生产,2022年,由宜明细胞生产且获批IND的微知卓的基于慢病毒的人工肝项目,所使用的就是该细胞库(见图2)。未来,宜明细胞客户的慢病毒项目在向FDA进行IND申报时,可直接引用相应的DMF备案号,缩短产品审查和评估时间,加速相关药品的项目申报进程。
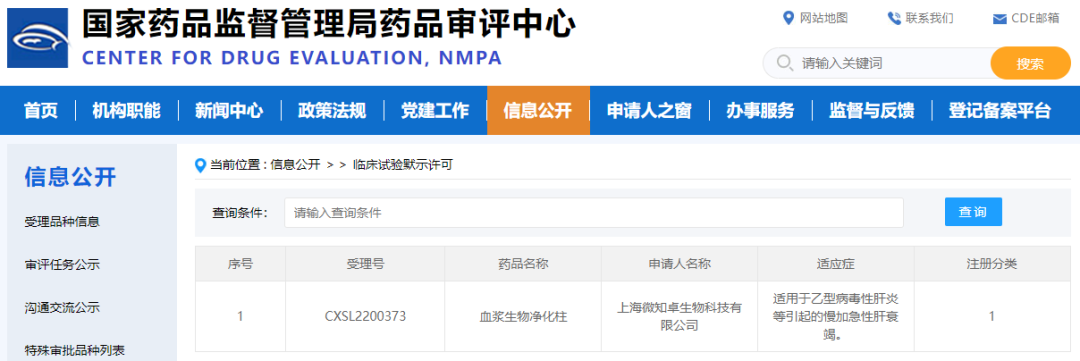
图2:微知卓中国首个生物人工肝产品(血浆生物净化柱)的临床试验申请(IND),用于治疗乙型病毒性肝炎等引起的慢加急性肝衰竭。
DMF是指原料供应商递交给FDA的药物存档文件,包含药物产品在生产、操作、包装和储存过程中用到的设施、操作流程、原料等保密细节信息。根据美国联邦食品、药品和化妆品法等规定,药品在上市之前必须向FDA提出相关的申请(如临床研究申请(IND)、新药注册(NDA)和生物制品许可证申请(BLA)等),并需要提供该药物在安全性、有效性和质量三方面的全部信息,其中还涉及到原料药以及辅料等相关技术内容。这些信息不仅繁冗复杂,而且涉及保密需求。DMF体系于是应需而生。
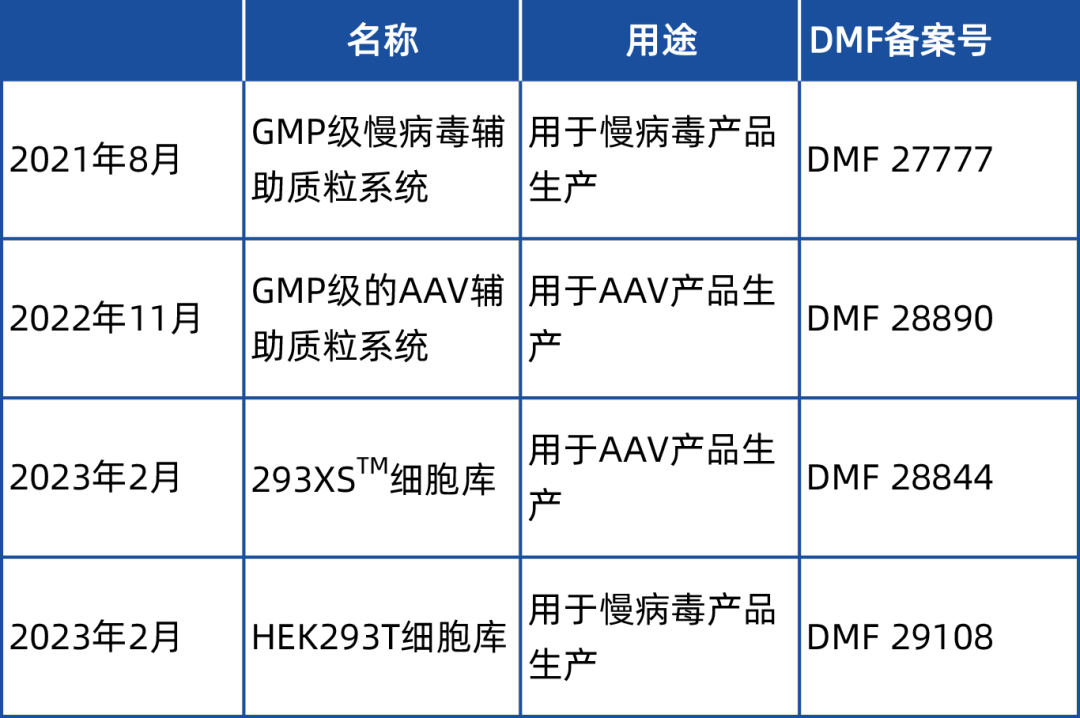
宜明细胞将以上信息以DMF文件的形式在FDA备案并获得相应产品的DMF备案号,迄今为止,已有四项自主研发品种完成在美国FDA的DMF备案(见表1),为宜明细胞客户在基于慢病毒以及AAV载体项目的在美申报中节约了审批成本、提高了审批效率、并且缩短了注册周期。
表1: 宜明细胞已有四项自主研发品种完成在FDA的DMF备案
(截至2023年2月)
宜明细胞董事长兼CTO孙秀莲博士说:“自2022年蓝鸟生物的两款慢病毒载体基因治疗药物获FDA批准上市,慢病毒载体在CGT领域又掀热潮。我很高兴我们自主驯化的HEK293T细胞库以及GMP级慢病毒辅助质粒系统都已获得FDA的DMF备案号,这极大地提高了客户慢病毒产品在美国申报的效率。宜明细胞作为一家CDMO服务商,以客户需求为导向,通过不断的技术创新开发稳健的病毒载体平台,为CGT新药企业提供高性价比的可扩展解决方案,节省资金与时间成本,助力客户项目的商业化成功,让新药好药多、快、好、省地惠及患者。”
关于宜明细胞
宜明细胞生物科技有限公司(Ubrigene)成立于2015年10月,是一家致力于基因治疗和细胞治疗(CGT) 技术的开发和应用、能够为CGT 产业化提供整体解决方案的研发生产型生物技术公司。宜明细胞在中国苏州和济南建有GMP基地,数十条质粒、病毒、细胞治疗药物生产线,总面积超过一万平,在美国和加拿大建有CMC研发中心,可向CGT客户提供GMP质粒、AAV、慢病毒、溶瘤病毒、CAR-T、IPSC制备的CDMO服务。 宜明细胞拥有专业的技术团队、完善的GMP 体系及成熟的项目经验,可满足客户早期研发、研究者发起的临床(IIT)、新药临床试验申报(IND)和 I/Ⅱ/Ⅲ 期临床试验、商业化生产的要求,支持中美双报,全方位为CGT客户提供从工艺开发、小试、中试到临床样品生产的一站式CDMO 服务,帮助客户加速基因及细胞药物的研发、临床试验和上市。 宜明细胞定位于生物与健康产业,坚持以成为生物医药的引领者、生命科学的推动者为使命,以推动研发国人用得起的新型生物药为己任,让基因及细胞药物早日惠及更多的患者。
<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论