
据药融云数据库显示:2023年5月12日,安斯泰来/Astellas的口服Fezolinetant新药Veozah®在美国首次获批上市,基于两项关键3期临床试验 SKYLIGHT 1和SKYLIGHT 2,以及 3 期长期安全性研究SKYLIGHT 4的结果。当前美国市场定价为每月550美元,全年费用约6600美元。
药融云数据库显示:Fezolinetant是一种正在进行开发的口服NK3受体(Neurokinin 3 Receptor)拮抗剂类非激素治疗药物,用于治疗绝经相关中重度血管舒缩症状(VMS,vasomotor symptoms)。Fezolinetant通过阻断神经激肽B(NKB)与Kisspeptin/神经激肽/强啡肽(KNDy)神经元的结合,调节脑(下丘脑)体温调节中枢的神经元活动,以降低绝经相关中重度VMS的发生频率和严重程度。本品最早由GPCR领域公司比利时Ogeda(前身Euroscreen S.A.)开发;2017年4月,Astellas以5亿欧元首付价格收购获得。相关专利:国内专利公开号CN102906093B,WO2011121137。
此前有机构预测:2028 年,Fezolinetant的销售额将达19亿美元。
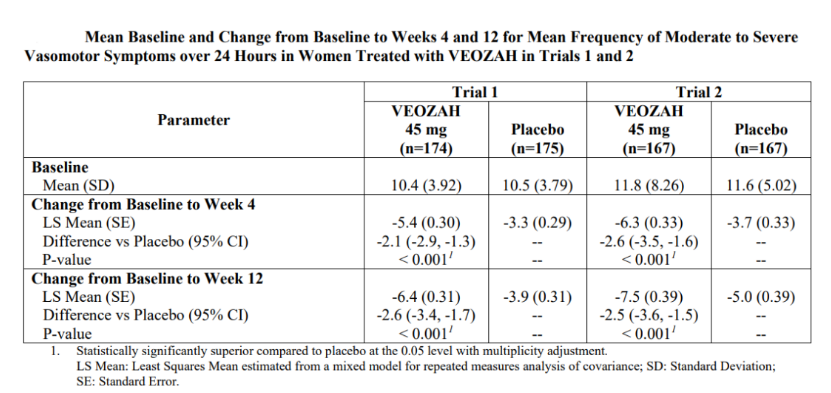
2022年9月,涵盖中国的相关临床数据披露,该研究的主要终点不良事件(AE)的发生频率和严重程度,基本与既往Fezolinetant III期研究结果相一致。MOONLIGHT 1™(NCT04234204)旨在研究Fezolinetant(30mg剂量)治疗亚洲女性绝经相关中重度VMS的有效性和安全性。试验前12周为双盲、安慰剂对照治疗期,随后12周为非对照扩展治疗期。
该试验在中国大陆、中国台湾和韩国的近60个研究中心共招募了302名绝经相关中重度VMS的女性患者。MOONLIGHT 3™(NCT04451226)是一项为期52周的单臂Ⅲ期临床试验,旨在评价Fezolinetant在绝经相关VMS的中国大陆女性患者中的长期安全性和耐受性。该试验在中国大陆的34个研究中心共招募了150名女性受试者。对于安全性问题,Fezolinetant不能与CYP1A2抑制剂一起使用,且患有肝硬化、严重肾损害或终末期肾病的患者不可以服用。
VMS是绝经期的常见症状,表现为潮热和/或盗汗。在全球范围内,40至64岁女性中50%以上经历过VMS。在东亚,40至64岁女性中约有80%经历过VMS,其中55%为中重度VMS。VMS会降低女性的日常活动和总体生活质量。
参考:
NMPA/CDE;
药融云数据库
FDA/EMA/PMDA;
相关公司公开披露;
https://www.astellas.com/en;
ClinicalTrials.gov;等等
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论