
据CDE官网显示,南京美瑞制药递交的4类仿制化药米拉贝隆缓释片的上市申请获受理。目前,国内已有4家企业的米拉贝隆缓释片获批并过评。
截图来源:CDE官网
米拉贝隆原研产品由安斯泰来开发,它是第一个用于治疗膀胱过度活动症的β3肾上腺素受体激动剂类药物,用于治疗成年膀胱过度活动症患者尿急、尿频和/或急迫性尿失禁的治疗。
米拉贝隆于2011年首先在日本上市(商品名为Betanis),2012年6月在美国获批上市(商品名为Myrbetriq),随后相继在英国、欧洲和加拿大等国家和地区上市。2017年9月获NMPA批准,商品名为贝坦利,2018年5月底正式上市销售。2020年,米拉贝隆通过医保谈判,成功进入国家医保目录(乙类)。
根据安斯泰来财报数据,米拉贝隆市场近年持续增长,2021年全球销售额为1723亿日元(约合88.4亿元),2022年全球销售额达1883亿日元(约合96.6亿元),同比增长9.5%。
该药物的国内市场,正在快速扩容中。据药融云数据库,2021年米拉贝隆缓释片院内销售额呈上升趋势;2022年销售超3千万元,同比增长167%。
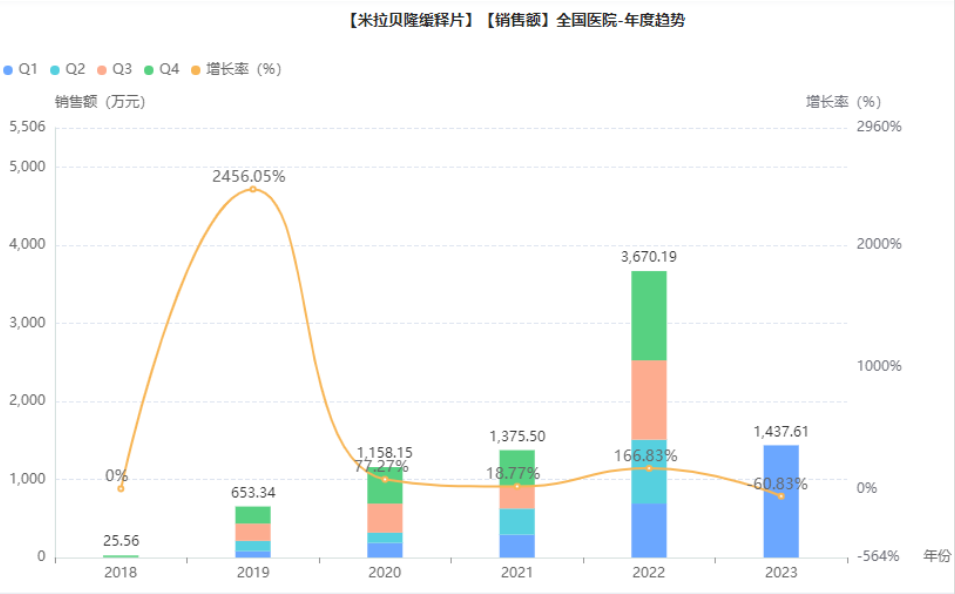
截图来源:药融云全国医院销售数据库
据要融云数据库统计,米拉贝隆缓释片目前在国内有5家药企拥有批文,包括一家进口Astellas,4家国产仿制(石药集团/四川国为制药/南京正大天晴/杭州华东医药),均已通过一致性评价,其中杭州华东医药为首家过评企业。
除了本次申报的南京美瑞制药,还有重庆医药、江西山香药业、广东东阳光药业、齐鲁制药等药企已递交米拉贝隆缓释片的上市申请,均在审评审批中。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论