
FDA于2021年批准阿杜那单抗的上市打破了近二十年阿尔茨海默病(AD)无新药的沉寂,尽管其争议不断。两年后,卫材仑卡奈单抗获批上市,这是一款近年来首次完全批准的药物,它是第一个从加速批准转换为传统批准用于治疗AD淀粉样蛋白β的定向抗体。(相关阅读:卫材:Leqembi在日本获批用于治疗阿尔茨海默病)
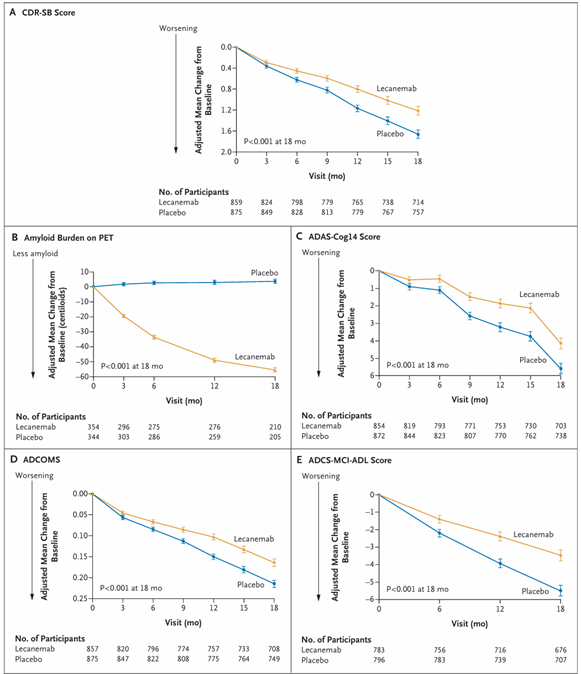
图1:仑卡奈单抗主要和关键次要终点数据(三期)
本年NMPA通过优先审评审批程序批准仑卡奈单抗注射液(商品名:乐意保/Leqembi)上市,一系列进展使得AD赛道重燃。
图2:来源药监局
全球约5,500万名AD患者,其中中国的AD患者人数已超过1,300万,预计患病率将呈现增加趋势。在 2020 年和 2021 年,当 COVID-19 进入十大死因行列时,AD超过已经COVID-19成为美国第七大死因。
近日,AD治疗管线综述更新(Alzheimer's disease drug development pipeline: 2024):
*截止2024年1月1日,有164项AD临床试验评估了127种潜在治疗药物,其中包括在3期测试了32种药物(共计48项试验);90项试验评估了81种处于2期的药物;以及26项一期试验,共计测试了25种潜在药物。
*目前正在进行的试验共需要 51,398 名参与者,包括 36,998 名处于临床第 3 阶段;第二阶段为13,138人;第一阶段1,262 名。
*潜在的阿尔茨海默病疗法从非临床研究进展到 FDA 审查的总开发时间约为 13 年。
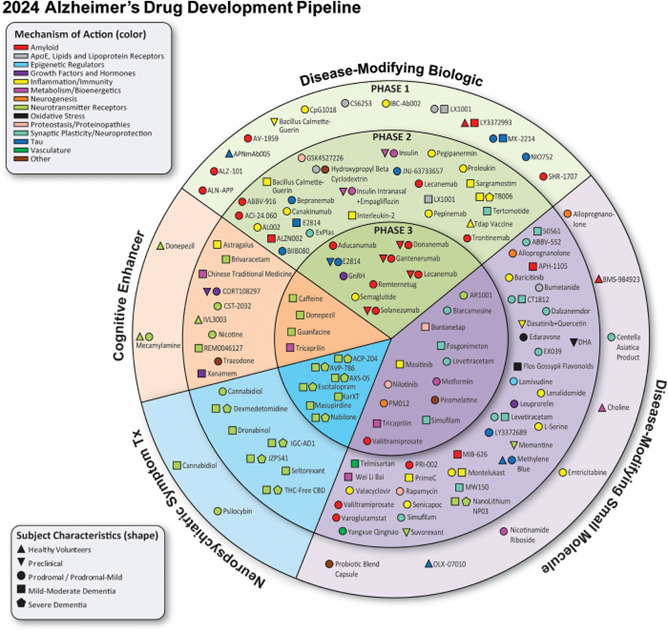
图3:治疗阿尔茨海默病的临床试验中的药物。绿色区域的药剂是生物制剂;紫色区域的药剂是改善疾病的小分子; 橙色区域的药剂是针对认知增强的症状药剂; 图中蓝色部分的药剂是针对行为和神经精神症状
下面细数一下药物以及靶点:
AD药物开发管线中的大多数药物(96 种)是疾病调节剂(disease-modifying therapies,DMT),占临床试验药物的 76%。12%的管线(15种)以认知增强为治疗目的,13% (16种)的药物被提议用于神经精神症状的治疗。在96种DMT中,53种(55%)是小分子药物,43种(45%)是生物制剂。临床第 3 阶段的占 66%(21 种药物);第 2 阶段的占 78%(63 种药物);第一阶段的占 84%(21 种药物)。
AD病理存在几种不同的的假说,开发管线中的药物针对广泛的靶点(最常见的靶向过程包括神经递质受体、炎症、淀粉样蛋白和突触可塑性)。28种药物(占在研药物的22%)靶向神经递质受体;25 种药物(20%)靶向神经炎症;23 种疗法(18%)靶向淀粉样蛋白 β 蛋白(Aβ);15 种药物(12%)涉及突触可塑性/神经保护;11 种药物(9%)靶向 tau 相关过程;8种药物(6%)涉及新陈代谢和生物能量学;5种(4%)药物靶向ApoE、脂质和脂蛋白受体;4 种药物(3%)分别涉及蛋白稳态/蛋白质病变以及生长因子和激素;3 种疗法(2%)针对氧化应激、神经发生和昼夜节律紊乱;2种药物(2%)靶向脉管系统因子;而肠脑轴和表观遗传调节因子的都有1种药物(1%)在研究中。
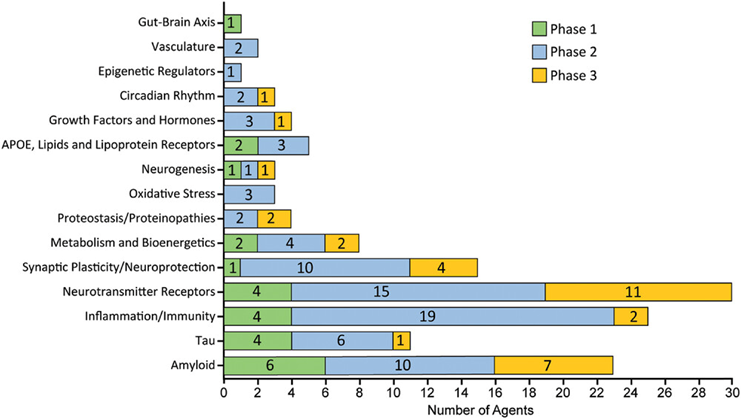
图4:阿尔茨海默病药物开发管道每个阶段的药物进行分类
在52项试验中(占当前试验的32%),有39种(占当前药物的31%)重新利用的药物正在开发中。在重新利用的药物中,15%(6种药物)是DMT生物制剂,54%(21种药物)是DMT小分子药物,15%(6种药物)靶向认知增强,15%(6种药物)正在评估用于治疗神经精神症状。
我们着重看下3期进展情况:
*药物研究方面:有48项3期试验评估了32种药物。3期药物(21种)中有66%是DMT,包括9种生物制剂(43%的DMT)和12种小分子(57%)。有4种(占 3 期药物的 12%)认知增强剂和7种(占 3 期药物的 22%)处于 3 期神经精神药物。
*靶点研究方面:第 3 阶段的药剂包括 11 种(34%)针对递质;7 种(22%)靶向淀粉样蛋白相关过程;4 项(12%)涉及突触可塑性/神经保护;2 项(6%)分别针对代谢和生物能量靶点、炎症和蛋白稳态/蛋白病;针对 tau、神经发生、生长因子和激素以及昼夜节律相关过程的药物各 1 项(3%)。在3期试验中,药物总共涉及10个生物过程类别。
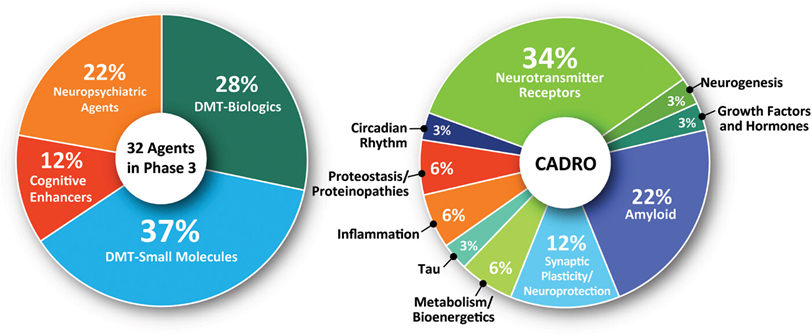
图5:3期阿尔茨海默病临床试验中药物的作用机制
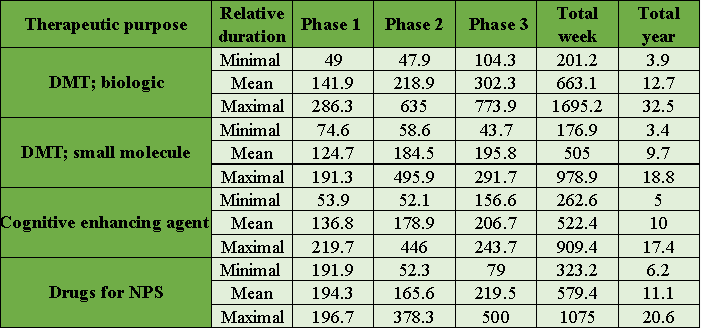
平均而言,生物制剂的DMT 3期试验(不包括预防试验)需要3.5年,小分子需要2.2年才能招募到所需数量的患者。认知增强剂的招募平均需要 3.4 年,神经精神症状的试验平均需要 3.7 年。治疗持续时间因治疗类别而异,生物制剂的 3 期预防试验的平均治疗期为 3.8 年。非预防性生物制剂的 3 期试验平均治疗期为 1.5 年;小分子的非预防性 3 期试验的平均周期为 1 年。平均而言,认知增强剂治疗暴露期和神经精神药物治疗期分别为4.5个月和4.8个月。
DMT生物制剂的三个药物开发阶段的平均持续时间为12.7年,DMT小分子药物为9.7年,认知增强剂为10年,神经精神症状药物为11.1年。
表1:试验的研究持续时间表(治疗加招募)
十年一剑,而药物研究的困难胜于铸剑。
与 2023 年的产品线相比,2024 年阿尔茨海默病药物开发管道收缩。2024年试验数量减少(164 vs.187 项)、药物减少(127 项vs. 141 项)、新化学实体减少(88 项vs.101 项)和类似数量的再利用药物(39 项vs. 40 项)。
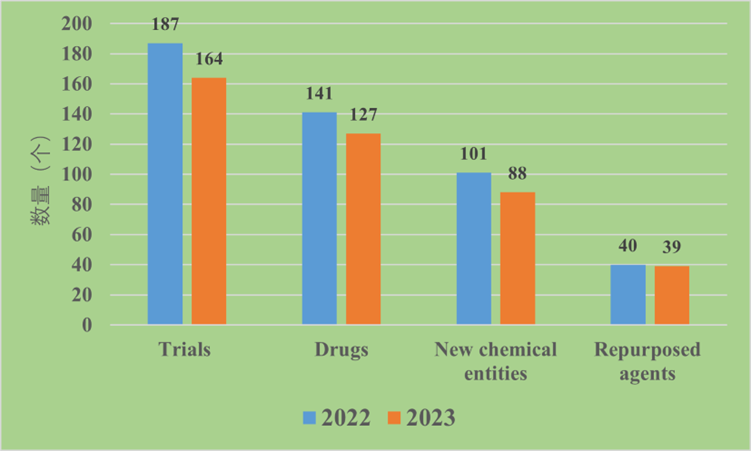
图6:近两年产品线
AD研究在不断试错中前行。
子弹击发之前需要明确的靶点,而研发需要有清晰指南来指引。FDA于时隔6年于本年3月再次对AD研发指南进行修订,增加对生物标志物以及替代终点的支持:“根据生物标志物来挑选早期 AD 患者来参加试验,选择早期 AD 临床试验的结果指标,并利用对 AD 特征性病理生理变化的影响支持这些人群的批准”。放宽条件无疑将进一步加速AD临床试验的进展。

图7:FDA发布的AD研发指南
NIH官网披露的在AD资助上的数据显示呈现增长趋势,成为填充 AD这一无底洞的催化剂。
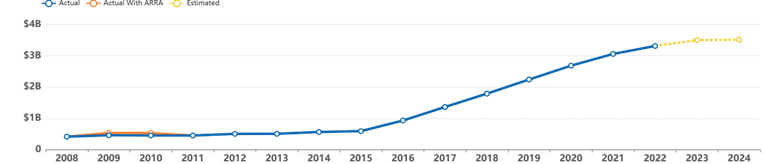
图8:2008至2022财年AD研究方面支持数据
目前,FDA批准上市的治疗 AD 药物非常有限,相关药物研发又一波三折。渤健于1月宣布停止静脉滴注用阿杜那单抗100mg/mL注射液的开发和上市,而FDA第二次延迟批准礼来AD新药Donanemab上市……
表2:目前FDA批准的AD药物汇总
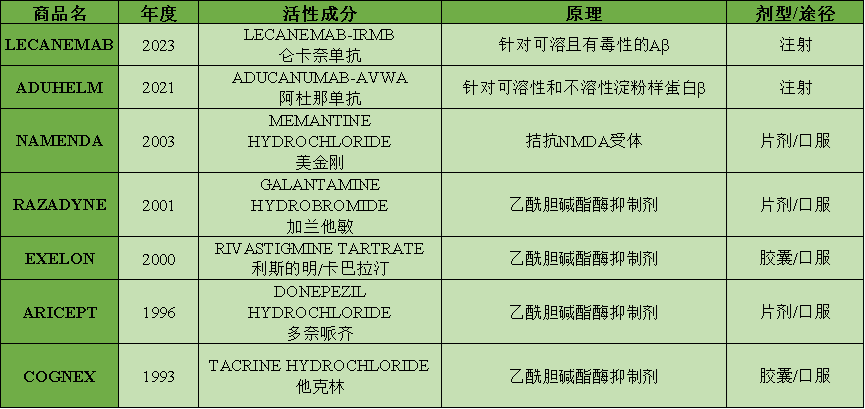
无数药企折戟,AD无疑是最具挑战的治疗领域,随着AD药物研发领域指南的更新以及投入,对未来我们自己可能要面对的敌人敢于亮剑,即使倒下,也要成为一座山,一道岭….
AD治疗的黄金窗口期是在AD早期阶段,尤其是在轻度认知障碍期间,早期诊断和治疗则显得尤为关键。
表3:国内AD诊断布局企业

我国人均预期寿命已经提高到了近80岁,老龄化可能会让AD出现呈现滚雪球的模式,AD病情的发展是不可逆的,这种被遗忘的死因可能还需要时间来治愈,找回丢失的记忆,让AD患者早日走出记忆的迷宫…前仆后继的医药人。
表4:国内AD治疗布局企业

附表1:临床3期药物
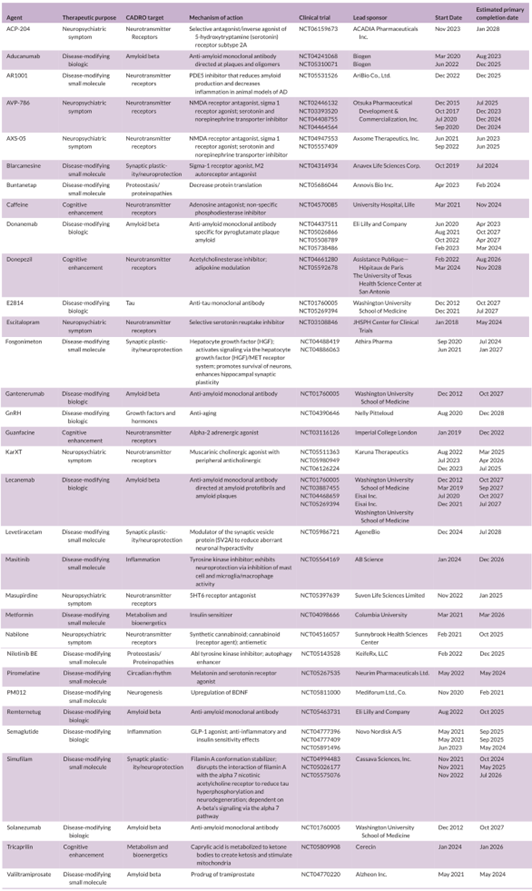
参考文献:
1.2023 Alzheimer's disease facts and figures. Alzheimers Dement. 2023
2.Alzheimer's disease drug development pipeline: 2024
3.Alzheimer's disease drug development pipeline: 2023
4.van Dyck CH,. Lecanemab in Early Alzheimer's Disease. N Engl J Med. 2023
5.https://www.fda.gov/regulatory-information/search-fda-guidance-documents/early-alzheimers-disease-developing-drugs-treatment
6.https://report.nih.gov/funding/categorical-spending#/
7.https://www.nmpa.gov.cn/zhuanti/cxylqx/cxypxx/20240109192251169.html
8.公司官网
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论