

康希诺生物股份公司(简称:康希诺生物)于2009年注册于天津滨海新区,是由跨国制药企业高管团队回国创立的国家级高新技术企业。康希诺生物以在世界范围内提供预防传染病和感染病的解决方案为己任,专业从事高质量人用疫苗的研发、生产和商业化,是国内领先的高科技生物制品企业。2019年3月,康希诺生物在香港联交所主板H股上市;2020年8月13日,康希诺生物正式登陆科创板,成为科创板开板以来首只“A+H”疫苗股。
康希诺生物公司基本信息
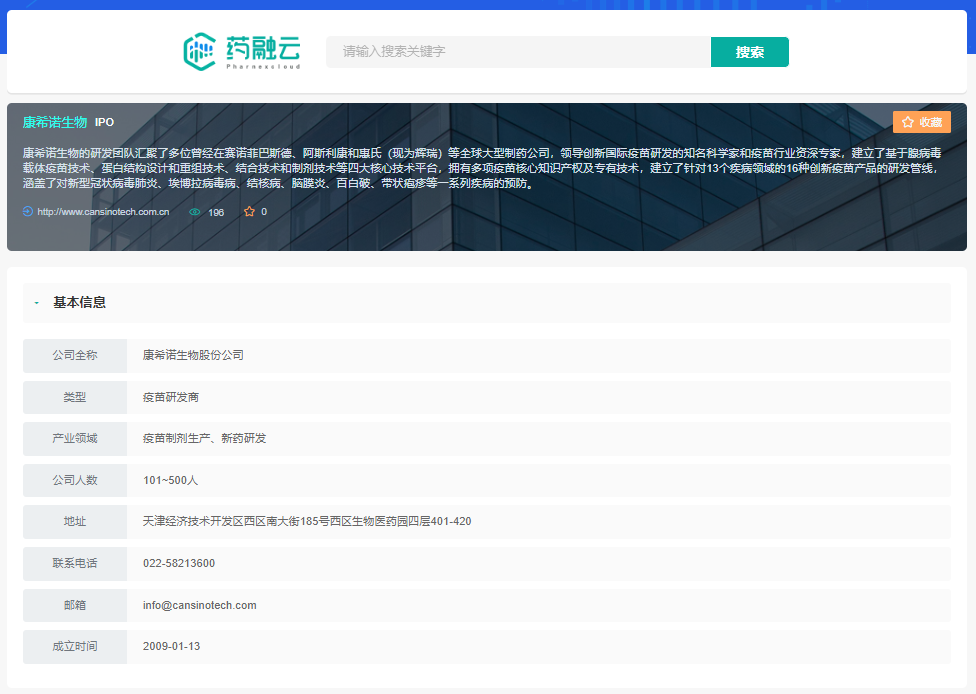
截图来源:药融云投融资数据库
01 发展历程
- 2009年,康希诺生物于中国天津注册成立及登记;
- 2011年,获得麦克马斯特大学有关结核病加强疫苗的全球授权;
- 2012年,完成设计符合GMP标准的中试车间的建设;
- 2013年,康希诺生物就MCV2及MCV4提交临床试验申请;
- 2014年,就在研DTcp提交临床试验申请;AD5-EBOV获得临床试验申请批准并开始临床试验;
- 2015年,中试车间通过EMA的QP认证;MCV2及MCV4获得临床试验申请批准;
- 2016年,Ad5-EBOV于塞拉利昂完成第二阶段临床试验;PBPV提交临床试验申请;
- 2017年,于中国取得Ad5-EBOV的新药申请批准;
- 2018年,康希诺生物完成商业生产中心的建设;DTcP及PBPV获得临床试验申请批准;完成MCV2及MCV4的Ⅲ期临床试验;PCV13i提交临床试验申请;
- 2019年,MCV2获得新药注册申请受理;香港主板上市;MCV4新药注册申请获得优先审评;
- 2020年,研发重组新型冠状病毒疫苗(腺病毒载体);A股发行获批成功挂牌上市;
- 2021年,重组新型冠状病毒疫苗(5型腺病毒载体)、MCV2及MCV4获批上市。
02 融资情况
经药融云数据库查询,康希诺生物最新一轮融资在2020年8月,完成了一项52亿人民币的IPO融资。至此,康希诺生物公司总融资已远超60亿元。
康希诺生物融资情况

截图来源:药融云投融资数据库
03 疫苗研发管线
疫苗是康希诺生物的主要研发领域,目前康希诺生物正为12个疾病领域研发17种疫苗产品,包括已于2017年获批的埃博拉病毒病疫苗,2021年获批附条件上市的国内首个腺病毒载体新冠疫苗以及自主研发的A群C群脑膜炎球菌多糖结合疫苗(CRM197载体)美奈喜®和国内首创的ACYW135群脑膜炎球菌多糖结合疫苗(CRM197载体)曼海欣®,还有7种处于临床试验阶段或临床试验申请阶段的候选疫苗,另外,康希诺生物还有6种在研疫苗处于临床前研究阶段,包括1种在研联合疫苗。
康希诺生物已上市疫苗
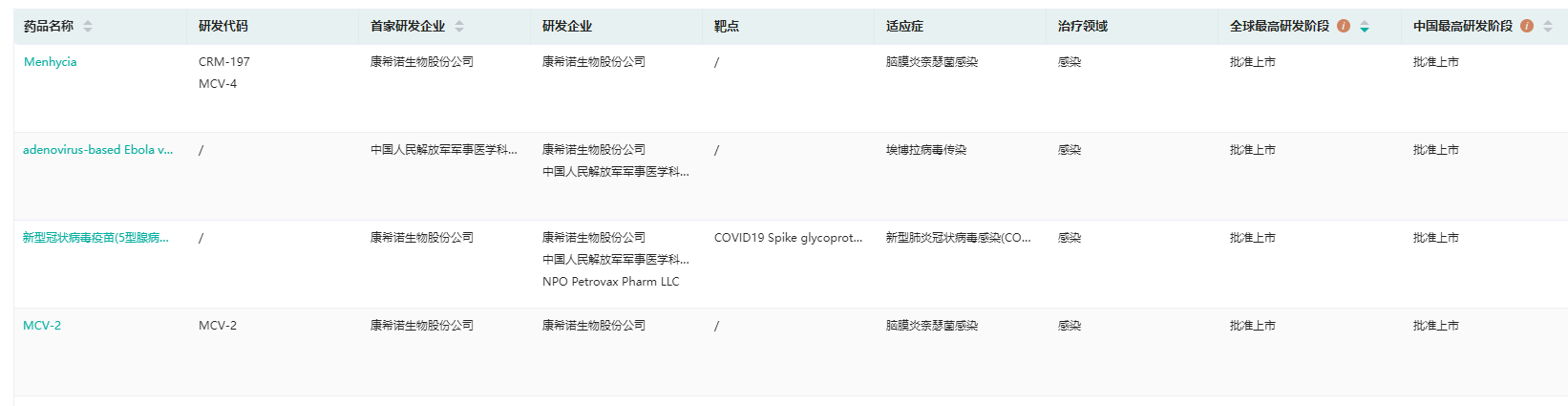
截图来源:药融云全球药物研发数据库
康希诺生物疫苗研发管线
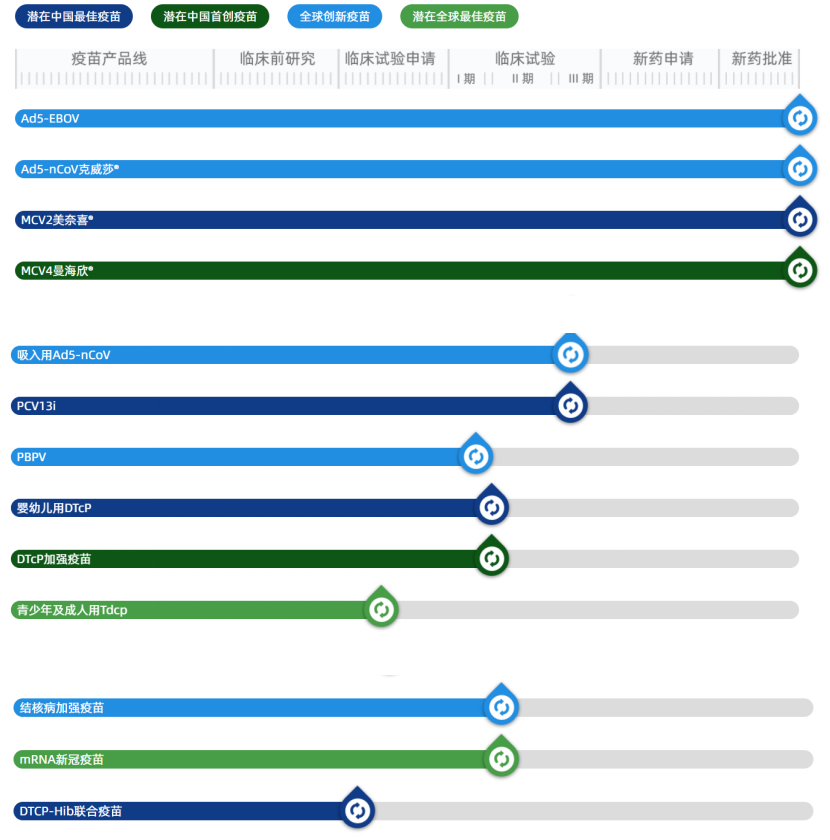
截图来源:康希诺生物官网
04 技术平台
康希诺生物拥有5大技术平台:基于病毒载体技术、合成疫苗技术、蛋白结构设计和重组技术、mRNA技术、制剂及给药技术。
(1)基于病毒载体技术
此技术使康希诺生物在短短三年内,将全球创新埃博拉病毒疫苗由一个概念转化为获批准的产品。该腺病毒载体技术亦适用于结核病加强疫苗和其他在研疫苗。
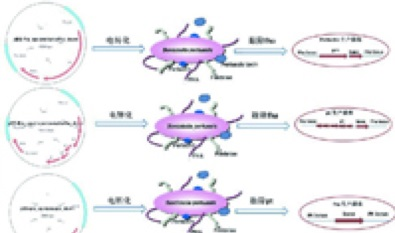
(2)合成疫苗技术
合成疫苗技术使康希诺生物能够生产各种结合疫苗。除了常用的DT和TT载体蛋白外,康希诺生物拥有若干载体蛋白,包括由康希诺生物专有的高产菌株生产并用于在研MCV的CRM197。各种载体蛋白使康希诺生物能够研发出更优质的多价结合和联合疫苗。
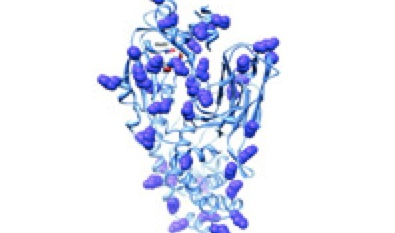
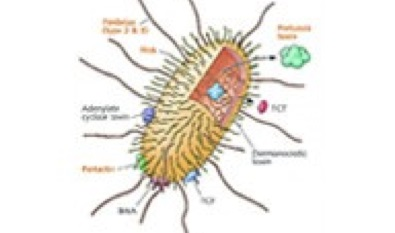
(3)蛋白结构设计和重组技术
康希诺生物已使用蛋白结构设计技术设计肺炎球菌蛋白抗原。此外,他们已研发新型重组菌株以生产新一代百日咳疫苗,亦研发出用于病毒载体生产的专利细胞系。
(4)mRNA技术
mRNA技术具有研发周期短、扩产容易、可作用于细胞内外靶点、表达多种蛋白、不进入细胞核、无需体外表达和纯化等特性。基于此技术研发的mRNA疫苗利用编码抗原的信使RNA,通过特定的递送系统使细胞摄取并表达编码抗原,从而引起体液和细胞介导免疫反应,mRNA疫苗的研发仅需在成熟技术平台上更换抗原序列,因此在针对突发传染病等方面有巨大优势。康希诺生物开发出的mRNA通用型工艺,有望大幅缩短产品开发时间,同时有利于快速产业化放大,应用该技术开发的预防性疫苗产品包括新型冠状病毒疫苗和其他多种病毒疫苗。
(5)制剂及给药技术
康希诺生物的培养基配方不含动物成分,最终产品制剂亦不含不必要的苯酚和防腐剂。此特点可确保产品质量稳定,减少潜在的副作用风险。
05 最新进展
- 7月16日,中国疫苗行业协会疫苗经济学专业委员会成立会议暨第一届第一次委员会会议在北京举行。会上,康希诺生物党委书记谢辉当选副主任委员。
- 7月5日,康希诺生物的ACYW135群脑膜炎球菌多糖结合疫苗(CRM197载体)曼海欣®(以下简称:四价流脑结合疫苗)首批产品今日成功发运。曼海欣®是国内首创、全球第三个可用于6月龄以下婴儿的流脑疫苗。
- 6月29日,四价流脑结合疫苗首批产品获得国家药品监督管理局签发的《生物制品批签发证明》,曼海欣®正式在国内上市销售。曼海欣®是国内首创的ACYW135群流脑结合疫苗,填补了该领域缺乏高端疫苗产品的空白。
- 5月25日,中国同马来西亚就联合开发人用疫苗开启全新合作并举行合作签约仪式。中国康希诺生物、马来西亚国立生物技术研究院(NIBM)和马来西亚制药公司Solution Biologics分别代表中马两国签署合作协议。协议内容主要涉及促进人类疫苗开发、研究、培训和商业化方面的长期合作。
参考资料:
[1] 康希诺生物官网
[2] 药融云数据库
推荐阅读:《荣瑞医药管线梳理!》
想要解锁更多药企信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息;投融资情况;最新动态;产品管线布局、药物基本信息、研进展、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论