
近日,康方生物宣布其自主研发的双特异性抗体新药AK152正式获得NMPA批准,开展用于治疗阿尔茨海默病(AD)的临床试验。
在过去的四十年里,AD药物研发的失败率高达惊人的99.6%,成为医药研发史上最昂贵的“坟场”。每当一款新药进入临床试验,科研界和患者群体都屏息以待,但大多数时候,等待他们的只是又一次失望。
然而,随着全球老龄化加剧,患者群体持续扩大,攻克阿尔茨海默病,已成为当今世界最迫切需要实现的梦想之一。在此背景下,康方生物的双抗新药能否撕开一道曙光?双抗技术真的会是AD治疗的终极答案吗?
一、半个世纪的探索与挣扎
阿尔茨海默病的治疗史,是一部充满挫折的药物研发史。
自1906年德国医生阿洛伊斯·阿尔茨海默首次描述这种疾病以来,人类对其发病机制的认知仍笼罩在迷雾中。目前,科学家针对阿尔茨海默病的主流的学说就有三种,分别是Aβ级联假说、Tau蛋白异常磷酸化假说、胆碱能假说。加上由于病程进展周期长、临床指标差异大、诊断难度大等问题,AD药物的研发始终止步不前。
根据美国药物生产与研发协会发布的研究报告,2000-2017年,全球累计在阿尔茨海默病药物上的研发投入超过6000亿美元,失败的临床药物超过300种,失败率高达99.6%,占所有药物研发失败率首位。
就连不少国际医药巨头也在AD领域屡屡受挫:2012年,强生与辉瑞合作开发的Bapineuzumab在III期临床阶段宣告失败;两年后,罗氏的Gantenerumab同样未能通过III期临床试验的考验;2016年,礼来备受期待的Solanezumab也未能达到主要临床终点;紧随其后,默沙东于2017年宣布停止BACE抑制剂Verubecestat的研发;2018年,强生再次折戟,不得不终止其BACE抑制剂Atabecestat的II/III期临床试验。
事实上,在2021年之前,美国FDA仅批准过6种阿尔茨海默病治疗药物,包括:他克林(Tacrine)、多奈哌齐(Donepezil)、卡巴拉汀(Revastigmine)、加兰他敏(Galantamine)、美金刚(Menantine)以及美金刚/多奈哌齐复方制剂。
其中,前四种都是基于胆碱能假说而开发的乙酰胆碱酶(AChE)抑制剂,美金刚为N-甲基-D-天冬氨酸(NMDA)受体拮抗剂。但这些药物都只能改善患者的症状,不能减轻阿尔茨海默病的病理变化,也不能逆转或减缓疾病进程,且都有不同程度的副作用。“无药可治”的困境让阿尔茨海默病成为继心血管疾病、脑血管疾病和癌症之后,老年人致残、致死的第四大疾病。
直到近几年,基于Aβ级联假说,AD新药研发领域不断传来令人振奋的消息。2023年1月,FDA宣布完全批准由卫材和渤健联合开发的AD新药仑卡奈单抗(Leqembi),用于治疗早期AD患者,成为全球首个能延缓AD进程的药物;2024年7月,礼来的新一代抗淀粉样蛋白β(Aβ)多奈单抗(Donanemab)获FDA批准上市,用于治疗AD所致的轻度认知障碍以及轻度AD。
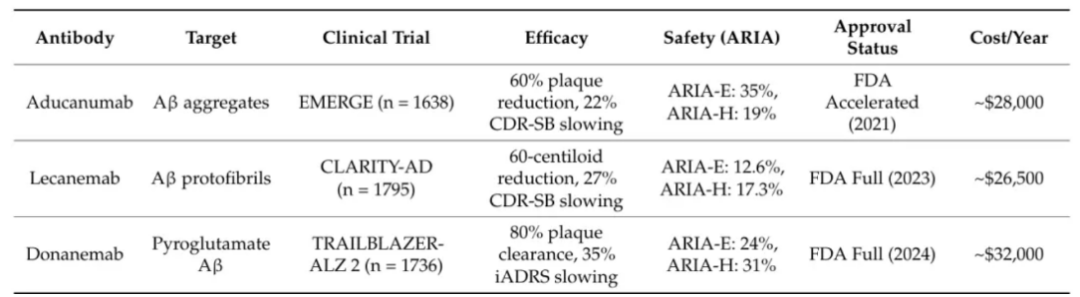
图1 阿尔茨海默病治疗用已上市抗Aβ单克隆抗体
图片来源:参考资料1
然而,即便是仑卡奈单抗和多奈单抗,它们在临床中仅能带来有限的认知功能延缓改善,同时还伴随着不容忽视的脑水肿和脑出血风险,高昂的治疗费用更是让无数患者家庭望而却步。
二、双抗会是答案吗?
越来越多的研究表明,阿尔茨海默病是一种由多重因素导致的复杂疾病,这也是导致单一靶点药物屡屡受挫的主要原因。
那么既然“Aβ级联假说”或“Tau蛋白假说”任何单一理论都不足以完全解释和攻克AD,那么,能否设计出一种药物,可以同时作用于多个关键病理环节,实现“协同作战”?
双抗药物恰好能够满足要求。双抗药物能够同时特异性结合两个不同靶点或表位,通过协同作用破解复杂疾病的治疗难题,成为破解AD治疗的新路径。
相较于单抗仅能干预单一病理环节,双抗药物通常可以通过两种方式发挥作用:一种是同时靶向两个靶点,同时阻断AD进程中的两个关键环节,比如同时清除Aβ沉积与抑制Tau蛋白聚集,形成“1+1>2”的协同治疗效果,突破单一靶点药物的疗效局限;另一种则是增强递送能力,通过一个靶点结合血脑屏障高表达的特异性受体,借助受体介导的转运机制实现抗体高效入脑,同时通过另一个靶点精准结合致病蛋白(如Aβ),从根本上解决传统抗体“进不了脑、浓度不够”的递送难题,为中枢神经系统疾病的抗体治疗开辟新路径。
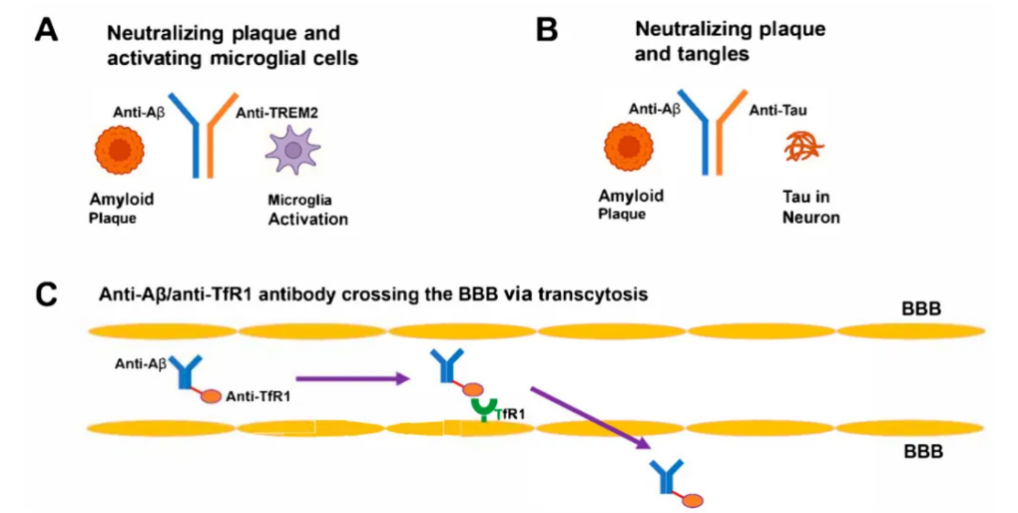
图2 双抗的核心作用方式
图片来源:参考资料1
康方生物的AK152正是基于后一种模式的针对性设计,在靶点选择上,AK152创新性地同时靶向Aβ和BBB高表达受体。目前已获批的仑卡奈单抗与多奈单抗均聚焦于Aβ通路,大量临床数据已经证实了通过清除脑内Aβ斑块可延缓认知功能下降,而AK152的Aβ端不仅能结合Aβ斑块,还能够高选择性结合更具神经毒性的可溶性Aβ多聚体,这类物质被认为是引发神经元损伤、突触功能障碍的关键元凶,毒性远高于成熟的Aβ斑块,AK152的精准靶向有望从源头阻断神经毒性传导。
与此同时,与现有Aβ单靶点抗体因入脑效率不足而限制疗效、并伴随安全性风险的困境相比,AK152利用BBB高表达受体介导的胞吞-胞吐转运机制,显著提高AK152的入脑率。临床前研究已初步验证这一设计的优势:AK152具有显著的生物活性和良好的安全性特征,相比单抗可有效提高抗体入脑率,更快清除Aβ斑块,展现出显著优于单抗的治疗药效,有望为阿尔茨海默病患者带来新的希望。
从行业格局来看,AD双抗研发仍处于早期探索阶段,全球范围内尚未有产品获批,AK152仍需面对“第一个吃螃蟹”的未知风险。但康方生物在双抗领域已积累成熟经验,其PD-1/VEGF、PD-1/CTLA-4双抗在肿瘤领域的成功上市,验证了其双抗平台的技术稳定性,为AK152的临床推进提供了有力支撑。
三、千亿美金市场的潜力与挑战
尽管阿尔茨海默病研发之路遍布荆棘,失败案例屡见不鲜,全球药企仍前赴后继,不断探索。其重要驱动力,正是这一疾病背后蕴藏的巨大未满足临床需求,以及与之相应的千亿级全球市场潜力。
数据显示,全球AD患者已超过5000万人,而中国患者约1700万,占全球总数近30%,且正以每年约10%的速度增长。随着全球人口结构持续老龄化,预计到2050年,全球AD患者将突破1.5亿,中国患者将超过4000万。
这一庞大的患者基数催生出一个巨大的治疗市场。据行业分析,2023年全球AD治疗市场规模已突破600亿美元,其中药物治疗约占40%,预计到2030年将增长至1200亿美元,年复合增长率超过10%。中国市场虽起步较晚,但增长迅猛,预计到2028年规模将突破300亿元,年复合增长率达15%以上。
在此背景下,任何一个被证实能够有效延缓疾病进展的疗法,都意味着一个千亿美元级别的市场机遇。近年来获批的Aβ单抗以其高昂的定价,已经初步揭示了这一市场的支付潜力与商业天花板。双抗作为下一代治疗技术的代表,若能在此领域取得临床突破,其市场价值将不止于药品本身,更可能重新定义AD治疗标准与市场格局。
然而,这片广阔的蓝海也意味着前所未有的竞争与挑战。康方生物的AK152并非孤例,全球范围内,一批采用类似思路的双抗或多抗分子正处于不同的研发阶段。国际医药巨头如罗氏、强生、礼来等凭借其在神经科学领域的深厚积累和强大的资金优势,已在AD双抗领域建立领先地位。如罗氏的 Trontinemab(2+1型双特异抗体)已进入III期临床,有望成为全球首个获批的AD双抗药物。
除了同靶点技术的竞争,AD治疗领域的技术路线本身也呈现出多元化的趋势。截至2025年1月1日,AD治疗领域,有138种潜在药物正在进行共182项临床试验。其中,处于III期临床阶段的试验共48项,涵盖31款药物;处于II期临床阶段的试验共86项,涵盖75款药物;处于I期临床阶段的试验共48项,涵盖45款药物。
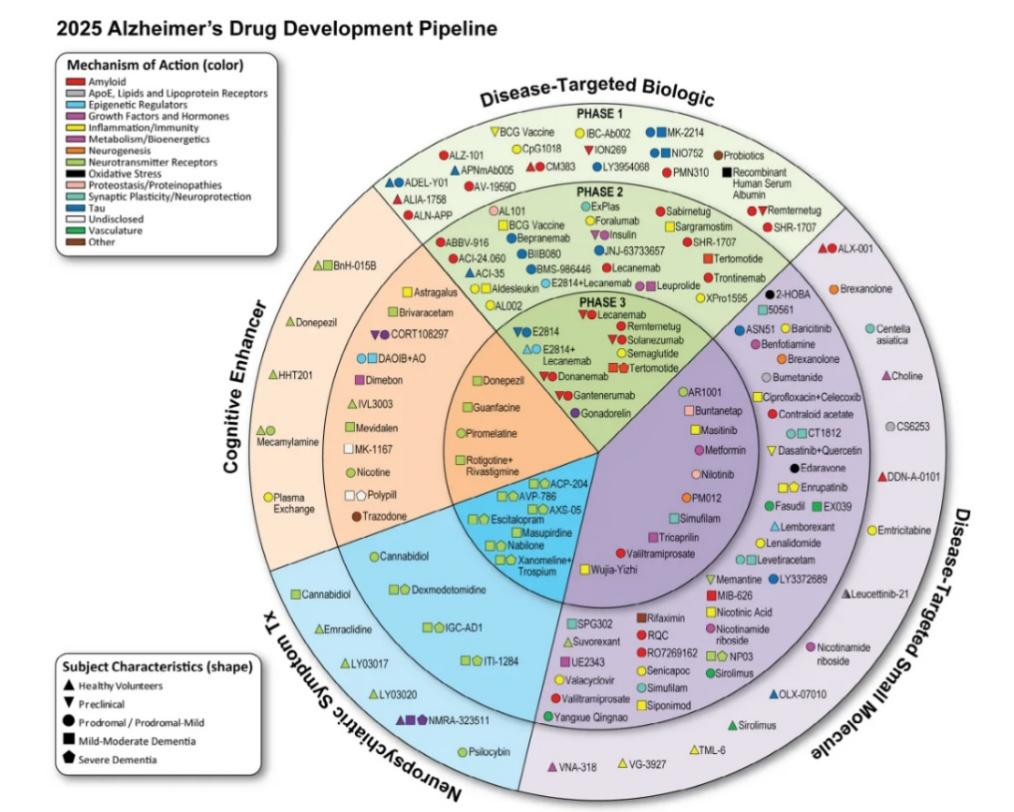
图3 2025年阿尔茨海默病临床管线
图片来源:参考资料2
除了靶向Aβ和Tau的抗体类药物,针对神经炎症、代谢异常、突触功能障碍等新兴靶点的探索也在持续进行;基因治疗、细胞治疗等前沿模式虽处于更早期阶段,但长期来看同样可能为AD治疗带来革命性变化。
四、结语
双抗药物从机制和临床上为阿尔茨海默病治疗带来了令人振奋的曙光,但它能否成为“终极答案”,仍需时间的检验。它或许不是终点,但它无疑是人类与阿尔茨海默病对抗史上的一个重要里程碑,为人类最终战胜阿尔茨海默病指明了新的方向。
参考资料:
1.《突破血脑屏障!阿尔茨海默病双特异性抗体疗法的逆袭之路》,抗体圈,2025-10-20
2.《Alzheimer's disease drug development pipeline:2025》,Alzheimers&Dementia,2025-06-03
文章来源:小药说药
原文链接:https://mp.weixin.qq.com/s/ofytCAOTVlQ78sXTLpbfsQ
扩展阅读:
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论