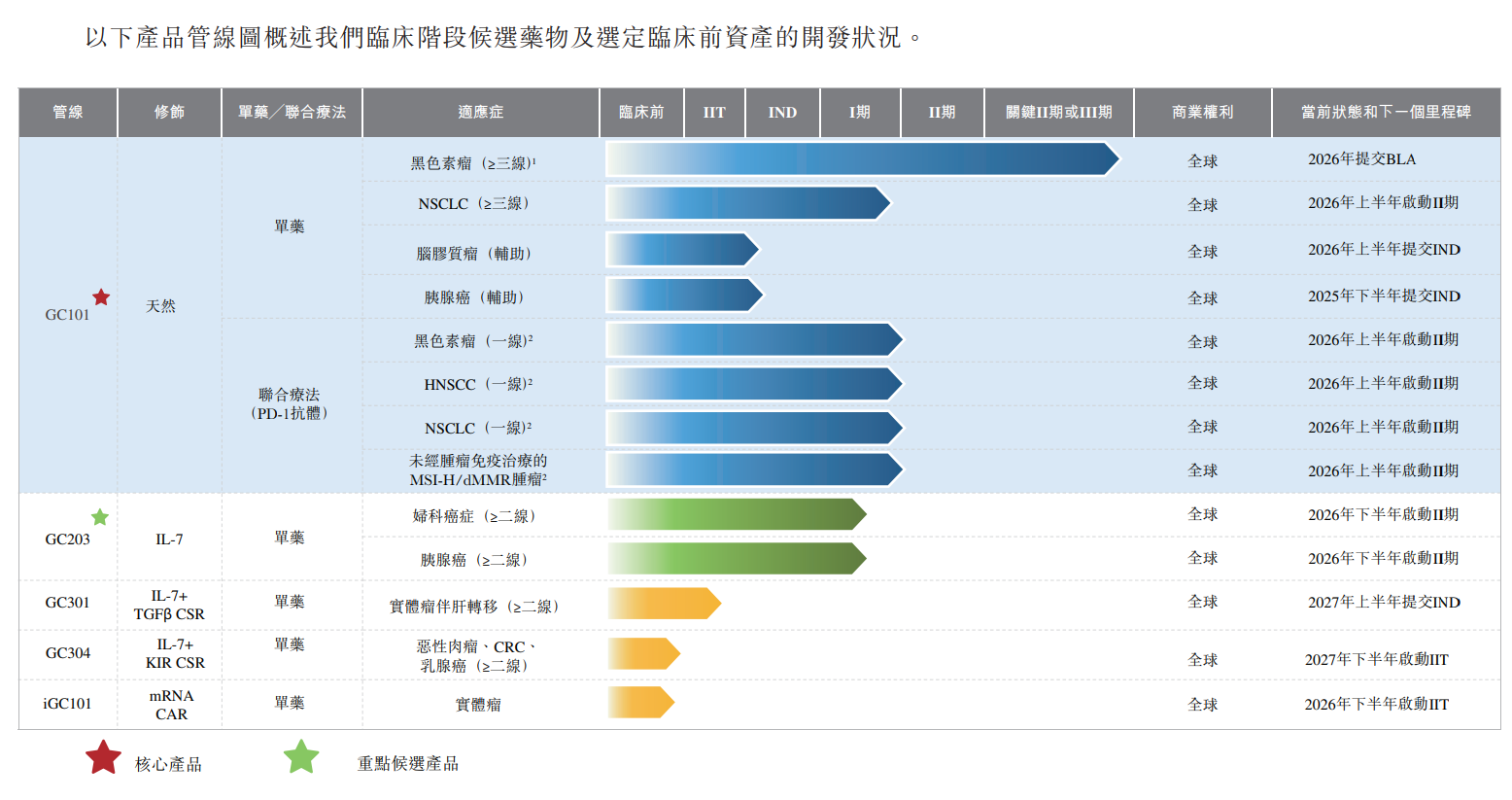
根据弗若斯特沙利文的资料,公司的核心产品GC101是全球首款无需高强度清淋化疗、无需IL-2给药的肿瘤浸润淋巴细胞(TIL)疗法,有望成为中国首个获批上市的TIL疗法。目前,GC101用于治疗黑色素瘤的临床试验正在开展关键II期临床试验,预计将于2026年提交生物制品许可申请(BLA)。
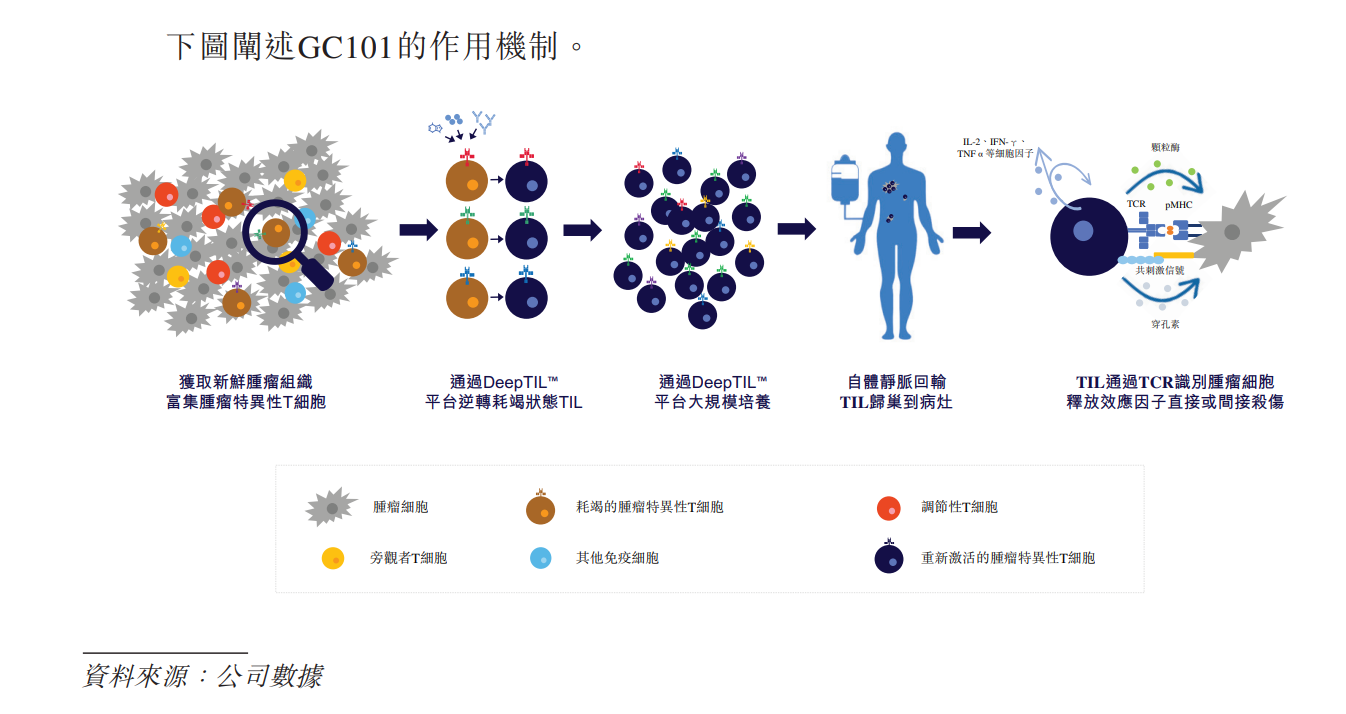
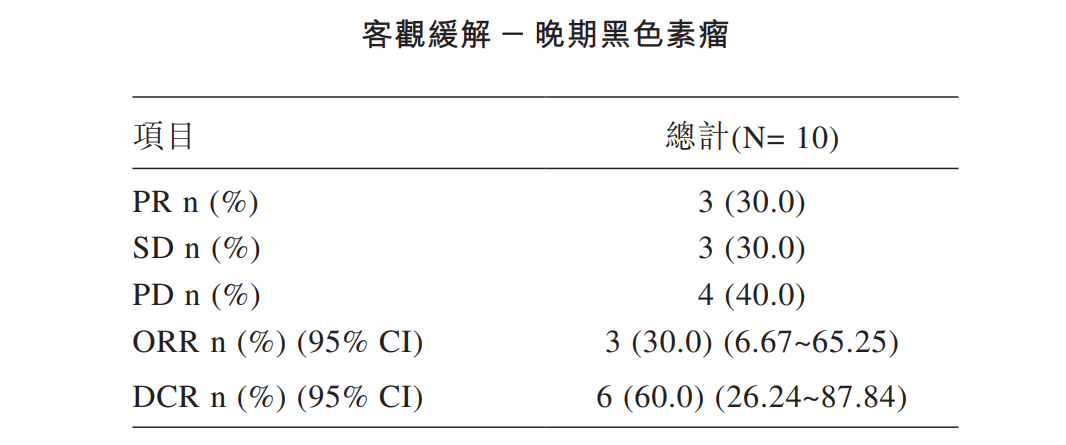
GC101针对多种类型标准治疗失败的晚期转移性实体瘤开展I期临床试验,已在黑色素瘤、非小细胞肺癌、宫颈癌等多种实体肿瘤展现客观缓解疗效。其中,针对标准治疗失败的10例转移性晚期黑色素瘤患者(中位前序治疗线数为3.5,100%经PD-1抗体治疗失败)客观缓解率为30%,中位无进展生存期为5.5个月。
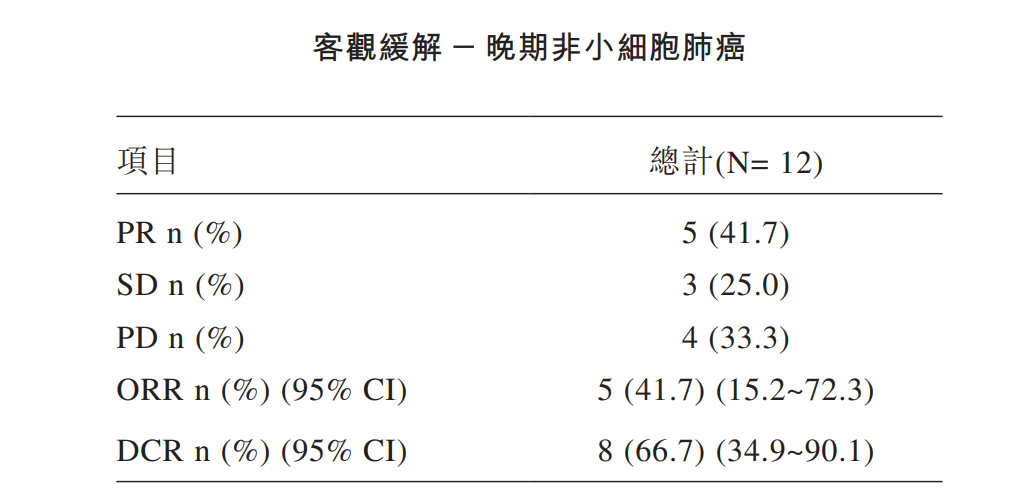
针对标准治疗失败的12例转移性晚期非小细胞肺癌患者(中位前序治疗线数为3),中位随访13.0个月时,GC101展示出41.7%的客观缓解率,中位缓解持续时间未达到;12个月总生存率为66.7%,中位生存期尚未达到。
根据弗若斯特沙利文的资料,公司重点品种 GC203 是全球首款非病毒载体基因修饰TIL细胞新药。在GC101基础上,GC203过表达独创的膜结合、自聚集型IL-7,强化TIL细胞的体内适应能力,并赋予其调动内源免疫细胞的活性。在IIT中,GC203治疗高度经治的卵巢癌患者,客观缓解率为33.3%,完全缓解率达11.1%,一年整体生存率达68.8%。
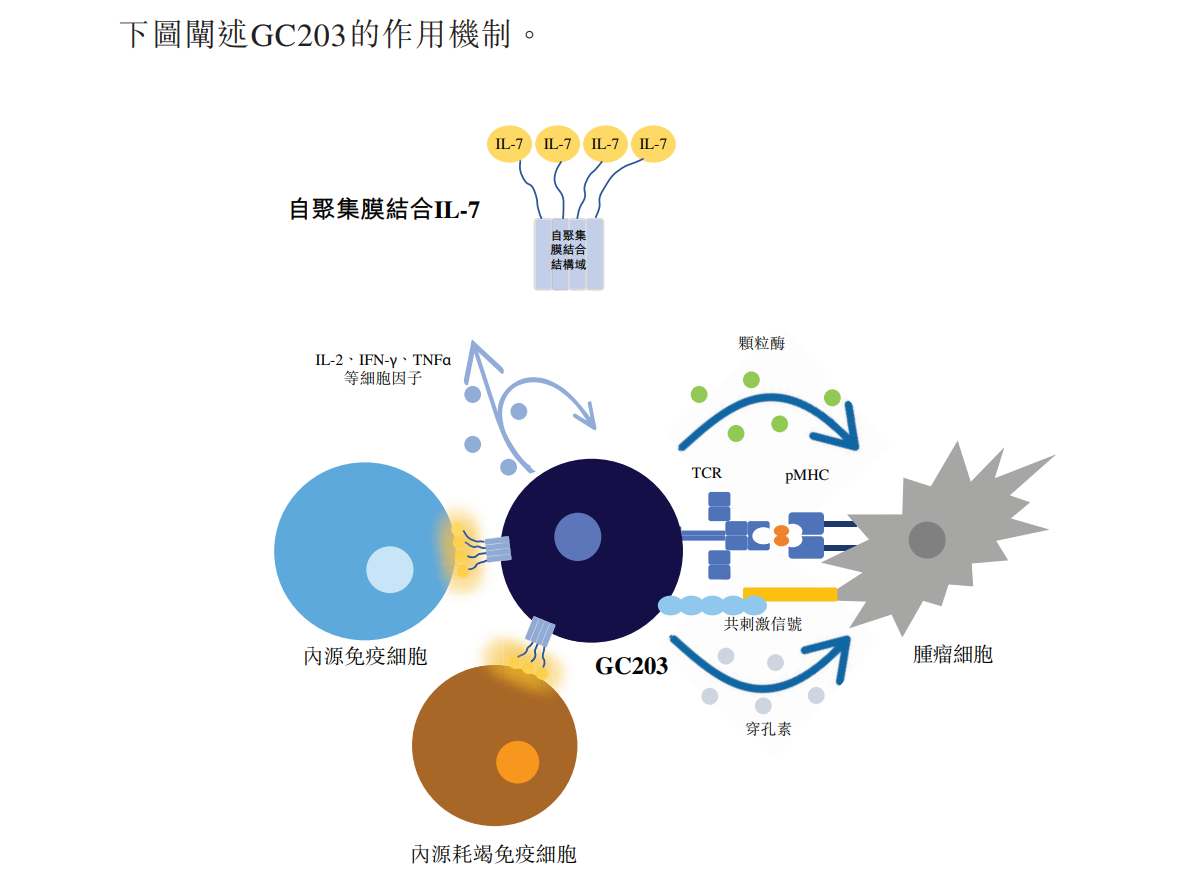

此外,基于分时段工艺,公司正在开发全球首创的内生TIL平台——RiverTIL™(快速内生扩增及反应TIL)平台,赋予预制的TIL种子细胞在患者体内直接扩增的能力。该方法大幅降低生产成本,缩短患者等待时间,显著提高TIL产品的可及性和覆盖面,有望使TIL疗法转变为一种普适性的个性化疗法。
公司扎根嘉定,近年来持续发展,在嘉定南翔建成3000㎡高标准硬件平台,在嘉定安亭建成超16000㎡目前全球设计产能最大、建设标准最高、设施最智能化的TIL细胞产业化基地。
截至递表,君赛生物已完成多轮融资,2025年11月公司完成1.37亿元C轮融资,投后估值21.37亿元。









公司最新股权架构如下:
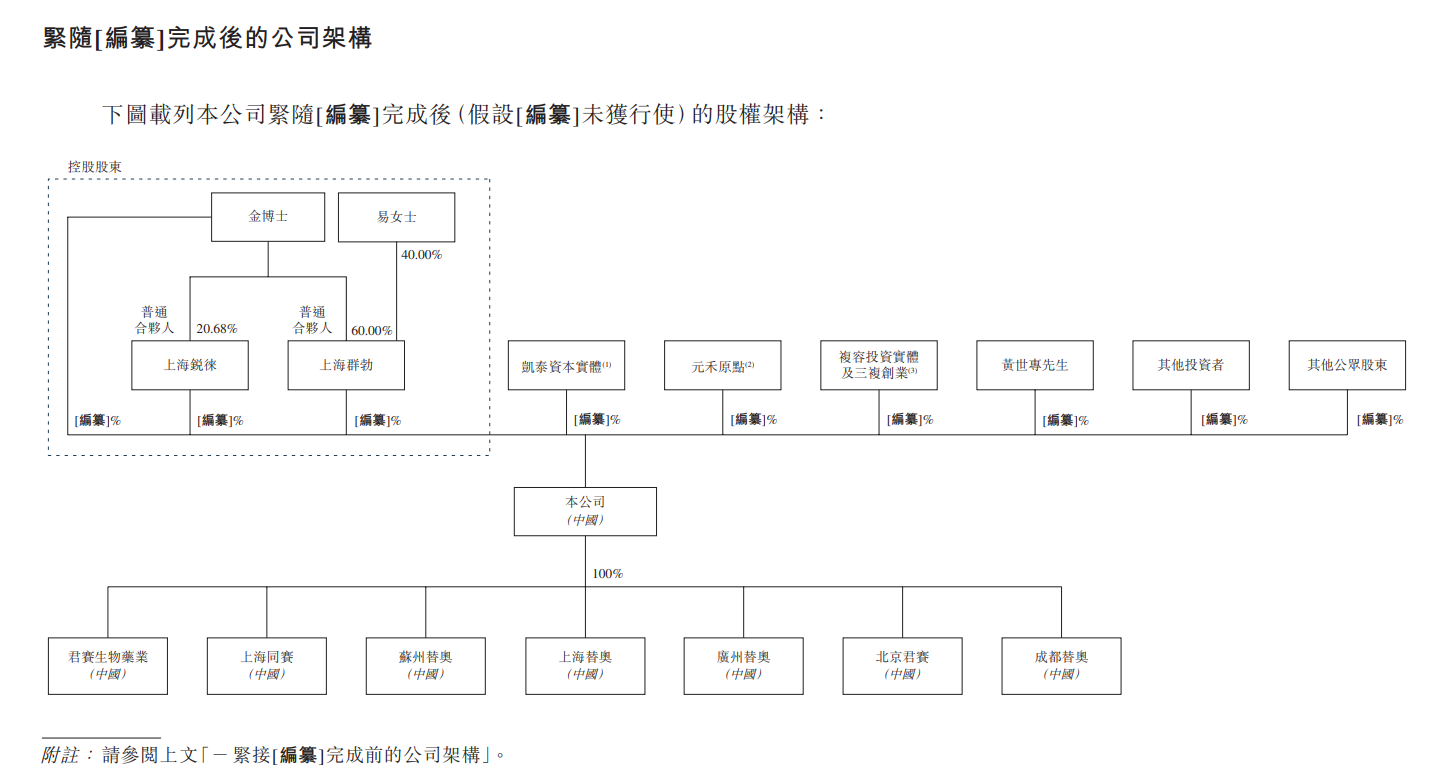
参考来源:
[1] 君赛生物招股书
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. Boundless的肿瘤创新疗法申请IPO!
2. Contineum Therapeutics申请IPO,推进多发性硬化症管线
3. Artiva冲刺IPO,融资8亿元助力NK细胞疗法突破
想要解锁更多药企信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!










































































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论