2022年1月26日,无锡智康弘义生物科技有限公司宣布其创新药首款双特异性抗体药物CD3/EGFR 项目(研发代号:BC3448)在上海肺科医院进行的I期临床试验完成中国首例受试者给药。该研究于2022年1月中旬在上海肺科医院举行临床启动会,由同济大学附属上海市肺科医院肿瘤科主任,同济大学医学院肿瘤研究所所长周彩存教授担任本项研究 PI。
该研究是一项I期、开放、首次人体剂量递增和剂量扩展的临床研究,在局部晚期或转移性恶性实体瘤患者中评估BC3448的安全性、耐受性、药代动力学特征和初步有效性,主要研究目的为评估BC3448单药在晚期恶性实体瘤患者的安全性和耐受性。
BC3448为介导T细胞杀伤作用的靶向CD3/EGFR双特异性抗体,利用EGFR作为肿瘤特异性抗原,通过结合EGFR和T细胞表面分子CD3,激活T细胞并募集至肿瘤细胞周围,发挥抗肿瘤作用。在临床前体外、体内研究中,BC3448在EGFR高表达、EGFR突变和KRAS或BRAF突变的细胞或动物模型中均展示出良好的药效活性。
BC3448基本信息
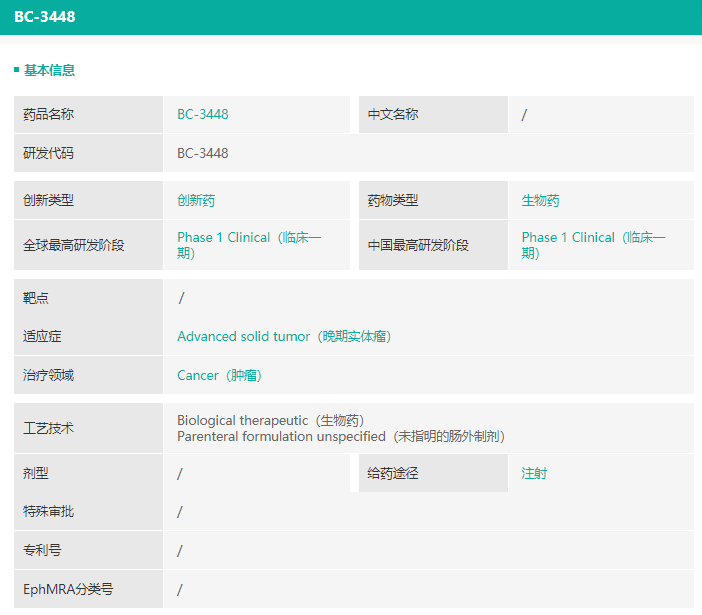
截图来源:药融云全球药物研发数据库
周彩存教授指出:“尽管如靶向EGFR胞外区的单抗药物、小分子酪氨酸激酶抑制剂等EGFR靶向药物不断取得突破性的进展,但依然面临很多新的挑战:例如临床中已出现的耐药患者,只有少量的肿瘤患者能从这些药物中获得持续的疗效。
因此,探索新的思路,开发改善EGFR耐药的免疫药物具有重要的临床意义。BC3448采用免疫治疗的思路,结合双特异性抗体的创新技术,通过CD3/EGFR激活T细胞杀伤有EGFR表达的肿瘤细胞,临床研究结果非常值得期待。”
智康弘义Co-CEO黑永疆博士表示:“智康弘义创建以来,以疾病生物学、转化医学为基础,通过扎实的内部创新与外部合作创新相结合的研发模式,以临床价值为导向,致力于全球范围内BIC、FIC药物的高效研发。
BC3448 是公司管线差异化策略下的一款双抗产品,其分子设计特意降低了 CD3 的亲和力以达到减少细胞因子风暴(CRS)的风险,同时保存了对 EGFR 较 强的亲和力,通过这种亲和力高低的特定设计,目的在保证药效的同时降低因作用于 CD3 分子而引起的 CRS 副作用。
目前全球范围内仅有少数几家公司的 CD3/EGFR 双抗进入临床I期,智康弘义凭借出色的临床业务的综合优势,有信心推动该款产品在全球率先获批上市,从而更好满足全球患者治疗需求、服务巨变中的临床新场景。”
关于BC3448
BC3448是智康弘义自主研发的靶向CD3/EGFR双特异性抗体,BC3448已获得中国国家药品监管管理局(NMPA)的IND批准,正在中国国内积极开展临床研究。
关于智康弘义
“做好药,为生命更美好/Better Medicine for Better life”,是智康弘义的崇高使命。
智康弘义成立于2017年12月,公司以患者和疾病为中心,关注疾病全周期,以未来重大未满足的临床需求为导向,现阶段积极推动领先的转化医学和临床研究业务平台化发展,优先专注于肿瘤、自身免疫等疾病“First-in-Class/Best-in-Class”创新药物的研发、临床试验和商业化。
自公司成立以来,在小分子实体、单抗、双抗、ADC等不同技术领域均进行了布局,凭借高效的研发和运营模式,目前已有6款新药进入临床Ⅰ期且均由国内域内顶级专家担任PI,在临床试验质量和进度上延续了产品临床前研究的优势,部分产品在全球范围内已取得临床进度上的领先。
智康弘义已组建了一支由科学、临床医学、转化医学等领域科学家组成的,且具有国际水平的核心科研管理团队领导各环节研发业务,同时配备了深耕本土、熟悉中国环境的运营团队,系统性地保证了公司全流程研发质量和效率。公司将进一步增强新技术领域及全球商业化的力量配置,以巩固公司领先的综合研发实力,积极布局和拓展海外市场。
智康弘义正以“快速成长为中国领先,拥有持续创新能力、核心组合产品、多样化创新疗法,及深度商业化能力的生物医药公司”为目标,致力于更好、更多地造福全球患者,为中国生物医药产业的新一轮发展贡献力量。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论