
7月29日,NMPA发布新一批药品批准证明文件待领取信息,其中,罗氏制药(Roche)的泛肿瘤抗癌药罗圣全®(英文商品名:ROZLYTREK,中英通用名:恩曲替尼/Entrectinib)获批上市。适用于经充分验证的检测方法诊断为携带神经营养酪氨酸受体激酶(Neurotrophic tyrosine receptor kinase,NTRK)融合基因且不包括已知获得性耐药突变,患有局部晚期、转移性疾病或手术切除可能导致严重并发症,以及无满意替代治疗或既往治疗失败的成人和12岁及以上儿童实体瘤患者。


截图来源:NMPA官网
恩曲替尼是罗氏制药开发的一款靶向泛TRK及ROS1酪氨酸激酶的具有中枢神经系统(Central Nervous System,CNS)活性的强效选择性的抑制剂,能够穿过血脑屏障。自2019年,恩曲替尼陆续在日本、美国、欧盟等地获批上市,用于治疗NTRK融合基因阳性实体瘤患者,以及ROS1阳性晚期非小细胞肺癌患者,是FDA批准的继Keytruda和Vitrakvi之后第三款“不限癌种”的抗癌疗法。
2021年10月,中国国家药品监督管理局药品审评中心(CDE)受理了罗氏制药递交的恩曲替尼胶囊的上市申请,并将其纳入优先审评,用于治疗NTRK融合阳性局部晚期或转移性实体瘤。
恩曲替尼胶囊审评概况

截图来源:药融云中国药品审评数据库
恩曲替尼首次引进中国,为长期等待的患者带来了新的治疗选择。据药融云数据库显示,罗氏制药的恩曲替尼还有2个申请上市的受理号尚在审评审批中。此外,罗氏制药还递交了帕妥珠单抗曲妥珠单抗注射液(皮下注射)、注射用维博妥珠单抗和曲妥珠单抗注射液(皮下注射)3款治疗用生物制品的上市申请。
罗氏制药待上市品种
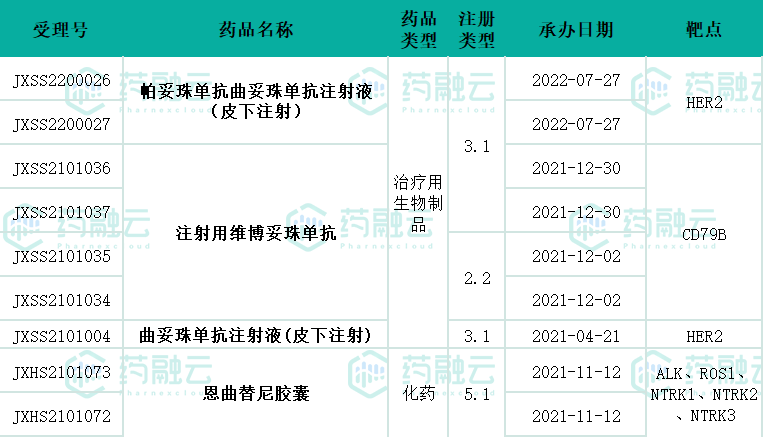
数据来源:药融云中国药品审评数据库
帕妥珠单抗曲妥珠单抗注射液(皮下注射)
2022年7月27日,药审中心承办了罗氏制药递交的帕妥珠单抗曲妥珠单抗注射液(皮下注射)的上市申请。据公开资料,这是一款由帕妥珠单抗、曲妥珠单抗和透明质酸酶构成的一种固定剂量组合,为HER2 单抗复方(商品名为Phesgo)。
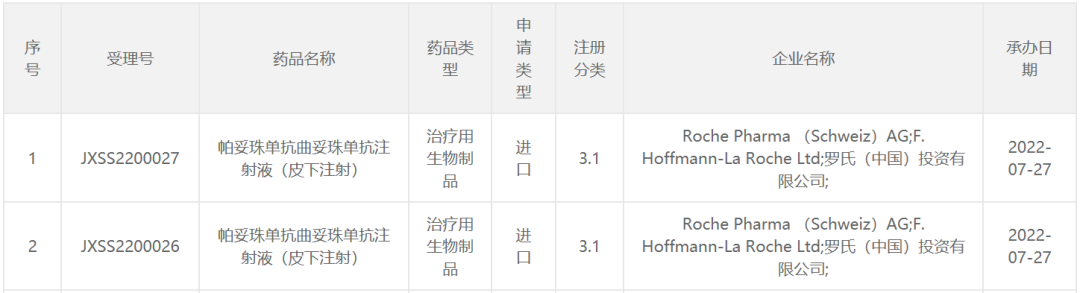
截图来源:NMPA官网
此前Phesgo已在美国、欧盟等国家和地区获批,用于治疗早期和转移性HER2阳性乳腺癌患者。该产品完成初始负荷剂量的给药时间约为8分钟,后续维持剂量的给药时间约为5分钟。相比之下,按照帕妥珠单抗和曲妥珠单抗各自的标准静脉注射方式,完成负荷剂量的给药时间约为150分钟,后续维持剂量的给药时间约为60~150分钟,相当于给药时间可以从数小时缩短至几分钟。
注射用维博妥珠单抗
维博妥珠单抗(Polivy,polatuzumabvedotin)是罗氏制药旗下基因泰克利用西雅图遗传学公司的ADC技术开发的一款B细胞抗原受体复合物相关蛋白β链(CD79b)靶向抗体偶联药物(ADC),由人源化抗CD79b抗体与小分子微管抑制剂MMAE(单甲基阿司他丁 E)偶联而成。
2019 年6 月,该药被FDA批准联合苯达莫司汀和利妥昔单抗用于复发或难治性弥漫性大B细胞淋巴瘤,成为全球首款用于弥漫性大B细胞淋巴瘤的ADC疗法。
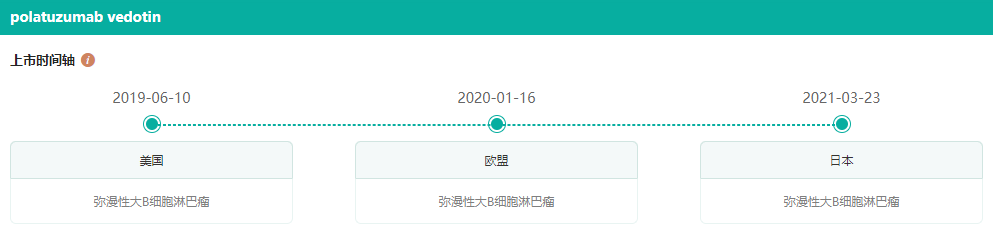
截图来源:药融云全球药物研发数据库
2021年12月,NMPA承办了维博妥珠单抗的上市申请,有望今年第4季度获批上市。此外,据药融云统计,罗氏制药维博妥珠单抗2021年全球销售额为3.4亿美元,同比增长了95%。
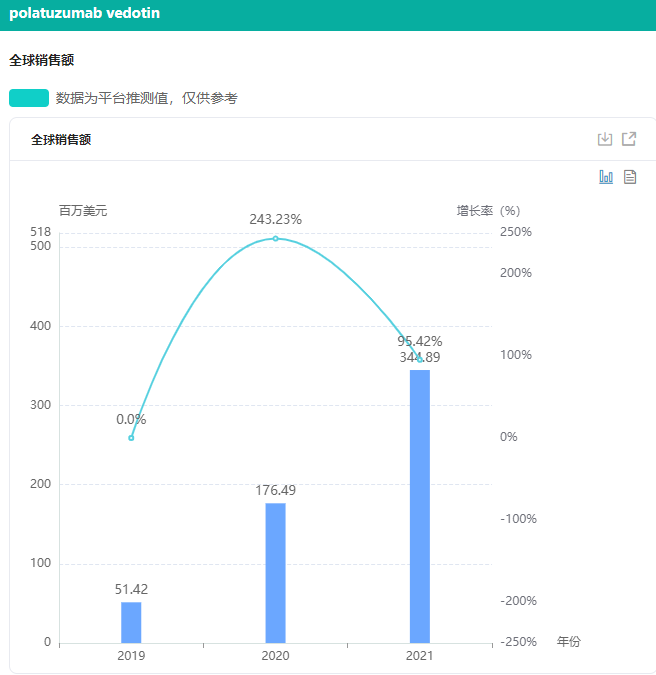
截图来源:药融云全球药物研发数据库
曲妥珠单抗注射液(皮下注射)
2021年4月,NMPA承办了曲妥珠单抗注射液(皮下注射)上市申请。据悉,这是罗氏制药开发的一款皮下注射型赫赛汀,商品名为Herceptin Hylecta,已于2019年2月在美国获批用于HER2阳性早期乳腺癌患者。
曲妥珠单抗注射液(皮下注射)上市时间轴
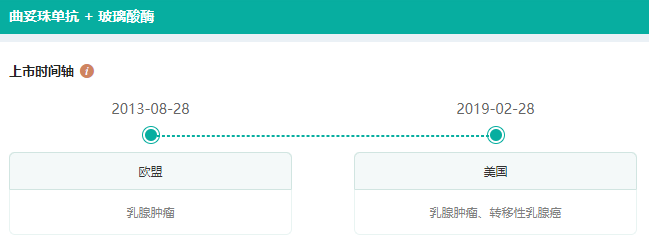
曲妥珠单抗上市时间轴
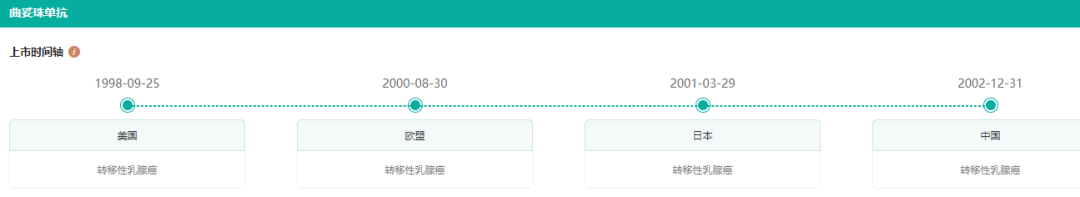
截图来源:药融云全球药物研发数据库
曲妥珠单抗是第一个批准用于治疗HER2阳性转移性乳腺癌和早期乳腺癌的单克隆抗体,广泛用于各期HER2阳性乳腺癌治疗,原研来自罗氏制药,是其重磅肿瘤学“三驾马车”之一。据罗氏制药早前新闻稿信息,曲妥珠单抗注射液(皮下注射)这种新剂型疗法是一种即用型制剂,可以在2至5分钟内完成给药,而静脉用赫赛汀需要30至90分钟。
2002年,罗氏制药曲妥珠单抗获批进入中国市场。2017年,曲妥珠单抗以65%的降幅进入医保目录,由此快速放量。据药融云统计,2021年国内曲妥珠单抗院内销售额达53.6亿元,根据今年第一季度的销售表现,市场还将进一步扩大。
注射用曲妥珠单抗院内销售情况
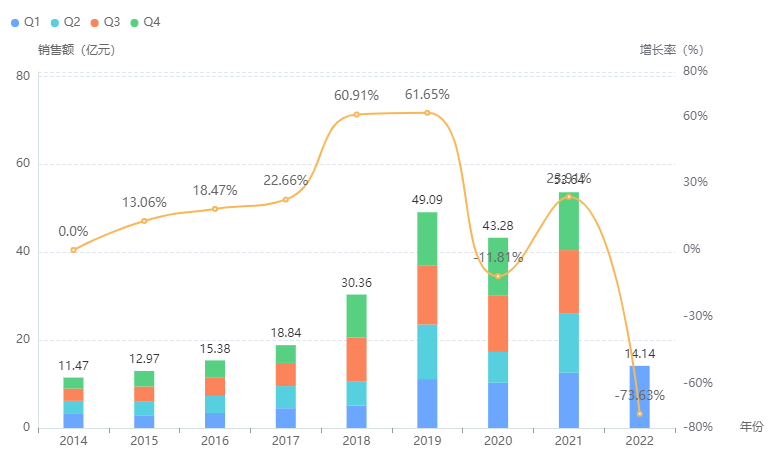
截图来源:药融云全国医院销售数据库
目前国内已有复宏汉霖研发的曲妥珠单抗生物类似药获批上市,值得注意的是,三生国健所研发的重组抗HER2人源化单克隆抗体伊尼妥单抗也已经于2020年获批上市,但根据三生国健所招股说明书中披露的内容,其不属于曲妥珠单抗的生物类似药。此外上海生物制品研究所、嘉和生物、正大天晴、华兰基因工程、海正药业、安科生物等企业的曲妥珠单抗生物类似药已处于III期临床阶段。
参考来源:
[1] NMPA官网
[2] 药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

—END—























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论