
据CDE官网最新公示,百济神州递交了替雷利珠单抗注射液(皮下注射)的临床申请并获受理,注册分类为2.1类。据公开信息,目前默沙东、辉瑞、罗氏、恒瑞、君实生物等国内外药企均已布局PD-(L)1的皮下注射剂型。

截图来源:CDE官网
2022国内最畅销PD-1,首款出海进行时
替雷利珠单抗(商品名:百泽安)是一款人源化IgG4抗PD-1单克隆抗体,设计目的旨在最大限度地减少与巨噬细胞中的Fcγ受体结合,帮助人体免疫细胞识别并杀伤肿瘤细胞,最早于2019年12月获NMPA批准上市,用于治疗淋巴瘤。
随后替雷利珠陆续获批包括尿路上皮癌、NSCLC、肝癌、食管癌、鼻咽癌在内的多项适应症,今年5月,替雷利珠第11项适应症获批上市,联合化疗用于一线治疗不可切除的局部晚期、复发或转移性食管鳞状细胞癌(ESCC)。
据药融云数据库,替雷利珠还有多项II期、III期临床试验开展中,适应症包括头颈部鳞状细胞癌、宫颈癌等。其递交的第12项适应症:治疗一线不可切除或转移性肝细胞癌(HCC)正在审评中

截图来源:药融云中国药品审批数据库
据百济神州财报数据,替雷利珠单抗近年来一直保持稳定的增长状态:2020年替雷利珠单抗的销售额为1.634亿美元;2021年为2.551亿美元,增速约56%;2022年于中国市场实现销售额约合28.98亿元人民币,同比增长66%。
截至5月底,替雷利珠单抗在国内累计获批11项适应症,超过了恒瑞医药的卡瑞利珠单抗(艾瑞卡)。同时,据业内人士分析,从销售额来看,2022年替雷利珠单抗已超过卡瑞利珠单抗,成为国内PD-1药物最畅销的品种。
替雷利珠单抗已经在全球8个国家或地区递交新药上市申请。其中FDA正在审评替雷利珠单抗用于二线治疗ESCC的新药上市申请,百济神州还将携手诺华尽早推动相关现场核查工作,FDA或将于今年内做出审评决议。这意味着替雷利珠单抗将成为走向国际市场的首款国产PD-1。
与此同时,欧洲药品管理局人用药品委员会(CHMP)也于7月发布其推荐替雷利珠单抗注射液获得上市许可的积极意见,建议批准替雷利珠单抗注射液单药用于治疗既往接受过含铂化疗的不可切除、局部晚期或转移性食管鳞状细胞癌(ESCC)成人患者。距离替雷利珠单抗在欧盟上市,仅差“临门一脚”了。
PD-1内卷新形态,MSD、罗氏、BMS、恒瑞领跑
截至2023年3月底,国内已有16个PD-(L)1产品获批上市,其中有10款PD-1单抗(8款国产,2款进口)。其中,默沙东的博利珠单抗2022年全球销售额已超200亿美元。
8 月 1 日,默沙东公布了 2023 年 Q2 业绩,其K 药帕博利珠单抗Q2 销售额分别为 62.71 亿美元(+19%),H1共实现120.65 亿美元销售额,提前锁定 2023 年药王宝座(据艾伯维半年报,修美乐H1销售额 75.53 亿美元,同比下滑 25.2%)。
实际上,除了不断拓展适应症,国内外药企针对PD-(L)1的布局还体现在剂型方面,除了百济神州的替雷利珠,多家药企均布局有皮下注射剂型。相比于静脉注射剂型,皮下注射抗PD-1单抗有望缩短治疗时间,提高治疗依从性和便利性。
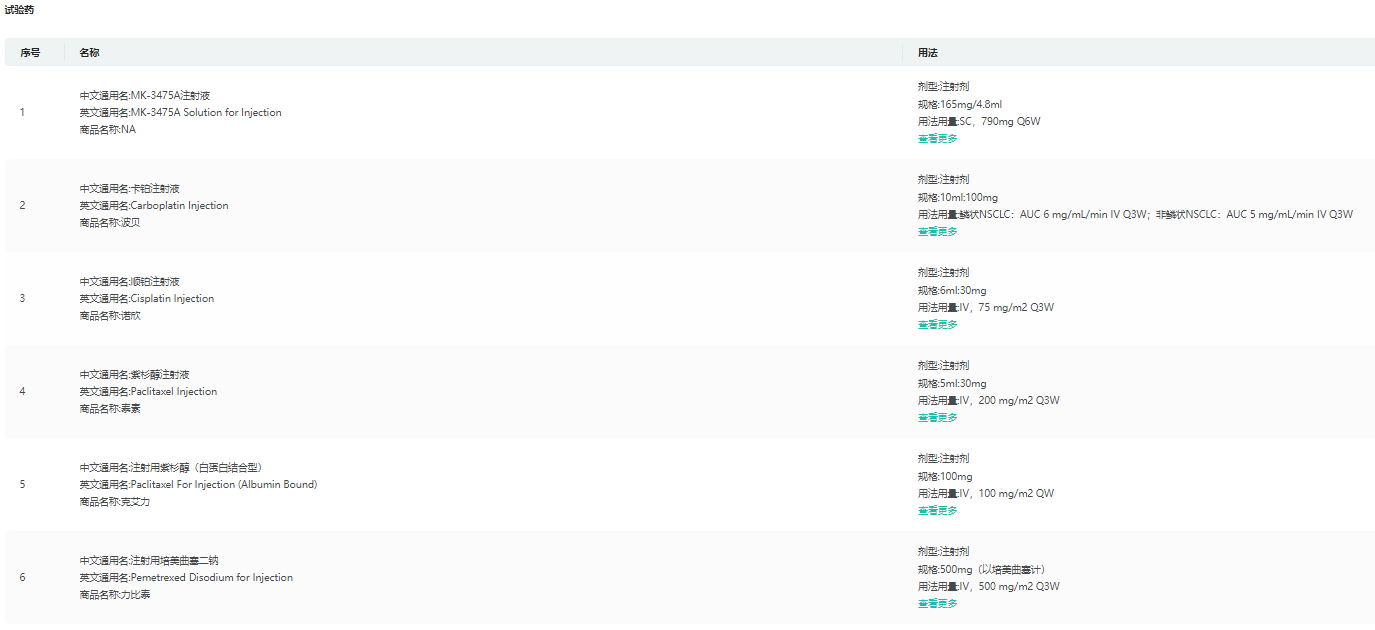
4月12日,据中国药物临床试验登记与信息公示平台显示,默沙东已经启动了PD-1单抗MK-3475A注射液的一项国际多中心3期临床试验的中国部分(登记号:CTR20231113),拟用于治疗转移性非小细胞肺癌一线治疗。公开资料显示,MK-3475A由帕博利珠单抗与透明质酸酶组成,为皮下注射(SC)剂型。

截图来源:药融云中国临床试验
 截图来源:药融云中国临床试验
截图来源:药融云中国临床试验
2月16日,歌礼口头报告了其皮下注射抗PD-L1抗体ASC22(恩沃利单抗)对照安慰剂队列的最终数据,显示ASC22可以实现慢性乙型肝炎功能性治愈。7月25日,歌礼宣布了ASC22联合西达本胺用于人类免疫缺陷病毒(HIV)感染功能性治愈的2期临床结果。目前,该产品治疗微卫星高度不稳定(MSI-H)或错配修复基因缺陷型(dMMR)晚期实体瘤的适应症已在中国获批。
2022年12 月 1 日,罗氏宣布其 PD-L1 单抗阿替利珠单抗(Tecentriq)皮下注射制剂的 III 期 IMscin001 研究的最新关键数据。从给药时间来看,与标准静脉输注所需 30-60 分钟相比,皮下给药可将每次注射的治疗时间缩短至仅需 7 分钟。罗氏已向全球监管机构提交了 IMscin001 研究数据,并为阿替利珠单抗皮下制剂寻求批准静脉输注剂型的所有获批适应症。
此外还有百时美施贵宝的纳武利尤单抗(Opdivo)、辉瑞的Sasanlimab、恒瑞医药的 SHR-1901 、君实生物的 JS001sc 注射液等皮下注射品种已登记开展相关临床试验。
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论