
10月13日,百济神州宣布,美国食品药品监督管理局(FDA)已授予索托克拉突破性疗法认定(BTD),用于治疗复发或难治性(R/R)套细胞淋巴瘤(MCL)成人患者。
此外,FDA已接受百济神州参加Orbis计划的申请。在该计划的框架下,抗肿瘤药物可向参与的全球卫生管理部门同时递交申请并接受审评。

索托克拉是一款新一代且具有同类最优潜力的在研B细胞淋巴瘤2(BCL2)抑制剂,BCL2是帮助肿瘤细胞存活的几种蛋白质之一。索托克拉类属BH3类似物,可模拟自然细胞死亡信号。实验室和早期药物开发研究结果表明,索托克拉是一种具有强效性和特异性的BCL2抑制剂,半衰期短且无蓄积。索托克拉在多种B细胞恶性肿瘤中表现出良好的临床活性。迄今为止,共有近2,000例患者入组了该药物全球开发项目。
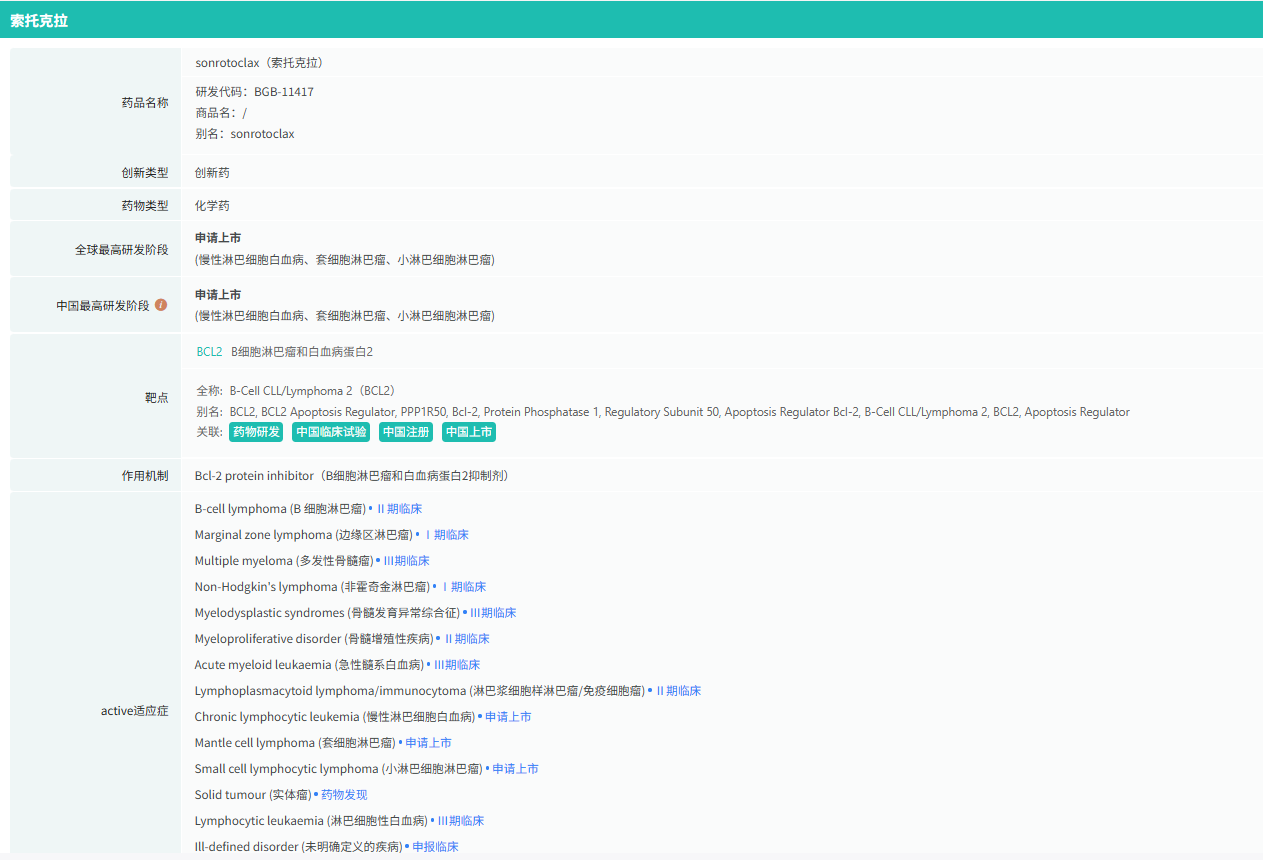
截图来源:摩熵医药数据库
FDA授予索托克拉BTD认定并批准参加Orbis计划,该决定基于BGB-11417-201的研究数据。BGB-11417-201是一项在接受过布鲁顿酪氨酸激酶抑制剂(BTKi)和抗CD20疗法治疗的R/R MCL成人患者中评价索托克拉治疗的1/2期研究。该研究近期公布的积极结果显示索托克拉有潜力提供深度和持久的缓解,有望成为首款且唯一一款在美国获批治疗R/R MCL的BCL2抑制剂。。3期确证性临床研究CELESTIAL-RRMCL(BGB-11417-302;NCT06742996)正在进行中。
据新闻稿披露,这是索托克拉获得的首个突破性疗法认定,也是百济神州血液瘤研发管线获得的第二个突破性疗法认定。
此外,FDA还授予索托克拉用于治疗MCL和华氏巨球蛋白血症(WM)成人患者的快速通道认定,以及用于治疗MCL、WM、多发性骨髓瘤(MM)和急性髓系白血病(AML)的成人患者的孤儿药认定。
参考来源:
[1] 企业官方披露
[2] 摩熵医药(原药融云)数据库
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论