
2023年8月14日,Taysha Gene Therapies(纳斯达克:TSHA)是一家临床阶段的基因治疗公司,专注于开发和商业化基于aav的基因疗法,用于治疗中枢神经系统(CNS)的单基因疾病。宣布完成融资为1.5亿美元(约10.9亿人民币)。本轮融资由RA Capital Management牵头,新老投资者参与,公司预计现金跑道可以延长到2025年第三季度。
同时Taysha报告了第一名成年rett综合征患者在1/2期临床试验中的积极的初步临床数据,并提供了公司2023年第二季度财务业绩的最新数据:上半年营收710万美元,研发费用支出3231万美元。
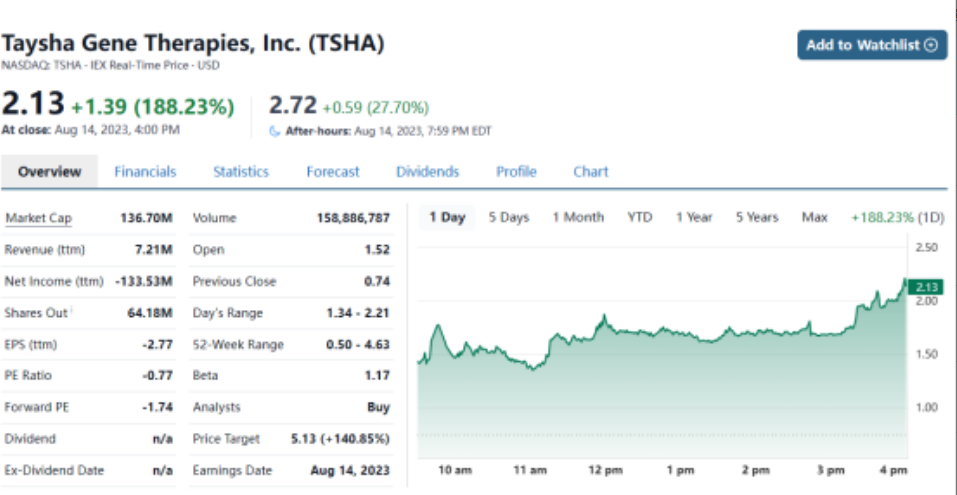
受到融资和临床数据消息刺激,Taysha Gene Therapies股价大涨188%,该公司2020年在美国纳斯达克上市,目前市值1.36亿美元。
TSHA-102:一种自体补充鞘内递送AAV9基因转移疗法用于Rett综合征的临床评估,TSHA-102利用一种新型的miRARE平台,旨在介导CNS中每个细胞的MECP2水平,而不会有过表达的风险。TSHA-102已获得FDA的孤儿药和罕见儿科疾病指定,并已获得欧盟委员会的孤儿药指定。
TSHA-102正在REVEAL 1/2期临床试验中进行评估,这是一项首次人体、开放标签、随机、剂量递增和剂量扩展研究,评估TSHA-102治疗因MECP2功能丧失突变而患Rett综合征的成年女性的安全性和初步疗效。主要疗效终点是临床医生使用临床整体印象量表-改善(CGI-I), Rett综合征手功能量表和修订运动行为评估(R-MBA)对患者进行评估。次要终点包括临床医生和护理人员使用临床总体印象量表-严重程度(CGI-S)、Rett综合征行为问卷(RSBQ)和其他临床评估量表对患者进行评估。
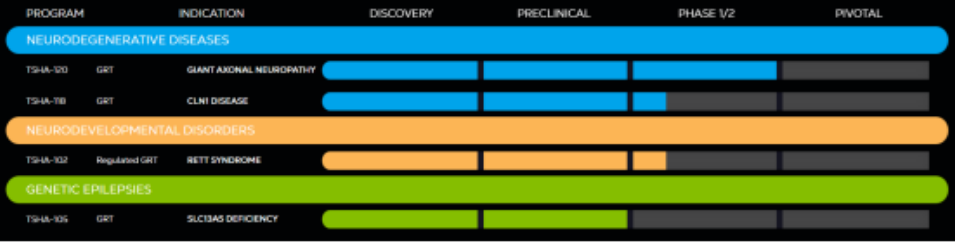
Taysha的在研管线
在REVEAL 1/2期临床试验中首次给药的成年患者的数据显示,TSHA-102耐受性良好,截至6周的评估和关键疗效指标的改善,包括临床总体印象-改善(CGI-I)、临床总体印象-严重程度(CGI-S)和Rett综合征行为问卷(RSBQ),治疗后4周,首席研究员(PI)观察到多个领域的临床改善。包括自主神经功能(睡眠和呼吸),发声,以及大运动技能(获得了独立坐三分钟的能力)和精细运动技能(获得了拿东西的能力),这些都有初步的临床数据和视频证据支持。
“我们对本季度我们在两个主要研究项目的临床评估中取得的进展感到高兴。对于治疗Rett综合征的TSHA-102,我们相信,在治疗后4周,在第一位患有严重疾病的成年患者身上看到的初步安全性和显著的临床改善,加强了我们的基因疗法在解决Rett综合征根本原因方面的变革潜力。重要的是,这些早期数据表明miRNA-Responsive Auto-Regulatory Element (miRARE)技术在CNS中以细胞为基础介导MECP2表达,支持miRARE的调控控制。我们对TSHA-102的初步数据感到非常鼓舞,并专注于继续探索其治疗潜力,第二名患者的给药预计将在第三季度进行”
Taysha董事长兼首席执行官Sean P. Nolan表示,“我们还获得了FDA批准,开始在美国儿科患者中开展TSHA-102的临床开发,并已向MHRA提交了TSHA-102用于Rett综合征儿科患者的CTA,这将扩大我们的临床评估到早期疾病进展阶段的儿童。”“对于GAN中的TSHA-120,我们利用疾病进展模型(DPM)的新的综合数据分析已提交给FDA,我们计划在第三季度与该机构一起审查TSHA-120的潜在监管途径。”
药融云数据库关于Taysha临床试验情况
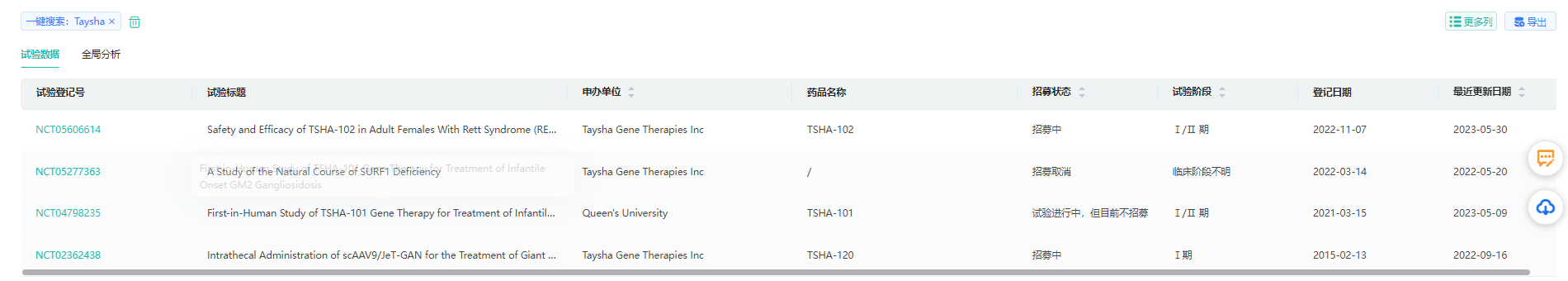
截图来源:药融云全球临床实验数据库
Rett综合征(Rett syndrome, RTT)是一种X染色体连锁遗传性神经发育障碍,Mecp2基因突变是导致RTT的重要原因。该疾病的特征是智力残疾、沟通障碍、癫痫发作、发育迟缓和/或倒退、运动和呼吸障碍以及预期寿命缩短。据估计,在美国、欧盟和英国,由致病性/可能致病性MECP2突变引起的Rett综合征影响了1.5万至2万名患者。
参考资料:
公司官网
药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!




































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)


















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论