 2024年2月27日,Cytokinetics公司(纳斯达克股票代码:CYTK)公布了第四季度及2023年全年财报:2023年公司总营收为753万美元,同比下降92%;2023 Q4总营收167.2万美元,同比下降15%,收入减少的主要原因是2022年确认了8700万美元的递延收入,这是含mavacamten产品净销售额的特许权使用费,是特许权使用费义务解除的结果。
2024年2月27日,Cytokinetics公司(纳斯达克股票代码:CYTK)公布了第四季度及2023年全年财报:2023年公司总营收为753万美元,同比下降92%;2023 Q4总营收167.2万美元,同比下降15%,收入减少的主要原因是2022年确认了8700万美元的递延收入,这是含mavacamten产品净销售额的特许权使用费,是特许权使用费义务解除的结果。

2023年全年净亏损和2023 Q4净亏损分别为5.262亿美元和1.369亿美元;2022年同期净亏损为3.89亿美元和1.374亿美元 。截至2023年12月31日,现金、现金等价物和投资总额为6.554亿美元。
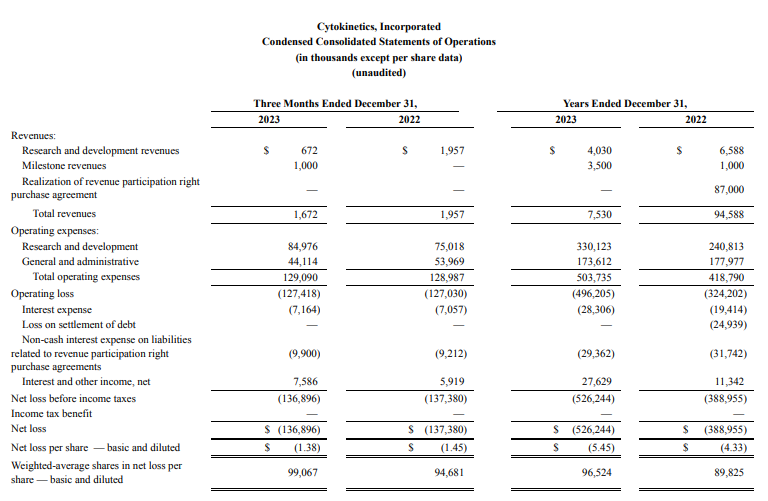
该公司宣布了2024年的财务指导,预计收入将在300万至500万美元之间,运营支出将在4.2亿至4.5亿美元之间,净现金利用率约为3.9亿至4.2亿美元。
Cytokinetics在近期实现的进展主要有:
Aficamten(心肌肌球蛋白抑制剂):12月,Cytokinetics宣布了Aficamten在有症状的梗阻性肥厚型心肌病(HCM)患者中进行的关键3期临床试验 SEQUOIA-HCM的积极顶线结果。1月,在CMR 2024大会上公布了FOREST-HCM(Aficamten对HCM持续治疗的随访、开放标签研究评估)的最新长期数据。2月与FDA举行会议,讨论SEQUOIA-HCM的初步结果,并为提交新药申请 (NDA) 做准备。继续在MAPLE-HCM研究中招募患者,该3期临床试验比较了在症状性阻塞性HCM患者中单药aficamten治疗与单药美托洛尔治疗的效果。
omecamtiv mecarbil(心肌酶激动剂):2023 Q4收到欧洲药品管理局 (EMA) 关于omecamtiv mecarbil上市许可申请 (MAA) 的第180天未决问题清单,并于2024年第一季度提交答复。向FDA新药办公室提出的正式争议解决请求 (FDRR) 遭拒,该请求与我们收到的针对omecamtiv mecarbil新药上市许可申请的完整答复函 (CRL) 有关,FDA表示需要至少两项充分且对照良好的临床研究提供证据。
CK-4021586(CK-586,心肌酶抑制剂):在健康参与者中开展CK-586 1期研究的多剂量递增(MAD)队列。
CK-3828136(CK-136,心肌肌钙蛋白激活剂):在健康参与者中开展CK-136第一阶段研究的多剂量组群。
2024年预计实现的里程碑有:
aficamten预计在2024 Q2的医学会议上展示SEQUOIA-HCM 的主要研究成果。预计在2024 Q3向FDA提交新药申请 (NDA),在2024 Q4向欧洲药品管理局 (EMA) 提交上市许可申请 (MAA)。在2024 Q3完成MAPLE-HCM的注册。继续推进aficamten的上市战略。
omecamtiv mecarbil预计CHMP将于2024 Q2就omecamtiv mecarbil的 MAA发表意见。
CK-4021586将于2024 Q2分享CK-586 1期研究数据。
CK-3828136预计在2024 Q2完成CK-136的第一阶段研究。
Cytokinetics公司总裁兼首席执行官Robert I. Blum表示:“我们在2023年结束时取得了SEQUOIA-HCM的积极成果,这将推动我们公司进入下一阶段的规划,实现我们的专科心脏病学业务模式。在我们准备aficamten的监管申请时,我们正在开展商业准备活动,同时还在oHCM和nHCM患者中开展3期临床试验,我们相信这将进一步为我们的下一步目标提供证据支持,以帮助更多的肥厚型心肌病患者。凭借强大的资产负债表、充裕的现金流和多种资金渠道,我们很高兴能为 Cytokinetics 和所有利益相关者翻开新的一页。”
公司管线
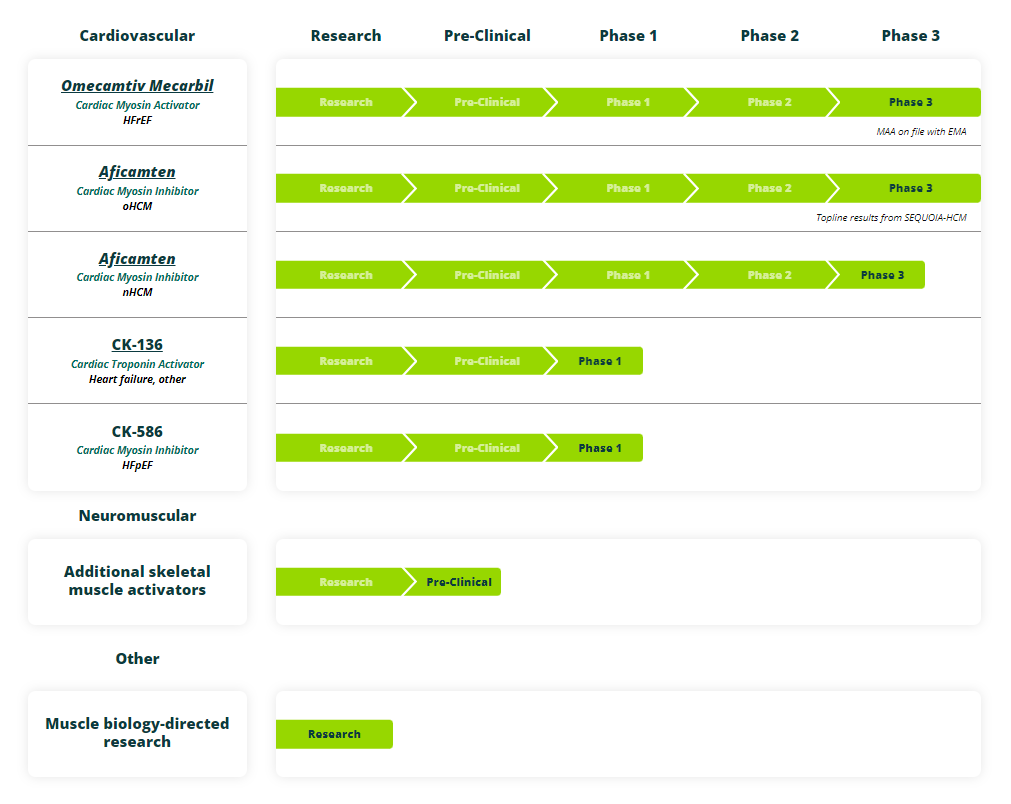 2020年7月,箕星药业引进Aficamten的大中华区权益,在中国处于三期临床阶段。
2020年7月,箕星药业引进Aficamten的大中华区权益,在中国处于三期临床阶段。

<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论